
Кальций и магний
Мы уже неоднократно имели возможность заметить, что один и тот же металл выполняет несколько биохимических обязанностей: железо переносит кислород и электроны, медь участвует в аналогичных процессах, цинк способствует гидролизу полипептидов и разложению бикарбонатов и т. д.
Но кальций побивает в этом отношении все рекорды. Ионы кальция образуют защитные оболочки у кораллов, скопления которых достигают громадных размеров; кальций необходим для работы ферментов, обеспечивающих мышечную деятельность; кальций регулирует систему свертывания крови, активирует некоторые ферменты; он же входит в состав костей и зубов у позвоночных и т. д.
Круговороту кальция способствует различная растворимость его углекислых солей: карбонат СаСО3 мало растворим в воде, а гидрокарбонат Са(НСО3)2 растворим довольно хорошо, причем концентрация его в растворе зависит от концентрации диоксида углерода и, следовательно, от парциального давления этого газа над раствором; поэтому, когда углекислые воды горных источников вытекают на поверхность земли и теряют диоксид углерода (углекислый газ), карбонат кальция выделяется в виде осадка, образуя кристаллические сростки (сталактиты и сталагмиты в пещерах). Микроорганизмы осуществляют аналогичный процесс, извлекая из морской воды гидрокарбонат и используя карбонат для строительства защитных оболочек.
В организмах высших животных кальций также выполняет функции, связанные с созданием механически прочных структур. В костях кальций содержится в виде солей, близких по составу к минералу апатиту 3Са3(РO4)2*CaF2(Cl). Символ хлора в скобках указывает на частичное замещение фтора на хлор в этом минерале.
Формирование костной ткани происходит под влиянием витаминов группы D; эти витамины, в свою очередь, синтезируются в организмах под влиянием ультрафиолетового излучения Солнца. Значительное количество витамина D имеется в рыбьем жире, поэтому при дефиците витамина в детском питании кальций не всасывается в кишечнике и развиваются симптомы рахита; врачи назначают в качестве лекарства рыбий жир или чистые препараты витамина D. Избыток этого витамина очень опасен: он может вызвать обратный процесс - растворение костной ткани!
Из пищевых продуктов кальций содержится в молоке, молочных продуктах (особенно много его в твороге, так как белок молока казеин связан с ионами кальция), а также в растениях.
Белки, имеющие небольшую молекулярную массу (около 11000) и содержащиеся в мышцах рыб, проявляют способность активно захватывать ионы кальция. Некоторые из них (например, альбумин карпа) были тщательно изучены; их состав оказался необычным: они содержат много аминокислоты аланина и фенилаланина и вовсе не содержат гистидина, цистеина и аргинина - почти неизменных составных частей других белков.
Для комплексных соединений иона кальция характерно образование мостиков - ион связывает преимущественно карбоксильные и карбонильные группы в образующемся комплексе.
Координационное число иона кальция велико и достигает восьми. Эта его особенность, по-видимому, лежит в основе действия фермента рибонуклеазы, который катализирует важный для организма процесс гидролиза нуклеиновых кислот (РНК), сопровождающийся освобождением энергии. Предполагают, что ион кальция образует жесткий комплекс, сближая друг с другом молекулу воды и фосфатную группу; находящиеся в окружении иона кальция остатки аргинина способствуют фиксации фосфатной группы. Она поляризуется кальцием и легче подвергается атаке со стороны молекулы воды. В результате фосфатная группа отщепляется от нуклеотида. Было доказано также, что ион кальция в этой ферментной реакции нельзя заменить на другие ионы с той же степенью окисления.
Ионы кальция активируют и другие ферменты, в частности α-амилазу (катализирует гидролиз крахмала), но в этом случае кальций все же можно заменить в искусственных условиях трехзарядным ионом металла неодима.
Кальций является и важнейшим компонентом той удивительной биологической системы, которая больше всего походит на машину, - системы мышц. Эта машина производит механическую работу за счет химической энергии, заключенной в веществах пищи; ее коэффициент полезного действия высок; она почти мгновенно может быть переведена из состояния покоя в состояние движения (причем в покое энергия не расходуется); ее удельная мощность около 1 кВт на 1 кг массы, скорость движений хорошо регулируется; машина вполне пригодна для длительной работы, требующей повторяющихся движений, срок службы около 2,6*106 операций. Примерно так описал мышцу проф. Уилки в популярной лекции, добавив еще, что машина ("линейный двигатель") может служить пищей.
Ученым очень трудно было выяснить, что же происходит внутри этого "линейного двигателя", каким образом химическая реакция порождает целенаправленное движение и какую роль играют во всем этом ионы кальция. В настоящее время установлено, что мышечная ткань состоит из волокон (вытянутых клеток), окруженных мембраной (сарколеммой). В мышечных клетках находятся миофибриллы - сократительные элементы мышцы, которые погружены в жидкость - саркоплазму. Миофибриллы состоят из сегментов - саркомеров. В саркомерах находится система из нитей двух типов - толстых и тонких.
Толстые нити состоят из белка миозина. Молекулы миозина представляют собой вытянутые частицы, имеющие на одном конце утолщение - головку. Головки выступают над поверхностью нитеобразной молекулы и способны располагаться под различными углами к оси молекулы. Молекулярная масса миозина равна 470000.
Тонкие нити образованы молекулами белка актина, имеющими сферическую форму. Молекулярная масса актина - 46000. Частицы актина расположены так, что получается длинная двойная спираль. Каждые семь молекул актина связаны нитеобразной молекулой белка тропомиозина, несущей на себе (ближе к одному из концов) шарообразную молекулу еще одного белка - тропонина (рис. 19). Тонкая нить скелетной мышцы содержит до 400 молекул актина и до 60 молекул тропомиозина. Таким образом, работа мышцы основывается на взаимодействии деталей, построенных из четырех белков.
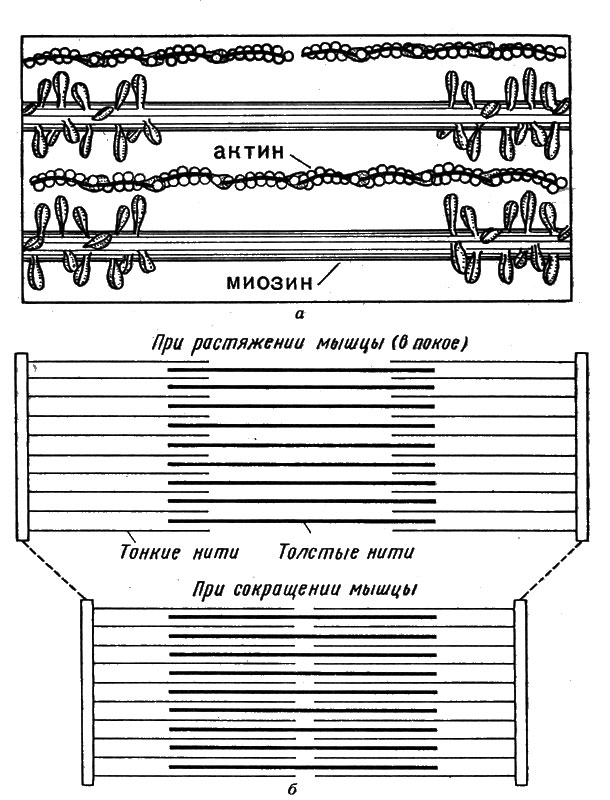
Рис. 19. Механизм мышечного сокращения: а - мостики между нитями актина и миозина; б - мышца расслабленная и мышца в состоянии сокращения: нити актина вдвинуты между нитями миозина
Перпендикулярно осям нитей располагаются белковые образования - z-пластинки, к которым прикрепляются одним концом тонкие нити. Толстые нити размещены между тонкими. В расслабленной мышце расстояние между z-пластинками составляет приблизительно 2,2 мк. Сокращение мышцы начинается с того, что под влиянием нервного импульса выступы (головки) молекул миозина прикрепляются к тонким нитям и возникают так называемые сшивки, или мостики. Головки толстых нитей по обе стороны пластинки наклонены в противоположные стороны, поэтому, поворачиваясь, они втягивают тонкую нить между толстыми, что и приводит к сокращению всего мышечного волокна.
Источником энергии для работы мышцы является реакция гидролиза аденозинтрифосфорной кислоты (АТФ); присутствие этого вещества необходимо для работы мышечной системы.
В 1939 г. В. А. Энгельгардт и М. Н. Любимова доказали, что миозин и комплекс его с актином - актомиозин являются катализаторами, ускоряющими гидролиз АТФ в присутствии ионов кальция и калия, а также магния, который вообще часто облегчает гидролитические реакции. Особая роль кальция заключается в том, что он регулирует образование сшивок (мостиков) между актином и миозином. Молекула АТФ присоединяется к головке молекулы миозина в толстых нитях. Затем происходит какое-то химическое изменение, приводящее этот комплекс в активное, но неустойчивое состояние. Если такой комплекс вступит в соприкосновение с молекулой актина (на тонкой нити), то произойдет освобождение энергии вследствие реакции гидролиза АТФ. Эта энергия и заставляет мостик отклониться и подтянуть толстую нить ближе к белковой пластинке, т. е. вызвать сокращение мышечного волокна. Далее к актин-миозиновому комплексу присоединяется новая молекула АТФ, и комплекс немедленно распадается: актин отделяется от миозина, мостик более не связывает толстую нить с тонкой - мышца расслабляется, а миозин и АТФ остаются связанными в комплекс, находящийся в неактивном состоянии.
Ионы кальция содержатся в трубочках и пузырьках, окружающих одиночное мышечное волокно. Эта система трубочек и пузырьков, образованная тонкими мембранами, называется саркоплазматической сетью; она погружена в жидкую среду, в которой и находятся нити. Под влиянием нервного импульса изменяется проницаемость мембран, и ионы кальция, покидая саркоплазматическую сеть, выходят в окружающую жидкость. Предполагается, что ионы кальция, соединяясь с тропонином, влияют на положение нитевидной молекулы тропомиозина и переводят ее в такое положение, при котором активный комплекс АТФ - миозин может присоединиться к актину. По-видимому, регуляторное влияние ионов кальция распространяется с помощью нитей тропомиозина сразу на семь молекул актина.
После сокращения мышцы кальций очень быстро (доли секунды) удаляется из жидкости, вновь уходя в пузырьки саркоплазматической сети, и мышечные волокна расслабляются. Следовательно, механизм работы "линейного двигателя" заключается в попеременном вдвигании системы толстых миозиновых нитей в пространство между тонкими нитями актина, прикрепленными к белковым пластинкам, причем этот процесс регулируется ионами кальция, периодически появляющимися из саркоплазматической сети и снова уходящими в нее.
Ионы калия, содержание которого в мышце гораздо больше содержания кальция, способствуют превращению глобулярной формы актина в нитчатую - фибриллярную: в таком состоянии актин легче взаимодействует с миозином.
С этой точки зрения становится понятным, почему ионы калия усиливают сокращение мышцы сердца, почему они необходимы вообще для развития мышечной системы организма.
Ионы кальция - деятельные участники процесса свертывания крови. Нет надобности говорить, насколько важен этот процесс для сохранения жизни организма. Если бы кровь была лишена способности свертываться, ничтожная царапина представляла бы серьезную угрозу жизни. Но в нормальном организме кровотечение из небольших ран прекращается уже через 3-4 мин. На поврежденных тканях образуется плотный сгусток белка фибрина, закупоривающий рану. Исследование образования кровяного сгустка показало, что в его создании принимают участие сложные системы, включающие несколько белков и специальных ферментов. Не менее 13 факторов должны действовать согласованно для правильного хода всего процесса.
При повреждении сосуда кровеносной системы в кровь поступает белок тромбопластин. Ионы кальция принимают участие в действии этого белка на вещество, называемое протромбином (т. е. "источником тромбина"). Еще один белок (из класса глобулинов) ускоряет превращение протромбина в тромбин. Тромбин действует на фибриноген - высокомолекулярный белок (его молекулярная масса около 400000), молекулы которого имеют нитевидное строение. Фибриноген образуется в печени и является растворимым белком. Однако под влиянием тромбина он превращается сначала в мономерную форму, а затем полимеризуется, и получается нерастворимая форма фибрина - тот самый сгусток, который и прекращает кровотечение. В процессе образования нерастворимого фибрина опять участвуют ионы кальция.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'