
Соли
Одним из самых широко используемых соединений меди (II) является ее сульфат - CuSO4. Существует несколько форм кристаллогидратов: CuSO4·nH2O, где n равно 1, 3, 5, 6 и 7. Наиболее устойчивым из них является пентагидрат CuSO4 · 5H2O, его можно представить и как комплексное соединение [Cu(H2O)4]SO4 · H2O. Медный купорос хорошо растворим в воде. При нагревании он дегидратирует:
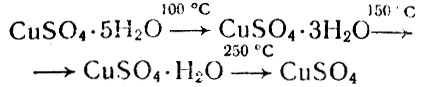
Водные растворы и кристаллогидраты сульфата меди (II) имеют синий или голубой цвет, а безводный сульфат CuSО4 бесцветный. Безводный CuSО4 жадно поглощает воду. Такое свойство позволяет использовать его как осушитель.
Сульфат меди (II) при нагревании восстанавливается водородом, углеродом и оксидом углерода (II). Соль CuSО4 служит исходным продуктом для получения других соединений меди, применяется в гальванопластике, используется в качестве антисептика, в сельском хозяйстве для борьбы с вредителями.
Сульфид меди (II) черного цвета, в воде нерастворим, но легко растворяется в серной и азотной кислоте:
CuS + 2H2SО4 = CuSО4 + SО2 + S + 2H2О
6CuS + 22HNO3 = 6Cu(NO3)2 + 3H2SO4 + 3S + 10NO + 8H2O CuS в природе встречается в виде минерала ковелина, а в лаборатории может быть получен действием сероводорода на растворы солей меди (II).
CuSО4 + H2S→CuS + H2SO4
Эти реакции используются в аналитической химии в ходе количественного определения Сu (II).
Другой реакцией, используемой при определении меди в сплавах и рудах, является взаимодействие Сu(II) с иодидом калия:
CuSO4 + 4KI→2CuI + I2 + 2K2SO4
Иодид меди (I) выпадает в осадок, а жидкость окрашивается иодом в бурый цвет.
Эта реакция происходит из-за того, что иодид меди (II), который получается первоначально, неустойчив и быстро разлагается:
2CuI2→2CuI + I2
Выделившийся иод можно оттитровать тиосульфатом натрия и тем самым определить имевшуюся в растворе концентрацию ионов меди (II):
I2 + 2Na2S2O3→2NaI + Na2S4O6
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'