
Биологические функции меди
В растительных и животных организмах содержание меди колеблется в широких пределах от 10-5 до 10-3 % в расчете на сырое вещество. Особенно богаты медью некоторые беспозвоночные - моллюски и членистоногие (крабы, осьминоги, кальмары). Еще в 1847 г. А. Харлесс, исследуя голубую кровь улитки, пришел к выводу, что голубой цвет обусловлен содержанием в крови меди. Было установлено, что медь находится в ионном состоянии и входит в состав белка, названного "гемо-цианином", что означает по-гречески "синекровный". Гемоциаиины различных организмов имеют молекулярную массу от 36 000 до 825 000 и содержат 0,15- 0,25 % меди.
В составе гемоцианина медь находится в степени окисления +1.
Ее функции состоят в переносе кислорода и электронов. Предполагается, что два иона меди связывают одну молекулу кислорода. Точный состав комплексного соединения меди в гемоцианине пока неизвестен. Вероятно, что медь связана с аминогруппами или дисульфидными мостиками полипептидной белковой цепи. Число активных центров (т. е. пар ионов меди, связывающих одну молекулу кислорода) гемоцианина у членистоногих всего 6, тогда как у моллюсков оно может достигать 200.
Белки, содержащие медь, широко распространены в природе. Они играют роль переносчиков электронов и катализируют реакции гидроксилирования и окисления. Особенно важны медьсодержащие ферменты, ускоряющие реакции окисления, т. е. оксидазы. Оксидазы, в молекуле которых содержится не менее четырех атомов меди на молекулу фермента, ускоряют восстановление кислорода до воды. Их синяя окраска интенсивна настолько, что эту группу оксидаз иногда называют "синие" оксидазы, в отличие от другой группы медьсодержащих оксидаз, в молекуле которых всего один-два атома меди ("несиние" оксидазы). Последние окрашены менее ярко и катализируют восстановление кислорода до пероксида водорода. К синим оксидазам относится, например, церулоплазмин - медьсодержащий белок, найденный в плазме человека и многих позвоночных. Церулоплазмин катализирует окисление ионов железа (II) в ионы железа (III), а также реакции окисления полиаминов и полифенолов - обычных составных частей обмена веществ в организмах. На одну молекулу белка приходится 6 атомов меди, причем половина из них находится в степени окисления +2, а остальные в степени окисления + 1.
Действие ионов меди в реакциях окисления сводится к попеременному окислению и восстановлению, т. е. к переходам типа:
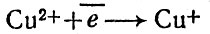
Показано, что ионы Сu2+ обратимо окисляются и восстанавливаются по указанной схеме, а ионы Сu+ окисляются очень трудно и только при разрушении белковой части фермента. В животном организме медь концентрируется преимущественно в печени (в виде белков гемокупреина и гепатокупреина). Значительно повышая интенсивность окислительно-восстановительных процессов, медь оказывает стимулирующее влияние на дыхание и фотосинтез, углеводный обмен, синтез гемоглобина и жиров, образование витаминов Р и В.
Недостаток меди в организме ведет к развитию анемии. Однако ее избыток также вреден и может повлечь за собой тяжелые заболевания печени. Ядовитое действие (в больших концентрациях) меди на низшие растительные организмы используют для борьбы с грибками, паразитирующими на культурных растениях (яблонях, винограде и др.). С этой целью зараженные растения опрыскивают растворами солей меди.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'