
Калориметрия
Калориметрия (буквально означает "измерение тепла") - основной экспериментальный метод термохимии. Предназначен для точного измерения количества тепловой энергии, выделяемой или поглощаемой в химических, физических или биологических процессах. Эти результаты позволяют заранее, до постановки химических опытов, рассчитывать состав равновесных смесей, которые образуются, когда вещества вступают в обратимые реакции (см. Равновесие химическое). Измерения делаются с помощью специальных приборов-калориметров. Простейший калориметр представляет собой сосуд, в котором теплота изучаемого процесса Передается жидкости, температура которой точно измеряется. Зная теплоемкость жидкости и ее массу, химик после точного измерения роста (или снижения) ее температуры вычисляет, сколько теплоты выделено или поглощено.
Разработаны калориметры многих конструкций, способные работать как при температурах, близких к абсолютному нулю, так и при жаре в тысячи градусов. Есть миниатюрные калориметры, предназначенные для микроизмерений, и есть многотонные гиганты.
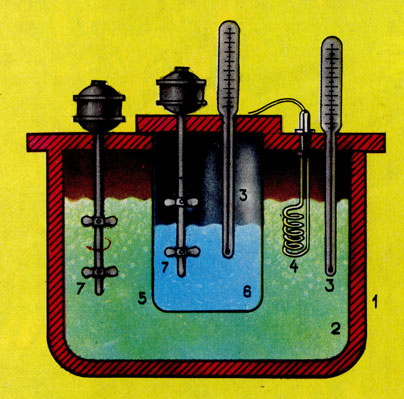
Схема простейшего калориметра: 1 - внешний сосуд, стенки которого обеспечивают теплоизоляцию рабочей жидкости (2), чтобы исключить неконтролируемый обмен теплом с окружающей средой; 3 - термометры; 4 - нагреватель, регулирующий температуру рабочей жидкости, для работы при пониженной температуре заменяется охлаждающим устройством; 5 - внутренний сосуд с металлическими стенками, обеспечивающими передачу тепла от реагирующей смеси веществ (6) к рабочей жидкости; 7 - мешалки
Например, уникальный ионизационный калориметр, предназначенный для измерения энергии космических лучей, установлен на горе Арагац в Армении.
Весит он 70 т.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'