
Ферменты
Ферментами называются белковые вещества (см. Белки), ускоряющие жизненно важные химические реакции в клетках организмов. Являясь катализаторами, они образуют с исходными веществами неустойчивые промежуточные соединения: эти соединения, распадаясь, дают конечный продукт данной реакции и освобождают ферменты.
Действие некоторых ферментов легко наблюдать в опыте. Так, фермент белковой природы - каталаза значительно ускоряет разложение пероксида водорода Н2O2 на воду и кислород. Это жизненно важная реакция, так как пероксид водорода образуется в результате обмена веществ в клетке и сам по себе оказывает на клетку вредное действие. Каталаза содержится почти во всех клетках животных и растительных организмов.
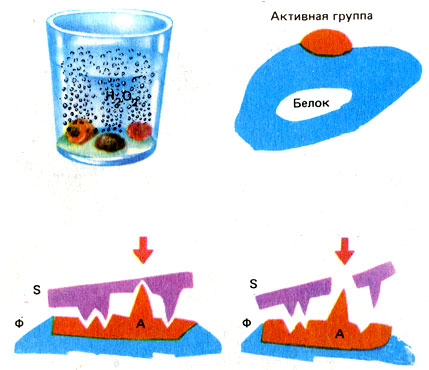
Кусочки моркови, мяса, картофеля разлагают пероксид водорода с выделением кислорода; это действует фермент каталаза (вверху слева). Общая схема строения фермента (справа). Внизу - схема действия фермента Ф. S - вещество, на которое действует фермент. Активная группа А облегчает разрыв химической связи в месте, указанном стрелкой
Известно очень много ферментов, и каждый из них ускоряет только одну какую-либо реакцию или группу однотипных реакций. Эту особенность ферментов называют специфичностью или селективностью (избирательностью) действия. Направленность их действия позволяет организму быстро и точно выполнять сложную химическую работу по перестройке молекул пищевых веществ в нужные ему соединения. Уже во рту во время пережевывания пищи под влиянием фермента амилазы сложные сахара, в частности крахмал, начинают разлагаться на менее сложные. Эта работа в дальнейшем будет продолжена в кишечнике ферментами карбогидразами. В желудке и кишечнике разложению с участием пепсина, трипсина, химотрипсина подвергаются белки пищи. Жиры разлагаются на глицерин и карбоновые кислоты (или их соли) под влиянием ферментов, называемых липазами. Все эти реакции разложения протекают по одному принципу: разрывается определенная химическая связь в молекуле белка, углевода или жира, и освободившиеся валентности используются для присоединения группы ОН- и иона Н+ из молекул воды. Происходит процесс гидролиза. Для молекулы белка эту реакцию можно представить так:
- R1 - CO - NH - R2 - + HOH = - R1COOH + NH2 - R2 -
Известны ферменты, оказывающие иное действие на молекулы. Некоторые из них ускоряют окислительно-восстановительные реакции: они способствуют переносу электрона от одной молекулы (окисляемой) к другой (восстанавливаемой). Существуют ферменты, соединяющие молекулы друг с другом; ферменты, переносящие большие и сложные группы атомов от одной молекулы к другой, и т.д.
Располагая богатым набором ферментов - катализаторов, клетка разлагает молекулы пищевых белков, жиров и углеводов на небольшие фрагменты и из них заново строит белковые и иные молекулы, которые будут точно соответствовать потребностям данного организма. Вот почему великий русский физиолог И. П. Павлов назвал ферменты носителями жизни.
Активность большего числа ферментов определяется строением белковой молекулы. Определенное пространственное расположение остатков аминокислот, образующих цепеобразную молекулу белка (полипептидная цепь, см. Пептиды), создает условия для протекания катализируемой ферментом реакции. Длинная цепочка остатков аминокислот свернута в сложный клубок, так, что аминокислоты, расположенные в цепи далеко друг от друга, могут оказаться соседями. Некоторые из возникших таким путем группировок остатков аминокислот проявляют каталитические свойства и образуют активный центр фермента.
Пепсин, химотрипсин, принимающие участие в пищеварении, могут служить примером ферментов, в которых активная группа является частью молекулы белка.

В лаборатории электронной микроскопии Мордовского государственного университета им. Н. П. Огарева
Другие ферменты для проявления активности нуждаются в веществах небелковой природы - так называемых кофакторах. Кофактором может быть ион металла (цинка, марганца, кальция и др.) или молекула органического соединения; в последнем случае ее часто называют коферментом. Иногда для действия фермента бывает необходимо присутствие как ионов металлов, так и коферментов. В отдельных случаях кофермент очень прочно соединен с белком; это наблюдается, например, у фермента каталазы, где кофермент представляет собой комплексное соединение железа (гем). В некоторых ферментах коферменты - это вещества, близкие по строению молекулы к витаминам. Витамины, таким образом, являются предшественниками коферментов. Так, из витамина В1 (тиамина) в клетках образуется тиаминпирофосфат - кофермент важного фермента (его называют декарбоксилаза), превращающего пировино-градную кислоту в оксид углерода (IV) и аце-тальдегид; из витамина В2 получаются коферменты флавиновых ферментов, осуществляющих в клетках перенос электронов - одну из стадий окисления пищевых веществ; из витамина В12 образуются коферменты, необходимые в процессе кроветворения, и т.д.
В последние годы в различных отраслях промышленности (хлебопечение, виноделие, кожевенное производство, фармацевтика) широко используются так называемые иммобилизованные (неподвижные) ферменты. Для ускорения нужной производственной реакции их закрепляют на поверхности инертного "носителя". В качестве его обычно используют силикагель - пористую белую массу, по составу оксид кремния (IV) или полимерные материалы. Через эту массу фильтруют исходные вещества. Фермент быстро и точно производит высокоспецифичную "химическую работу", в результате которой получаются продукты, почти не содержащие посторонних соединений.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'