
Электрон
Электрон-элементарная частица, носитель наименьшей массы и наименьшего электрического заряда в природе. Электрон обладает отрицательным зарядом, величина которого составляет, по современным данным, - 1,6021892 · 10-19 кулон или - 4,803242 · 10-10 ед. СГСЭ, а масса электрона равна 0,9109534 · 10-27 г.
Установление существования электрона было подготовлено трудами многих выдающихся исследователей. В 1897 г. электрон был открыт английским физиком Дж. Дж. Томсо-ном. Название "электрон" для этой элементарной частицы предложил в 1891 г. ирландский физик Дж. Стони.
Для химии электрон представляет большой интерес, так как эта частица - неотъемлемая составная часть атомов и молекул. Движение электрона, как и других элементарных частиц, подчиняется законам квантовой механики (см. Квантовая химия). В чем же заключается главная особенность квантовомеханического описания движения микрообъектов? Рассмотрим такой опыт. Электроны определенной энергии, вылетая из источника, проходят поодиночке через маленькие отверстия, находящиеся в поставленной на их пути преграде (например, пластинке), а затем попадают на фотопластинку, вызывая ее почернение. После проявления фотопластинки на ней можно увидеть совокупность чередующихся светлых и темных колец (рис. 1), т.е. дифракционную картину. Дифракционная картина представляет собой очень сложное физическое явление, включающее в себя как собственно дифракцию - огибание волной препятствия, так и интерференцию, т.е. наложение вторичных волн. И дифракция, и интерференция говорят о наличии у электрона волновых свойств, ибо только волны способны огибать препятствия и налагаться друг на друга в местах их встречи. Однако, попадая на фотослой, электрон дает почернение лишь в одном месте, в одном зерне фотослоя, что свидетельствует о наличии у него корпускулярных свойств. Ведь, будь он волной, он засвечивал бы, более или менее равномерно, всю пластинку.
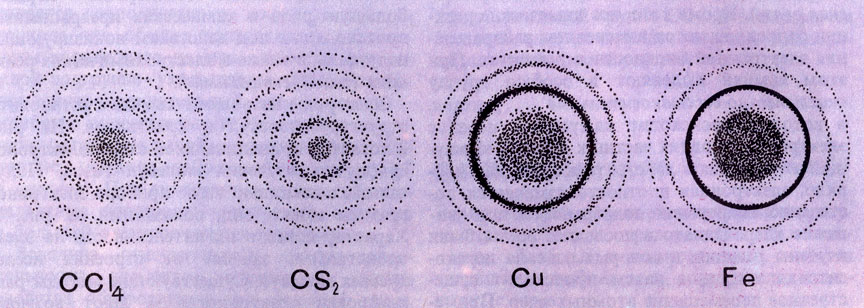
Рис. 1. Электронограммы газов (слева) и кристаллов (справа). Центральное пятно обусловлено нерассеянным пучком электронов, а кольца - электронами, рассеянными под разными углами
Таким образом, получается, что в одних условиях, скажем проходя через малое отверстие, электрон ведет себя как волна, тогда как в других, засвечивая фотопластинку, как частица (корпускула).
Вследствие дифракции электрон, пройдя отверстие, может в принципе попасть в любую точку фотопластинки, но с разной вероятностью. Иными словами, можно говорить о вероятности обнаружения электрона в той или иной области фотослоя или, более общо, в области пространства. Именно с помощью понятия вероятности описывают физики движение электрона.
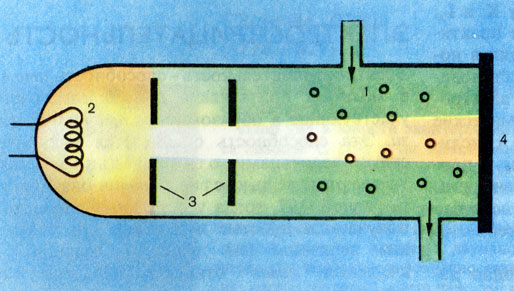
Рис. 2. Принципиальная схема электронографа для изучения строения молекул газов. 1 - пары исследуемого вещества; 2 - источник электронов (сильно нагретая металлическая нить); 3 - устройство для ускорения электронов ; 4 - фотопластинк а. Встречаясь с молекулами, электроны дифрагируют. Результат дифракции регистрируется на фотопластинке
Часто вероятность нахождения электрона в пространстве изображают наглядно с помощью множества точек, похожего на облако (рис. 3). Поэтому, говоря о вероятности обнаружения электрона в той или иной области пространства, употребляют выражения: "электронное облако", "распределение электронной плотности" или просто "электронная плотность". Следует помнить, что электронное облако - это не наглядный образ самого электрона, "размазанного" в пространстве, а лишь наглядное изображение распределения вероятности его нахождения в разных областях пространства, т. е. в конечном счете электронное облако характеризует движение электрона (см. Атом).

Рис. 3. Электронное облако атома водорода
Распределение электронной плотности в атомах и молекулах - их важнейшая характеристика, так как позволяет понять многие их физико-химические свойства (см. Химическая связь). Кроме того, все химические реакции сопровождаются изменением распределения электронной плотности в реагентах. При этом химики выделяют в особую группу окислительно-восстановительные реакции, в которых происходит кажущийся перенос электронов от одних частиц к другим. "Кажущийся"-так как в действительности, как правило, электронная плотность изменяется постепенно, непрерывно подстраиваясь под движения ядер. Однако в последнее время были изучены реакции, в которых сначала переносится электрон, а затем происходит существенное перемещение атомных ядер. Примером может служить следующая газофазная реакция:
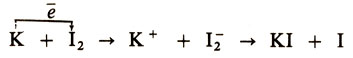
Благодаря скачку электрона реакция начинается на таком расстоянии между К и I2, когда обычные химические силы еще практически равны нулю. Химические реакции в ионосфере, многие окислительно-восстановительные реакции в растворах и на электродах, многие радиационно- и фотохимические процессы, некоторые каталитические окислительно-восстановительные процессы, процессы дыхания и фотосинтеза в живых организмах - вот далеко не полный перечень сложных процессов, включающих в себя стадию переноса электрона.
В последние годы возникло еще одно направление в "химии электрона" - изучение так называемого сольватированного электрона 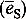 . Понятия о
. Понятия о 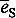 появилось впервые при изучении свойств растворов щелочных металлов в жидком аммиаке. Эти растворы имеют яркую окраску: синюю, голубую или бронзовую. С ростом концентрации металла уменьшается плотность раствора, повышается его электропроводность, а при больших концентрациях появляется характерный блеск и ряд других металлических свойств. Еще в начале XX в. было высказано предположение, впоследствии полностью подтвердившееся, что щелочной металл, растворяясь в аммиаке, диссоцирует на ион металла и сольватиро-ванный электрон: Me + xNH3 → ē(NH3)x + Me+. В 1960-х годах был открыт сольватированный электрон в воде. Если мы возьмем водный раствор, то электрон в нем долго не "живет". Он сравнительно быстро (время жизни электрона в воде составляет примерно миллисекунду) вступает в реакцию с молекулами воды:
появилось впервые при изучении свойств растворов щелочных металлов в жидком аммиаке. Эти растворы имеют яркую окраску: синюю, голубую или бронзовую. С ростом концентрации металла уменьшается плотность раствора, повышается его электропроводность, а при больших концентрациях появляется характерный блеск и ряд других металлических свойств. Еще в начале XX в. было высказано предположение, впоследствии полностью подтвердившееся, что щелочной металл, растворяясь в аммиаке, диссоцирует на ион металла и сольватиро-ванный электрон: Me + xNH3 → ē(NH3)x + Me+. В 1960-х годах был открыт сольватированный электрон в воде. Если мы возьмем водный раствор, то электрон в нем долго не "живет". Он сравнительно быстро (время жизни электрона в воде составляет примерно миллисекунду) вступает в реакцию с молекулами воды:
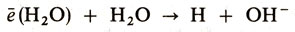
Сольватированные электроны играют большую роль в химических превращениях, происходящих под действием ионизирующих излучений, а также в электрохимических реакциях (см. Электрохимия).
Электроны позволяют химикам установить структуру молекул и кристаллов. На рис. 2 показана принципиальная схема электроно-графа для изучения молекул газов. Получаемые с помощью этого прибора электроно-граммы имеют вид, показанный на рис. 1. Характер колец и их интенсивность на элек-тронограмме зависят от строения исследуемых молекул. Существующие методы расшифровки электронограмм дают возможность установить по ним симметрию молекулы, величины валентных углов и межъядерных расстояний.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'