
Электронная связь, изотопы, ядерные реакции
Оставался еще не выясненным вопрос, как осуществляется связь, например, в двухатомных молекулах одинаковых элементов. Ответ на это независимо друг от друга дали Вальтер Коссель в 1915г., а спустя год Гилберт Н.Льюис и Ирвинг Ленгмюр. Исходя из представлений Бора и Мозли о распределении электронов вокруг ядра атома, Коссель, Льюис, Ленгмюр объясняли связь между атомами в таких молекулах тем, что электроны атомов участвуют в образовании одной или более электронных пар. Таким образом, в молекуле становится возможным образование стабильной электронной конфигурации инертного газа. Например, при образовании молекулы хлора Сl2 происходит связывание электронов УИ-орбитали с образованием одной общей электронной пары двух атомов
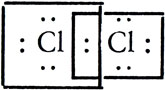
Объяснение физической природы химической связи на основе образования общих электронных пар ("атомная", гомеополярная ковалентная связь) имело особенное значение для органической химии при трактовке образования связей между двумя или несколькими атомами углерода или между атомами углерода и водорода. Впоследствии (после 1920 г.) Нэвил В. Сиджвик распространил представление о ковалентной связи и на неорганические соединения.

Ирвинг Ленгмюр (1881-1957)
После этого химические реакции стали интерпретироваться как результат смещения электронов, протоны при этом не играли никакой роли. В отличие от всех элементов только атом водорода, превращаясь в ион, может полностью освободиться от электронов (поскольку электрон у него единственный).
В 1913 г. английский радиохимик Фредерик Содди решил еще одну проблему. Исследование продуктов распада радиоактивных элементов приводило к противоречию с периодической системой. Например, свинец, образующийся при распаде урана, имел атомную массу, отличающуюся от массы обычного свинца. Ф. Содди предложил в 1913 г. название "изотоп" для любого элемента, который отличается от известного ранее элемента атомной массой, но занимает то же место в периодической системе*. Причина такого отклонения была обнаружена только в 1932 г. благодаря открытию нейтронов английским физиком Джеймсом Чэдвиком. Изотопами стали называть элементы, обладающие одинаковыми химическими свойствами и одним и тем же порядковым номером, но отличающиеся атомными массами. Порядковый номер определяется зарядом ядра атома (числом протонов), а атомная масса - числом протонов и нейтронов в атомном ядре. Благодаря использованию масс-спектрометрии после 1920 г. было обнаружено также, что многие элементы, образующиеся не в результате радиоактивного распада, являются смесью изотопов.
* (О жизни и деятельности Ф. Содди см. в книге [249].- Прим. ред.)
Как до 1900 г. считалось, что атом в соответствии с его определением является неделимым, так и до 1919 г. атомное ядро тоже считалось неделимым. Открытие ядерного распада при исследовании радиоактивности поставило перед учеными новую задачу: нельзя ли искусственным путем разделить протоны в ядрах. Сомнения, существовавшие по этому поводу, были обусловлены тем, что силы, связывающие протоны, были чрезвычайно велики. Но в 1919 г. Э. Резерфорду удалось осуществить первую ядерную реакцию. Резерфорд бомбардировал газообразный азот быстрыми а-частицами (ядрами гелия), в результате чего ему удалось превратить атомы азота в атомы кислорода.
После открытия ядерных реакций физику и химию стали рассматривать как две взаимно дополняющие друг друга науки, занимающиеся исследованием явлений природы. Позже к ним присоединилась биохимия. Проникая таким образом в сокровенные тайны природы, люди получили сегодня мощное средство влияния на саму природу. Это средство в руках человека обладает не только созидательной, но и огромной разрушительной силой! И хотя уже 500 лет назад человечество осознало, что Земля не является центром Вселенной, следует помнить, что наша планета - пока единственное наше жизненное пространство и ее страдания - это наше горе, а ее радости - это наше счастье.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'