
Введение
Биологическая химия является наукой, которая изучает химический состав органов и тканей животных и растений и химические процессы, лежащие в основе их жизнедеятельности. Биохимия изучает жизнь во всех ее проявлениях - от прорастания зерна до высшей нервной деятельности.
Биохимия сравнительно недавно, около 100 лет назад, оформилась в самостоятельную науку. Она возникла в пограничной области биологии и химии. Однако за этот короткий срок и особенно в последние 20-30 лет биохимия стремительно развивалась. Именно этим объясняется тот факт, что научные исследования в области биологии, физиологии, микробиологии, клинических дисциплин и даже в некоторых областях промышленности в значительной степени развиваются благодаря использованию биохимических методов.
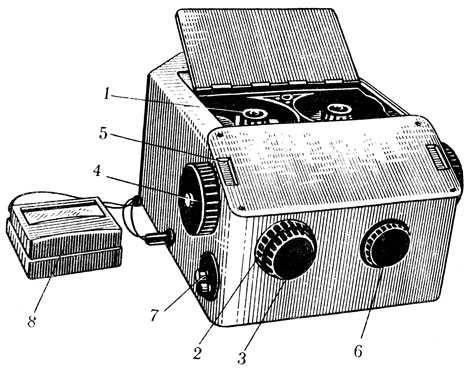
Рис. 1. Фотоэлектроколориметр (ФЭК-М). 1 - держатели кювет; 2, 3 - узел нейтральных клиньев; 4 - щелевая диафрагма; 5 - шкала; 6 - переключатель светофильтров; 7 - переключатель чувствительности; 8 - гальванометр
Задачи, стоящие перед биохимией, можно разрешить лишь путем объединения результатов биохимии с данными биофизики, морфологии, генетики и Многих других биологических дисциплин. В последние годы развитие биохимии, в большей степени определяется достижениями физики, математики, кибернетики, механики и т. д., ибо изучение состава и структуры вещества биологического профиля невозможно без использования сложных и точных приборов и различных аппаратов. Сейчас в клинических лабораториях широко используются различные электрофотоколориметры (рис. 1), спектрофотометры (рис. 2), флюориметры и другие приборы, а биохимические лаборатории трудно представить себе без аппаратов электрофореза, аминокислотного анализатора, автоматического коллектора отбора фракций (рис. 3), колоночной хроматографии и пр. В качестве примера можно указать на изучение структуры и состава белка. Решение этого вопроса стало возможным только после того, как были разработаны такие методы исследования, как гидролиз, хроматография, электрофорез, использование меченых атомов, рентгеноструктурный анализ. Но применение этих методов потребовало создания аппаратов для хроматографии, выпрямителей для электрофореза, приборов для спектрального анализа, аминокислотных анализаторов, ультрацентрифуг, электронно-вычислительных машин. Необходимым условием для выполнения таких анализов является получение особо очищенных реактивов, синтетических смол с определенными специфическими свойствами, радиоактивных изотопов, особых видов хроматографической бумаги.
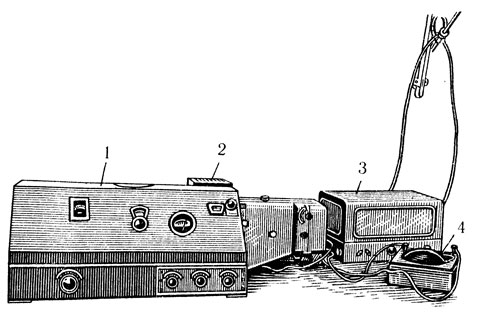
Рис. 2. Спектрофотометр (СФ-4). 1 - корпус спектрофотометра; 2 - осветитель с источником ультрафиолетового излучения (водородная лампа) или видимого света (лампа накаливания); 3 - стабилизатор; 4 - гальванометр напряжения
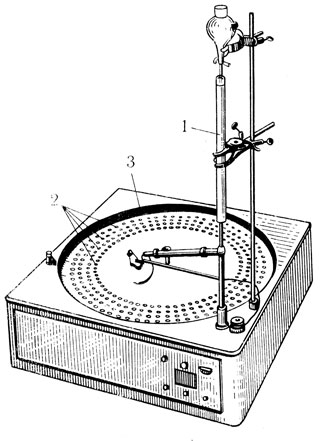
Рис. 3. Автоматический коллектор для сбора фракций. 1 - колонка, на которой происходит разделение. Вытекающие фракции растворов собираются в пробирки (2), установленные в барабане (3), автоматически передвигающемся. Передвижение барабана происходит через определенные промежутки времени (установка 'на время') или же когда в пробирки выливается определенный объем (установка 'на объем')
В свою очередь развитие целого ряда биологических дисциплин основано на достижениях биохимии. Так, физиология и гигиена труда, процессы нервной и мышечной проводимости, проблема памяти, вопросы рационального питания решаются с учетом знаний биохимии этих процессов, так же как и проблемы сельского хозяйства: повышение производительности сельскохозяйственных культур и животноводства. Современная пищевая промышленность в своей основе также базируется на биохимии, которая, детально изучив процессы хлебопечения, виноделия, переработку молока, жиров, консервирования и т. д., помогает увеличить выпуск и улучшить вкусовые качества пищевых продуктов. Есть еще одна область знаний, в которой трудно переоценить значение биохимии,- это медицина. Еще М. В. Ломоносов писал: "Медик без довольных познаний химии совершенен быть не может".
В человеческом организме постоянно протекают тысячи и тысячи различных химических реакций, которые обеспечивают его существование. И задача биохимии состоит в том, чтобы, изучив состав организма и продуктов его обмена веществ, выяснив функции различных органов и тканей, познать " существо процессов жизнедеятельности организма. В основе этих исследований лежит знание взаимодействия разнообразных физических и химических процессов, взаимозависимости между структурой и функцией веществ, регуляторных механизмов, контролирующих деятельность обмена веществ.
Таким образом, биохимия является теоретической основой медицины. Знание биохимических процессов, протекающих в нормальном здоровом организме, позволяет понять и природу различных заболеваний, которые в своей основе представляют разнообразные отклонения протекающих в организме химических реакций - патогенез заболеваний. Не менее существенным является использование данных биохимии в вопросах диагностики и лечения.
Трудно представить врача, который бы ставил диагноз без результатов тщательного биохимического анализа крови, мочи, кала, желудочного содержимого, спинномозговой жидкости и т. д. Определение широкого круга веществ в этих жидкостях позволяет врачу с большей степенью точности, своевременно и правильно поставить диагноз. Изменения концентрации многих веществ при заболеваниях являются специфическими. Например, стойкое по сравнению с нормой увеличение сахара в крови и моче является специфическим для сахарного диабета; снижение в крови γ-глобулинов характеризует понижение сопротивляемости организма к вредным воздействиям; значительное повышение цистина в моче является симптомом цистинурии, наличие в моче больших количеств мочевой кислоты является следствием подагры.
В последние годы в клинике стали широко применять определение активности ферментов как диагностических тестов. Сущность применения этих анализов заключается в том, что в определенных органах и тканях протекают специфичные для данной ткани химические процессы, которые катализируются соответственно определенными ферментами. При заболеваниях этих органов и тканей происходит нарушение структуры клеток и ферменты вымываются в кровь, что проявляется изменением их активности в крови по сравнению с нормой. Так, при инфаркте миокарда в крови увеличена активность одной из аминотрансфераз и лактатдегидрогеназы, при заболеваниях поджелудочной железы повышена активность амилазы, а при рахите - фосфатазы. Особенностью ферментной диагностики является их органная и тканевая специфичность и возможность ранней постановки диагноза, в ряде случаев в первые часы развития заболевания или еще в доклинический период, как, например, при рахите. Сейчас в клиниках начинают внедрять методы определения изоферментов, представляющих собой ферменты, катализирующие одну и ту же реакцию, но различающиеся по своим электрофоретическим и иммунологическим свойствам. Изоферменты характеризуются органной специфичностью. Так, различают 5 изоферментных форм лактатдегидрогеназы, одна из которых, наиболее электрофоретически подвижная, специфична для миокарда, другая, менее подвижная, в основном обнаруживается в печени.
Таким образом, результаты биохимических анализов с учетом данных клинического обследования больного и применением других необходимых исследований дают в руки врача те сведения, которые помогают ему своевременно и правильно поставить диагноз.
Основными средствами лечения заболеваний являются разнообразные химические вещества, влияющие определенным образом на нарушенные биохимические процессы обмена веществ и энергии в организме. Действие лекарственных препаратов включает блокировку или подавление активности различных вредных агентов (микробов или вирусов), снабжение организма недостающими веществами (витаминами, минеральными солями, гормонами и др.), активирование деятельности биохимических процессов вследствие гипофункции органов и тканей и пр. Например, использование сульфаниламидных препаратов при кокковых инфекциях, широкое применение антибиотиков, различных вакцин и сывороток при заболеваниях вирусного или микробного происхождения, введение витаминов для лечения а- и гиповитаминозов, инсулина при сахарном диабете, соляной кислоты и пепсина при пониженной кислотности в желудке и т. п.
Разработка новых высокоэффективных лекарственных веществ основана на знаниях химических процессов в органах и тканях и их соответствующих изменений при определенных заболеваниях. Все вышесказанное достаточно полно характеризует значение биохимии для медицинской науки.
История развития биохимии. История биохимии - это история происхождения жизни на земле. Поэтому именно биохимия явилась ареной ожесточенной борьбы двух противоположных мировоззрений - материализма и идеализма в науке. Именно биохимия неопровержимыми доказательствами очищала биологическую науку от идеалистической шелухи.
И первым, кто заложил основы материалистического взгляда на процессы жизнедеятельности, был великий русский ученый М. В. Ломоносов, открывший закон сохранения материи и энергии. В работах А. Лавуазье этот закон получил свое практическое подтверждение. В последующие годы трудами многих ученых всего мира были сделаны крупнейшие научные открытия, которые способствовали развитию биохимии на основе материализма.

Дж. Нортроп
Получением синтетической мочевины из неорганических веществ в 1828 г. Ф. Вёлер доказал возможность синтеза органических соединений без vis vitalis - "жизненной", или "божественной", силы. Его результаты послужили теоретической основой для последующего искусственного получения различных органических соединений. Так, Н. И. Зининым был получен анилин, М. Бертло - жиры, А. М. Бутлеровым - углеводы, А. Я. Данилевским и Э. Фишером - пептидоподобные вещества и пептиды и, наконец, проф. В. Ингремом - первый белок - гормон инсулин.

Н. И. Лунин (1854-1937)
В последующие годы в связи с развитием химических, физических,, математических дисциплин биохимия стала стремительно развиваться. Дж. Самнер и Дж. Нортроп впервые выделили ферменты - уреазу и пепсин. Э. Фишер открыл нуклеиновые кислоты. Н. И. Лунин и К. Функ - витамины, О. Варбург и А. Сент-Дьердьи вскрыли основу процессов получения энергии в организме, Л. Поллинг и В. Кори установили структуру простых белков, а Дж. Уотсон и Ф. Крик - структуру ДНК, С. Очао, А. Корнберг и Э. Чаргафф много сделали для открытия генетического кода и и т. д. - вот далеко не полный перечень величайших открытий в биохимии.

А. Н. Бах (1857-1946)
Среди творцов науки отечественные ученые всегда стояли в первых рядах. А. Я. Данилевский был основоположником биохимии в России. Его стараниями в 1862 г. была впервые в мире создана кафедра медицинской химии в Казанском университете (до последних лет медицинская биохимия называлась физиологической химией). Первый учебник по физиологической химии был издан в 1847 г. А. И. Ходневым.

В. И. Палладин (1859-1922)
Работы М. М. Манассеиной, К. С. Кирхгофа, А. И. Лебедева легли в основу учения о ферментах. Трудам И. П. Павлова по ферментативным и гуморальным механизмам пищеварения, А. Н. Баха и В. И. Палладина о биологическом окислении, В. А. Энгельгарда о значении АТФ в мышечном сокращении, А. И. Опарина по созданию стройной системы происхождения жизни, С. Е. Северина по изучению обмена углеводов, А. Е. Браунштейна об аминокислотном обмене заслуженно отдается приоритет в этих вопросах биохимиками всего мира.

В. А. Энгельгард
Настоящее развитие биохимии в России началось после Великой Октябрьской социалистической революции. Партия и правительство уделяют большое внимание биохимии. Большая армия научных сотрудников работает в биохимических институтах и лабораториях, которые возглавляются крупными учеными нашей страны, такими, как С. Е. Северин, А. И. Опарин, В. А. Энгельгард, А. Е. Браунштейн, А. В. Палладии, С. Р. Мардашов, В. Н. Орехович, А. Н. Спирин, И. И. Иванов, А. А. Покровский и др.

А. И. Опарин
Общие представления об обмене веществ. В основе всех биохимических проявлений жизни лежат два основополагающих уравнения, которые четко показывают взаимосвязь организма с окружающей средой.
Первое из них - это процесс фотосинтеза:
6СО2 + 6Н2О + энергия солнца → C6H12O6 + 6О2.
При этом процессе образуются питательные, органические вещества и кислород. Детальное изучение фотосинтеза было проведено К. А. Тимирязевым. Фотосинтез протекает в зернах хлорофилла, которые, по образному выражению Бернала, являются улавливающей системой фотосинтеза, вызывая у растений рост, у животных - движение, у человека - мысль.
Второе уравнение характеризует закон сохранения и превращения энергии в живых тканях:
С6H12О6 + 6О2 → 6СО2 + 6Н2О + энергия.
Расшифровка этого уравнения включает изучение превращений ряда веществ и энергии в организме. Эти два уравнения определяют круговорот углерода и энергии в природе. Наряду с этим между организмом и внешней средой происходит постоянный обмен азота, который поступает с продуктами питания и выделяется из организма в виде конечных продуктов, таких, как мочевина, мочевая кислота и т. д.
В изучении вопроса круговорота веществ большая заслуга принадлежит С. Н. Виноградскому. Им впервые научно доказан круговорот в природе азота, углерода, серы и многих других химических элементов.
Окружающая среда является для организма основным поставщиком питательных веществ, которые в организме подвергаются процессам распада - диссимиляции - с образованием необходимых веществ для построения клеток и тканей за счет энергии, которая при этом выделяется.
Изучение обмена веществ и энергии происходит на разных уровнях - целого организма, органа или ткани, клетки и молекулы. Изучение обмена веществ на молекулярном уровне является наиболее важным, так как позволяет вскрыть самые интимные механизмы различных видов обменов.
Основные методы, применяемые при биохимических исследованиях. Соответственно задачам исследований используются различные методы. Изучение обмена веществ на уровне целого организма является наиболее общим. Для этого применяются методы определения количества питательных веществ, полуденных организмом за определенный промежуток времени, и количества выделившихся. Таким путем, например, определяют баланс азота. Баланс энергии устанавливают методами калориметрии, когда учитываются энергетические ценности питательных веществ и энергетические траты организма. Для этих целей используют и "дыхательный коэффициент", который представляет собой отношение объема выделенного за определенный промежуток времени углекислого газа к объему поглощенного за то же время кислорода СО2/О2).
Установлено, что дыхательный коэффициент при окислении углеводов равен 1, жиров - 0,7 и белков - 0,8.
Обмен веществ органа изучают с использованием, например, метода ангиостомии, предложенного Е. С. Лондоном. Сущность этого метода заключается в том, что артерии и вены исследуемого органа выводят наружу и в оттекающей от этого органа крови определяют различные вещества, введенные в кровоток, что позволяет судить об усвоении и выделении этих веществ в органе.
Метод переживающих тканей предусматривает выделение ткани из организма и содержание ее в определенной среде, в которой ткань может нормально существовать и функционировать.
Методом тканевых срезов также изучают обмен веществ в органе или ткани. С этой целью получают тонкий срез органа, помещают его в физиологический раствор с испытуемым веществом и изучают получающиеся при этом продукты.
Методами экстрактов и гомогенатов исследуют обмен на уровне клетки. Для этого приготавливают экстракты (вытяжки) из определенных клеток или гомогенат (измельченная кашица). Затем наблюдают, какие вещества получаются из данного соединения после прибавления его к экстракту или гомогенату.
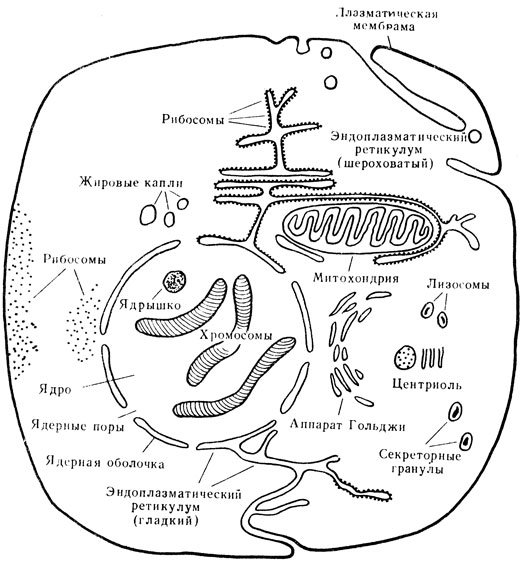
Рис. 4. Структура животной клетки по данным электрон пой микроскопии
Обмен веществ изучают и в субклеточных фракциях. При детальном рассмотрении структуры клетки, например под электронным микроскопом, дающим увеличение в сотни тысяч и даже миллионы раз, были открыты различные внутриклеточные органеллы - ядра, ядрышки, микросомы, лизосомы, митохондрии, эндоплазматический ретикулум и др., представленные на рис. 4. В каждой из этих структур протекают специфические химические процессы. Разработаны методы выделения этих структур путем дифференциального центрифугирования в центрифугах с большим числом оборотов, доходящим до 10 000 - 60 000 оборотов в минуту. В связи с различными величинами этих частиц они осаждаются при разных ускорениях. Определяя различные вещества и ферменты в субклеточных фракциях, изучают тонкие механизмы обмена веществ в организме.
В последние годы нашли широкое применение и такие методы исследований, как метод изотопов. Принцип его заключается в том, что синтезируется вещество, в молекулы которого вводят атомы радиоактивных или тяжелых изотопов. При этом учитывается, что живой организм одинаково использует как природные вещества, так и их изотопы в процессах обмена. Поэтому по поведению изотопа в организме судят о судьбе вещества, в составе которого этот изотоп находится.
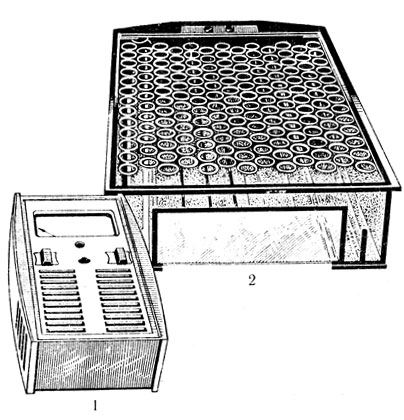
Рис. 5. Аппарат для электрофореза белков на бумаге (ЭФ-2). 1 - источник питания; 2 - электрофоретическая ванна
Одним из методов, позволяющим проводить детальный анализ веществ, является электрофорез. Он основан на том, что в электрическом поле молекулы вещества, обладающие электрическим зарядом, будут передвигаться к катоду или аноду. Их скорость и направление зависят от величины заряда молекулы, ее формы, размера и т. д. Этот анализ проводится в аппарате для электрофореза (рис. 5), который в принципе состоит из стабилизатора, дающего постоянный ток, и камеры. В последней имеются две ванночки для буферного раствора, к которым подведены электроды. Между ванночками располагают полоски бумаги с исследуемым веществом. При включении тока на полосках бумаги, пропитанных буферным раствором, создается электрическое поле, в котором и будут передвигаться молекулы анализируемого вещества. Этот метод успешно применяется для разделения белков на отдельные фракции (альбумины, различные типы глобулинов и т. д.), для выделения изоферментов и т. д. В клиниках метод электрофореза используется в диагностических целях, так как при различных заболеваниях изменяется количество и состав белковых фракций сыворотки крови и тканей.
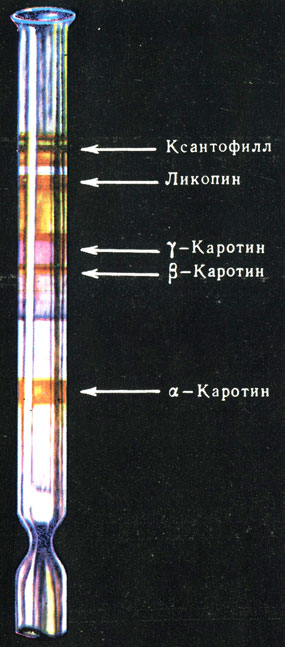
Рис. 6. Разделение каротиноидов красного перца на колонке
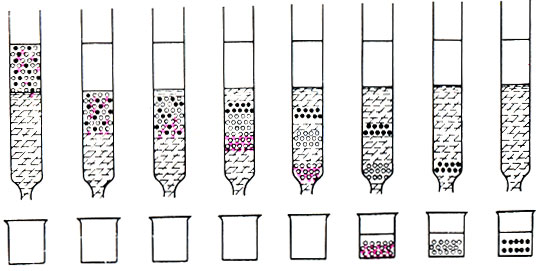
Рис. 7. Схема разделения смеси трех веществ на адсорбционной колонке
Хроматографические методы введены в науку и практику М. С. Цветом. Сущность метода заключается в том, что различные вещества обладают различной способностью адсорбироваться на определенных веществах - адсорбентах. Поэтому, пропуская смесь веществ через стеклянную трубку, наполненную каким-либо адсорбентом (М. С. Цвет использовал для этой цели окись алюминия), вещества распределяются на разных уровнях. На рис. 6 показано разделение каротиноидов из красного перца. Как видно из рисунка, быстрее всех передвигается а-каротин и медленнее других - ксантофилл. Чтобы собрать отдельно каждое вещество, колонку промывают растворителем. Быстрее других будет вымываться то вещество, которое было слабо связано с адсорбентом. На рис. 7 такое вещество расположено в самом конце колонки и обозначено светлыми кружочками. Вещество, прочнее соединенное с адсорбентом (обозначено на рисунке крестиками), будет вымываться последним. Разновидностью колоночной хроматографии является хроматография на бумаге. При этом смесь веществ, подлежащих разделению, наносят на полосу хроматографической бумаги, конец которой помещают в раствор с органическими растворителями (например, со смесью бутилового спирта и уксусной кислоты, фенола, пиридина и др.). В силу различной растворимости вещества смеси распределяются на разных участках полосы бумаги. Окрашивая эти вещества, можно определить состав смеси и их количества. На рис. 8 представлена хроматограмма смеси аминокислот.
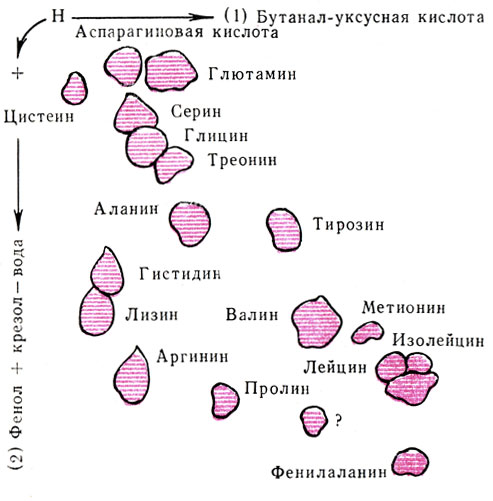
Рис. 8. Двухмерная хроматограмма смеси аминокислот
Изучение обмена веществ и энергии на всех уровнях с применением самых различных методов исследований как в норме, так и при патологии, является существенным фактором для дальнейшего развития медицины в борьбе за здоровье человека.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'