
Физико-химический анализ
Новая область химии, названная впоследствии академиком Н. С. Курнаковым физико-химическим анализом, развивалась В. В. Куриловым и его учениками и отражена в их трудах. Отдавая должное его научным заслугам, можно сказать, что среди химиков-неоргаников варшавского периода имя Венедикта Викторовича Курилова занимает одно из видных мест.
В. В. Курилов известен физико-химическими исследованиями аммиакатов, являющихся частным случаем обширного класса комплексных соединений, именуемых продуктами присоединения, и разработкой методов физике-химического анализа в приложении к двойным системам с органическими и неорганическими компонентами. Он разработал принципы общей классификации искусственно получаемых и природных веществ.
В. В. Курилов
В. В. Курилов родился 1 марта 1867 г. в деревне Тимошенской Велико-Устинского уезда Вологодской губернии в семье государственного крестьянина. По окончании гимназии в Архангельске он поступил сначала в Петербургский университет, а затем перевелся в Казанский, который окончил в 1889 г. по математическому отделению физико-математического факультета. Научную деятельность В. В. Курилов начал студентом под руководством профессора Ф. М. Флавицкого. В 1886 г. им была выполнена первая работа - "Исследование терпенов масла из смолы ели", опубликованная в 1888 г.1. Это исследование требовало большого труда, исключительной кропотливости и умения проводить сложный эксперимент.
1 (В. В. Курилов. ЖРФХО, 21, 357 (1888).)
Первоначальное изучение небольших количеств масла из смолы ели показало, что оно содержит две фракции: высшую, представляющую изотерпен со значительной примесью терпена, и низшую, содержащую терпен с примесью изотерпена.
Использовав большие количества масла, В. В. Курилов после проведения нескольких десятков фракционированных перегонок сумел отделить терпен от изотерпена. Автор тщательно проанализировал обе полученные фракции, определил их плотность, коэффициент расширения, изучил оптическую деятельность и нашел коэффициент преломления. Это позволило ему установить, что высшая фракция представляет собой левовращающий изотерпен с удельным вращением 47,5°, имеющий две двойные связи; низшая фракция была оптически недеятельным терпеном. Целеустремленный труд привел молодого исследователя к успешному разрешению вопроса о составе масла из смолы ели.
В студенческий период жизни В. В. Курилов провел и другие интересные исследования по получению перекисей цинка, кадмия и магния. Им было установлено, что способность названных металлов образовывать перекиси находится в зависимости от величины их атомных весов и возрастает с увеличением последних. Работа эта была опубликована под названием "Действие перекиси водорода на гидраты окисей кадмия, цинка и магния"1. Ученый совет Казанского университета за эту работу удостоил В. В. Курилова золотой медали, а Московское общество любителей естествознания отметило ее почетным отзывом.
1 (В. В. Курилов. ЖРФХО, 22, 171 (1890).)
Студентом В. В. Курилов выполнил исследование на физико-математическую тему "Методы определения трех элементов земного магнетизма". Эта работа тоже была отмечена на торжественном собрании университета и награждена серебряной медалью1.
1 (Дипломы о награждении В. В. Курилова золотой и серебряной медалями хранятся в Ростовском областном архиве. Ф. 313, св. 34, оп. 4.)
В 1890 г. молодого исследователя, успешно закончившего университет, оставляют в нем на два года для подготовки к профессорскому званию по кафедре химии. В январе 1891 г. он командируется в С.-Петербургский университет для занятий в химических лабораториях. В С.-Петербурге одновременно с занятиями в лаборатории он работает преподавателем физики и математики в одной из частных гимназий, а затем и в реальном училище.
С 1893 по 1894 г. В. В. Курилов был лаборантом Петербургского университета. Здесь, пользуясь новейшими методами физической химии, основываясь на законе действия масс и правиле фаз В. Гиббса, посредством измерения упругости диссоциации твердых веществ и растворов он начал свои исследования аммиакатов.
Изучение явлений диссоциации впервые было произведено в 1867 г. Лебре, показавшим, что диссоциации твердых тел можно сравнить с явлениями испарения жидкостей. Много ценного для исследования упругости диссоциации твердых тел сделал Изамбер, установивший закон постоянства выделяющегося газа при разложении твердого тела при данной температуре. Если же разлагается система веществ, образующих несколько химических соединений, то,как показал Изамбер, переход от одного соединения к другому ведет за собой резкое "изменение упругости выделяющегося газа. Этот метод был положен в основу установления индивидуальности химических соединений. Нужно было решить вопрос, будут ли соблюдаться закономерности в случаях, когда разложению подвергаются не твердые, а жидкие тела, образующие при этом твердые или жидкие продукты и газообразные вещества.
Упругости диссоциации жидких веществ, кроме Изамбера, изучали и такие выдающиеся химики, как Розебом и Михаэлис. Характерно, что все они получили противоречивые результаты по затронутому вопросу. Тем более велика была заслуга В. В. Курилова, успешно разрешившего эту задачу.
Свой эксперимент В. В. Курилов обобщил в работе "Упругость диссоциации как признак индивидуальности химических соединений"1.
1 (В. В. Курилов. ЖРФХО, 25, 170 (1893).)
Опыты по исследованию упругости диссоциации в гетерогенных системах В. В. Курилов начинает с изучения поглощений аммиака раствором нитрата аммония, так как именно по этому вопросу в литературе имелись самые противоречивые данные. Так, Дайверс, исследуя соединение нитрата аммония с аммиаком, пришел к выводу, что оно представляет собой жидкий раствор соли в аммиаке. Рауль, а вслед за ним и Трост, основываясь на своих опытных данных, утверждали, что жидкость Дайверса - химическое соединение состава 2NH4NO3×3NH3.
ИнОе показали исследования В. В. Курилова. В специально сконструированном для этой цели приборе он установил, что при постепенном отнятии аммиака из жидкости Дайверса величина упругости паров жидкости падает до тех пор, пока остаются непотлопленными 1,33 моля аммиака. Эта величина будет в свою очередь постоянной до тех пор, пока в жидкости Дайверса останется 0,4 моля аммиака. При этом в указанном концентрационном интервале система теряет гомогенность и состоит из твердой и жидкой фаз. Начиная с концентрации 0,4 моля видимые следы жидкой фазы исчезают. На основании опытных данных В. В. Курилов приходит к выводу, что жидкость Дайверса представляет собой раствор нитрата аммония в аммиаке, а упругость аммиака, приводимая Тростом для соединения 2NH4NО3×3NH3, соответствует гетерогенной системе из жидкого и твердого тела, в которой количество поглощенного аммиака отвечает насыщенному раствору соли при 0°.
Подобные же исследования были проведены В. В. Куриловым и для случаев поглощения аммиака бромистым аммонием. При этом наблюдалась полная аналогия с ходом разложения жидкости Дайверса с той лишь разницей, что в системе аммиак-бромистый аммоний падение упругости имело место в пределах от 1,02 до 0,94 моля концентраций аммиака. При дальнейшем разложении системы, после исчезновения всей жидкости, упругость паров все время оставалась постоянной.
Опыты В. В. Курилова показали, что область постоянных упругостей соответствует соединениям NH4Br×3NH3 и NH4Br×NH3.
"Таким образом, случай поглощения аммиака бромистым аммонием,- говорит В. В. Курилов,- представляет пример, как легко совершается переход от подобных жидких систем к телам твердым с резко выраженным характером определенных соединений. Изучением явлений диссоциации именно таких систем удастся, может быть, связать концы и поныне еще разорванной цепи, в которой химизм проявляется, с одной стороны, в резкой форме определенных соединений и с другой - в форме растворов с неопределенным составом и признаками механической смеси"1.
1 (В. В. Курилов. ЖРФХО, 25, 191-193 (1893).)
В. В. Курилов приходит к выводу, что отсутствие постоянства упругости пара не дает права не признавать характера определенного химического соединения за непрочным жидким телом, так как известен ряд жидких систем, которые в одно и то же время обладают свойствами растворов и определенных соединений.
Изучая упругости диссоциации соединений хлористого цинка с аммиаком, т. е. твердых аммиакатов, В. В. Курилов установил, что, кроме аммиакатов, указываемых Изамбером, т. е. ZnCl2×6NH3, ZnCb×4NH3 и ZnCl2×2NH3, существует еще соединение ZnCl2×NH3.
Ученый впервые нашел для хлористого кадмия аммиакаты следующего состава: CdCl2×6NH3, CdCl2×4NH3, CdCl2×3NH3 и CdCl2×NH3.
Рассмотренные работы приводят автора к выводам, что для диссоциации систем из твердых компонентов достаточно установить точно два значения величин упругости, характеризующих резкий скачок при переходе от одного состава к другому, чтобы признать существование новой формы соединения. В жидких системах точное исследование изменения кривизны кривых представляет пока единственный путь для установления химизма между их компонентами. Материал по продуктам присоединения аммиака к растворам солей составил содержание магистерской диссертации "Разложение (диссоциация) химических соединений, образованных поглощением аммиака солями", которая была успешно защищена в Казанском университете в 1895 г.
В 1896-1898 гг. В. В. Курилов получает командировку за границу. Здесь он занимается в лабораториях Розебома (Амстердам), Нернста (Геттинген), Кюетера (Бреславль), Вант-Гоффа (Берлин). За границей В. В. Курилов продолжал работать и над идеей, уже высказанной им в магистерской диссертации,- изыскание новых путей в установлении химической индивидуальности и применение закона действия масс и правила фаз к изучению сложных химических образований. Экспериментально он устанавливает условия равновесия в системах из двух и трех компонентов. Результаты опытов обобщены в монографию1, в которой рассматривается применение физико-химических методов исследования для изучения комплексных соединений типа продуктов присоединения, частным случаем которых являются аммиакаты. Большое внимание уделяется здесь изучению равновесия β-нафтолпикрата в разнородных, не смешивающихся между собой жидкостях - в воде и бензоле. В. В. Курилов определил равновесие твердого β-нафтолпикрата в соприкосновении с водой и бензолом, а также нашел коэффициенты распределения реагирующих веществ.
1 (В. В. Курилов. Опытное изучение химических равновесий в системах из двух и трех веществ. Екатеринослав, 1899.)
В дальнейшем В. В. Курилов исследовал системы: ZnSO4-NH3-Н2O и FeCl3-K4Fe(CN)6-H2O.
Дополнительно к этим системам были выполнены под руководством В. В. Курилова его учениками Д. Е. Дионисьевым MgCl2-NH3-Н2О и Н. Н. Стасевичем Cu(NO3)-NH3-Н2O.
В 1899 г. В. В. Курилова назначают ординарным профессором по общей химии в Екатеринославском горном училище. Именно здесь он приступил к систематическому изучению сложных химических соединений-продуктов присоединения. В. В. Курилов задается целью дать общую классификацию всех природных и искусственно получаемых веществ. Частично эта задача была уже им выполнена и обобщена в труде "К учению об аммиакатах в связи с общей классификационной проблемой"1.
1 (В. В. Курилов. К учению об аммиакатах в связи с общей классификационной проблемой. Екатеринослав, 1905.)
Эта работа являлась обобщением огромного накопленного фактического материала по продуктам присоединения - аммиакатам. Она имеет несомненное теоретическое значение, так как в ней ученый делает попытку дать химическую классификацию всех веществ и устанавливает место аммиакатов в общей системе химии. Характеризуя аммиакаты как продукты присоединения, В. В. Курилов определяет их как "вещества, образованные комбинациями целых частиц аммиака с частицами солей, окисей и простых тел". Для распознавания природы аммиакатов он рекомендует изучать упругости их диссоциации в твердом состоянии, пользуясь для этого методами физико-химического анализа, как наиболее точными методами исследования.
Главное внимание в этом труде В. В. Курилов уделяет разработке классификации аммиакатов. Все аммиакаты автор подразделяет на два класса. К первому классу относит аммиакаты, к которым приложимы закон постоянства состава и закон простых стехиометрических отношений. По своей природе эти аммиакаты близко стоят к обычным химическим соединениям. От них путем непрерывного перехода можно, по трактовке автора, перейти к аммиакатам, которые не обладают постоянным составом, т. е. к аммиакатам второго класса. В подтверждение этого положения В. В. Курилов получил для азотнокислого серебра, кроме аммиаката с постоянным составом AgNО3×2NH3, аммиакаты, где на одну частицу азотнокислого серебра приходится переменное количество молекул аммиака. Автор установил, что для элементов, близких по своим свойствам, наблюдается одна и та же форма аммиаката, и этот факт может служить критерием для отнесения аммиакатов к тому или иному классу.
При разработке общей классификации Курилов находит и место аммиакатам в непрерывном ряду природных и искусственно получаемых веществ. По мнению ученого, аммиакаты занимают промежуточное положение между обычными химическими соединениями, к которым применимы основные законы химии: закон постоянства состава, простых кратных отношений и другие, и продуктами адсорбции, к которым неприложим закон постоянства состава.
По классификации В. В. Курилова, аммиакаты первого класса близко стоят к химическим соединениям, тогда как второго класса - к продуктам адсорбции аммиака. Между этими классами аммиакатов нет резкой границы, а имеют место взаимные переходы. В частности, В. В. Куриловым было показано, что аммиакат хлористого цинка, относящийся к представителям первого класса, при действии на него воды образует коллоидный раствор, который, свертываясь, превращается в гидрогель.
К веществам промежуточного ряда, кроме аммиактоз, В. В. Курилов относит также гидраты, двойные соли, силикаты, от которых легко можно осуществить переход к такому сложному конгломерату, каким является почва.
"Можно представить общую классификацию всех веществ как природных, так и искусственно получаемых в простой форме одной непрерывной цепи",- пишет автор.
Начальное звено такой цепи, по В. В. Курилову, составляют простые тела, за ними следует класс химических соединений, затем идут продукты присоединения, наконец, адсорбционные и коллоидные вещества, не подчиняющиеся основным законам химии и выходящие из рамок современной систематики; начальный член химической цепи генетически связан с первичной материей, а конечный - с живой плазмой.1
1 (В. В. Курилов. К учению об аммиакатах в связи с общей классификационной проблемой. Екатеринослав, 1905.)
Исследования в области аммиакатов составили содержание его докторской диссертации, которую он защитил в заседании Ученого совета Московского университета в 1906 г.
В дальнейшем В. В. Курилов изучает переход кристаллических веществ в коллоидное состояние. Ряд проведенных опытов дал ему возможность установить взаимосвязь и взаимообусловленность при превращении веществ неживой природы в состояние, присущее веществам живого организма.
К екатеринославскому периоду относятся исследования практического характера. По поручению губернского земства Курилов изучает почвы Екатеринославской губернии. Здесь ученый проявляет себя прекрасным организатором. Он вовлекает в работу агрономов, статистиков, почвоведов, геологов и др. Результаты выполнения задания губернского земства были обобщены в две научные работы1.
1 (В. В. Курилов и др. Почвенные исследования Екатеринославской губернии, настоящее их положение и их задачи по отношению к местному краю. Екатеринослав, 1907; Химия почвы с точки зрения эволюционного процесса. Журнал почвоведения, 1908, № 1, стр. 1-16.)
В. В. Курилов уделяет много времени и энергии общественной работе. По его планам в Екатеринославе был выстроен химический корпус Горного училища, там же им было создано научное общество и по его же инициативе это общество организовало Народный университет им. Караваева.
В 1909 г. В. В. Курилов одновременно был избран ординарным профессором Варшавского университета на кафедры неорганической и органической химии. Здесь он продолжает исследования в области дисперсных систем, разрабатывая вопросы химии коллоидов и химической классификации. Варшавский период наиболее плодотворный в деятельности ученого.
В 1912 г. В. В. Курилов заканчивает исследования в этом направлении и оформляет их в работе, в которой дает классификацию продуктов присоединения по принципу интенсивности. Согласно этому принципу, каждое вещество является носителем решительно всех ему присущих свойств, но интенсивность их проявления у различных веществ различна. Свою классификацию он основывает на законах постоянства состава, кратных отношений, действия масс и правила фаз, служивших одновременно базой для развиваемых им взглядов и критерием для суждения о веществе, как об определенном химическом соединении или как о продукте присоединения.
В соответствии с классификацией Курилова, первую группу составляют все вещества, которые обладают признаками определенных химических соединений; во вторую группу включаются продукты присоединения переменного состава, т. е. вещества, состав которых определяется природой и концентрацией реагентов, но при этом образованные по правилу валентности; к третьей группе относятся соединения переменного состава, которые нельзя выразить формулой с соблюдением валентности входящих в нее элементов, но которые подчиняются закону действия масс; для четвертой группы веществ сохраняется лишь неизменность состава во времени, т. е. это системы, к которым применимо правило фаз, и, наконец, к пятой группе принадлежат те продукты присоединения, состав которых изменяется во времени.
Таким образом, разработанную еще в 1905 г. схему непрерывной химической цепи веществ Курилов дополняет классификацией продуктов присоединения и этим завершает решение вопроса общей классификаци химических соединений.
Из развиваемых В. В. Куриловым представлений о постепенном изменении свойств веществ в зависимости от изменения сложности их частиц следовало, что в непрерывной химической пени соединений каждый средний член должен обладать свойствами смежных с ним членов. Так как продукты присоединения по существу есть комплексные соединения, то они должны обладать некоторыми свойствами, присущими комплексам.
В работе "Продукты присоединения и фотохимия гидрата хлорного хрома"1 он показывает, что комплексные соединения действительно, подобно продуктам присоединения, могут изменять свой состав под влиянием света. Так, зеленый гидрат хлорного хрома под влиянием света переходит в фиолетовый, что может быть объяснено реакцией
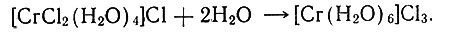
1 (В. В. Курилов. ЖРФХО, 47, 469 (1915).)
Кроме того, свойства растворов хлорного хрома близки к свойствам псевдорастворов продуктов присоединения. Зеленая окраска жидкой фазы также напоминает о сходстве, хотя и отдаленном, подобных веществ с природным хлорофиллом.
В. В. Курилов установил генетическую связь между комплексными соединениями и продуктами присоединения в том смысле, что комплексные соединения могут получаться за счет самопроизвольного распада продуктов присоединения, происходящего в зависимости от времени, температуры, концентрации и природы реагирующих молекул1.
1 (С точки зрения современной химии продукты присоединения составляют один из классов комплексных соединений (П. П.).)
В. В. Курилов был не только известным ученым, внесшим крупный вклад в сокровищницу отечественной химии, но и прекрасным педагогом-общественником, всегда стремившимся к популяризации и распространению научных знаний. Им написан и издан ряд учебников и пособий. Так, в 1909 г. в Екатеринославе вышел его учебник химии1. В 1910 г. в Варшаве был издан общий курс химии2.
1 (В. В. Курилов. Учебник химии. Начальные сведения из химии неорганической, органической и физической. Екатеринослав, 1909.)
2 (В. В. Курилов. Общий курс химии на современных основах. Варшава, 1910.)
В общем курсе химии изложены основы учения о химическом сродстве и свободной энергии, дано понятие о законе действующих масс и о правиле фаз, а также в надлежащем объеме теория растворов и гипотеза электролитической диссоциации С. Аррениуса. Здесь также рассматривается теория химического строения, необходимая в общем курсе химии для ознакомления с основами органической химии. Через весь курс химии автор проводит принцип изменения интенсивности свойств вещества, являющийся как бы своеобразным дополнением к периодической системе элементов.
Последний период научно-педагогической деятельности В. В. Курилова протекал в Ростовском университете, что было связано с эвакуацией Варшавского университета в Ростов-на-Дону. Этот период его жизни и научной деятельности освещается во второй части Очерков.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'