
2. Выделение молекулярного водорода микроскопическими водорослями
Важный природный феномен, который представляет большой интерес с точки зрения конверсии энергии, был обнаружен в 1942 г. Гаффроном и Рубиным [148]. При адаптации в темноте в анаэробных условиях в течение нескольких часов клетки Scetiedesmus obligenes при освещении начинают активно выделять водород. При этом общее количество выделившегося водорода в 10 раз превышает количество водорода, которое может образовываться в темноте. Поскольку микроскопические водоросли на свету способны продуцировать молекулярный кислород, представляется принципиальная возможность использовать механизм фотосинтеза для осуществления реакции биофотолиза воды с преобразованием световой энергии в топливную форму
2Н2О → 2Н2 + О2. (1.1)
Предельное теоретическое значение КПД преобразования солнечной энергии в системах получения водорода фотосинтетическим путем 35% по фотосинтетически активной радиации (15% по всему солнечному спектру) [149, 150].
В последующие десятилетия феномен образования водорода микроскопическими водорослями детально исследовался в ряде лабораторий. Обсуждение современного состояния этого вопроса дано в обзорных работах [151-153].
В целом выделение водорода микроводорослями характеризуется рядом особенностей. Образование молекулярного водорода у всех исследованных организмов протекает после определенного периода адаптации клеток в темноте в атмосфере инертного газа [154, 155]. В течение периода адаптации происходит активация гидрогеназы - терминального фермента, участвующего в образовании водорода. Возможен также дополнительный биосинтез фермента [156]. Зеленые микроводоросли способны выделять водород в темноте и на свету, однако на свету более интенсивно [157-161]. Насыщение "фотосинтеза водорода" происходит при существенно более низких интенсивностях света, чем поглощение СО2 и образование кислорода (300-5000 люкс) [160, 161]. Исследование кинетики фотовыделения водорода клетками Scenedesmus obligenes показало, что процесс имеет по крайней мере двухстадийный характер [162]. Наблюдаемое в начальный момент времени достаточно интенсивное выделение водорода меняется на сравнительно мало интенсивный стационарный процесс. Это наблюдение можно объяснить [162] наличием в первоначальный момент определенных количеств донора электронов, который быстро истощается в процессе реакции. При этом происходит смена лимитирующей стадии, стационарное выделение водорода определяется более медленным процессом образования этого донора, например в цикле Кребса. Добавление глюкозы или ацетата существенно стимулирует процесс фотообразования водорода (на 1 М глюкозы образуется 0,5 М Н2). Фотовыделение водорода на свету и в темноте сопровождается образованием углекислого газа [148, 157, 151]. Присутствие в газовой фазе значительных количеств углекислого газа, кислорода или водорода ингибирует процесс фотообразования водорода [148].
Важным является то обстоятельство, что процессы образования водорода и кислорода конкурируют друг с другом [151]. Культура Chlorella pyrenoidosa, адаптированная в анаэробных условиях при низких интенсивностях света, выделяет только водород. С увеличением интенсивности света уменьшается выделение водорода, затем регистрируется образование кислорода; переход выделения от кислорода к водороду обратим. Существует точка в значении интенсивности света, при которой отсутствует выделение как водорода, так и кислорода. Однако одновременное эффективное выделение кислорода и водорода наблюдать не удается [151].
В целом в клетках зеленых микроводорослей может протекать целый ряд реакций [162].
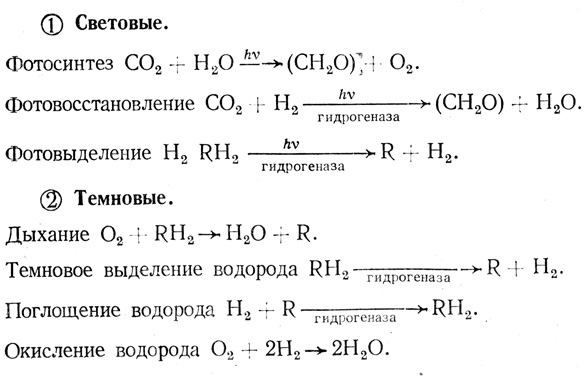
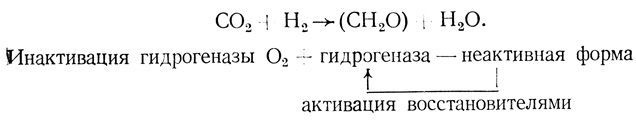
Протекание всей этой совокупности процессов с учетом регуляторных взаимодействий и обеспечивает достаточно сложную картину эффектов, описанную выше. Предполагается при фотообразовании водорода участие электронно-транспортной цепи фотосинтеза. Принципиальным вопросом при фотообразовании водорода в клетках микроводорослей является вопрос о доноре электронов в электронно-транспортную цепь. При условии, что донором электронов является вода на уровне фотосистемы II, можно было бы ожидать стехиометрического разложения воды на водород и кислород и осуществления реакции ее биофотолиза (схема I.I). Один из подходов к выяснению этого вопроса заключается в использовании ингибиторов, специфически блокирующих различные участки электронно-транспортной цепи. Классический ингибитор фотосистемы II диурон (рис. 7) даже при высоких концентрациях ингибирует реакцию фотовыделения водорода не полностью [151, 152]. (При этом полностью блокирует электронный транспорт на уровне фотосистемы II.)
![Рис. 7. Схема возможных путей фотообразования молекулярного водорода микроводорослями [151, 153]](pic/000019.jpg)
Рис. 7. Схема возможных путей фотообразования молекулярного водорода микроводорослями [151, 153]
Это указывает на то, что определенная часть водорода образуется без участия фотосистемы II, и донирование электронов происходит на уровне фотосистемы 1. В зависимости от вида водорослей степень участия фотосистемы II может варьироваться (табл. 10).
![Таблица 10. Участие фотосистемы II в световом выделении молекулярного водорода водорослями (данные работы [162])](pic/000020.jpg)
Таблица 10. Участие фотосистемы II в световом выделении молекулярного водорода водорослями (данные работы [162])
Таким образом, около половины фотообразовавшегося водорода возникает с участием фотосистемы II, донором которой является вода, другая половина образуется при донировании электронов в электронно-транспортную цепь фотосистемы I. В целом схему возможных путей фотообразования молекулярного водорода иллюстрирует рис. 7 [151, 153], где D - восстановленные органические соединения - доноры электронов.
Практическое использование феномена фотовыделения водорода макроскопическими водорослями для конверсии световой энергии в настоящее время еще не реализовано. Это связана с тем, что эффективность выделения водорода в стационарном режиме достаточно мала. Возможно, дальнейшее исследование, оптимизация и увеличение эффективности процесса создадут условия технологической эксплуатации этого явления.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'