
Термически модифицированный полиакрилонитрил
Термическая обработка полиакрилонитрила в анаэробных условиях приводит к его химической модификации. Термически обработанный полиакрилонитрил - достаточно хорошо изученный полимерный полупроводник [542]. При термической обработке до 300°С образуются предпочтительно структуры типа I, при обработке при 850°С - типа II:
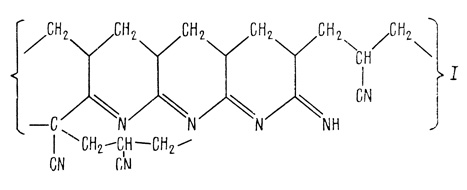 (4.18)
(4.18)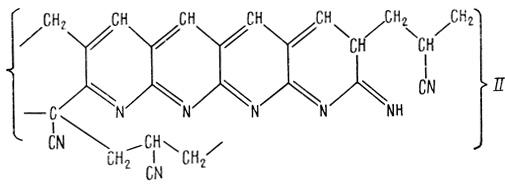 (4.19)
(4.19)Электропроводность образцов зависит от температуры термической обработки.
Полученные носители модифицировали следующим образом: 1) окисление концентрированной азотной кислоты (введение нитро- и оксогрупп); 2) обработка гидразином; 3) восстановление с образованием аминогрупп.
Иммобилизацию гидрогеназы проводили на окисленных образцах термически обработанного полиакрилонитрила, на образцах после гидрозинолиза и восстановления с использованием бифункционального реагента - глутарового альдегида. В ряде экспериментов гидрогеназу иммобилизовали на окисленный полимер, обработанный гексаметилендиамином.
Был обнаружен интересный факт: иммобилизация фермента на матрице, обладающей высокой электропроводностью, приводит к обратимой инактивации фермента. При нагревании матрицы с иммобилизованным ферментом последний может быть "снят" с матрицы. Это иллюстрирует рис. 64, на котором приведено изменение во времени активности гидрогеназы при инкубации фермента при температуре 70°С. Нагревание образца приводит к гидролизу шиффового основания, связующего фермент с носителем и переход фермента в раствор (гидрогеназная активность обнаруживается в растворе). Обработка образца с иммобилизованным ферментом боргидридом натрия, восстанавливающего шиффово основание, приводит к необратимой "фиксации" фермента на носителе в неактивном состоянии.
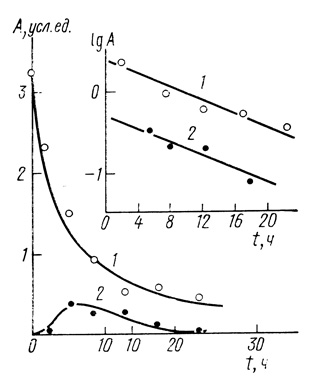
Рис. 64. Зависимость активности гидрогеназы Т. roseopersicina от времени инкубации при 70°С; pH 8,0; 0,01 М Na3BO3; 0,2 М КН2РO4: 1 - исходный фермент; 2 - иммобилизованный на полиакрилонитриле, прогретом при 850°С обработанном гидразином
Интересно отметить, что существует определенная корреляция между степенью окисления термически обработанного полиакрилонитрила и активностью иммобилизованного фермента (табл. 33). Аналогичная зависимость наблюдается между электропроводностью матрицы и остаточной активностью фермента (табл. 34).
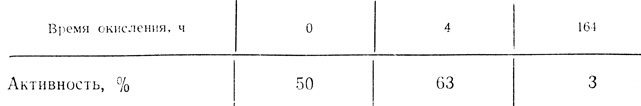
Таблица 33. Зависимость между временем окисления азотной кислотой полиакрилонитрила, термически обработанного при 190°С, и начальной активностью иммобилизованной гидрогеназы

Таблица 34. Зависимость между электропроводностью термически обработанного полиакрилонитрила и начальной активностью иммобилизованной гидрогеназы
Обратимую инактивацию гидрогеназы матрицей можно интерпретировать как следствие образования специфического комплекса между носителем и активным центром фермента (например, комплекса с переносом заряда). На это указывает то, что иммобилизация фермента через "ножку" гексаметилендиамина - глутарового диальдегида не приводит к инактивации фермента. Аналогично, фермент сохраняет свою активность при иммобилизации на пористом стекле. Данные по термической стабильности полученных образцов иммобилизованной гидрогеназы приведены на рис. 65.
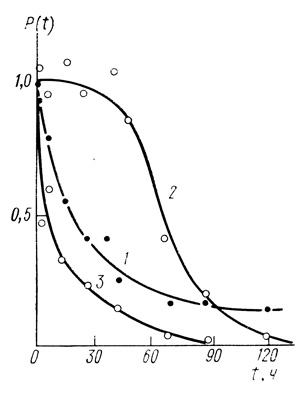
Рис. 65. Стабильность гидрогеназы Т. roseopersicina при 70°С; pH 8,0; 0,15 М КН2РO4; 0,5 КСl. 1 - исходный фермент; 2 - фермент, иммобилизованный на термически обработанном при 300°С полиакрилонитриле, окисленном в течение недели концентрированной азотной кислотой и обработанным гексаметилендиамином; 3 - фермент, иммобилизованный на пористом стекле, обработанном γ-аминопропилэтоксисиланом
Важно подчеркнуть, что неактивный фермент, иммобилизованный на матрицах с высокой электропроводностью или степенью окисления, может быть активирован продолжительным восстановлением матрицы с ферментом восстановленным метилвиологеном. При этом исчезает характерный период индукции, достигающий в ряде случаев 100 мин (рис. 66). Таким образом, термически модифицированный полиакрилонитрил, обладающий высокой электропроводностью, может служить носителем для иммобилизованных ферментов, емкость носителя до 200 мг белка на грамм полимера. Полученный гетерогенный катализатор можно использовать в качестве компонента композиционных электродных материалов.
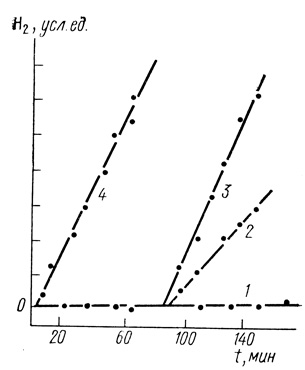
Рис. 66. Активация гидрогеназы Т. roseopersicina, иммобилизованной на термически обработанном при 300°С полиакрилонитриле, окисленном концентрированной азотной кислотой в течение недели: 25°С; pH 8,0; 0,15 М КН2РO4; 0,5 КСl; 1 - исходный иммобилизованный фермент; 2 - после добавления 0,82 г⋅экв Mv+ на грамм носителя; 3 - после добавления 1,34 г⋅экв. Mv+ на грамм носителя; 4 - после добавления 15 г⋅экв. Мv+ на грамм носителя
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'