
Резервы железа
Красные кровяные шарики - эритроциты живут всего около двух месяцев, затем они разрушаются и заменяются новыми. В то же время железо, которое содержится в эритроцитах (в форме гемоглобина), практически не выводится из организма. Человек получает очень немного железа с пищей, поэтому создается впечатление, что железо совершает в организме какой-то круговорот. Следовательно, должно существовать депо - "склад", предназначенный для хранения соединений железа, уже использованных ранее для создания гемоглобина и теперь дожидающихся, когда они снова понадобятся.
Ферритин. Надо иметь в виду, что ионы железа(III) не безвредны - в свободном (т. е. гидратированном) состоянии они обладают токсическими свойствами. Железо в такой степени окисления сохраняется в организме лишь после предварительного обезвреживания.
В 1937 г. из селезенки лошади был получен железосодержащий белок, названный ферритином и оказавшийся тем самым веществом, которое и сохраняет ионы железа (III) в нетоксичной форме. Позже выяснилось, что ферритин встречается не только в органах животных, но и у растений и даже у грибов.
У человека приблизительно 1/4 всего железа, совершающего круговорот, находится в форме ферритина, т. е. в депо, а около 3/4 - в гемоглобине крови.
В ферритине соединения железа связаны с белком и не проявляют токсичности; освобождение железа из ферритина сопряжено с восстановлением иона Fe3+ до степени окисления +2. Молекулярная масса ферритинового белка равна 450000, а у некоторых видов достигает 900000, иначе говоря, очень велика; ферритин окрашен в красно-коричневый цвет и содержит до 4500 атомов железа на молекулу белка.
Ферритин представляет собой белковые частицы, внутри которых, закутанные в полипептидные цепи, находятся ядра, или мицеллы, состоящие из сложных комплексов гидроксида и фосфата железа. Предполагают, что их состав можно приблизительно выразить формулой: (FeO-OH)8*(FeO-ОРО3Н2).
Состав белковой части ферритина в настоящее время известен. В этом белке много остатков глутаминовой кислоты, серина и лейцина, а также аспарагиновой кислоты. Как часто наблюдается у белков, молекула ферритина сложена из меньших по размеру субъединиц; формой она напоминает тутовую ягоду - 20 или 24 небольшие сферические частицы окружают центральное ядро, состоящее из соединений железа. Имеются данные, свидетельствующие о кристаллическом строении ядра; сам ферритин также можно получить в кристаллической форме.
Трансферрины. Ферритин не мог бы успешно выполнять свои функции, если бы не существовало специальных средств доставки ионов железа(III) к клеткам (называемым ретикулоцитами), в которых происходит образование гемоглобина. Дело в том, что при тех значениях кислотности, которые характерны для физиологических условий (рН около 7), ионы железа(III) существуют в виде гидроксида; растворимость его очень мала, и поэтому концентрация ионов железа(III) в растворе, находящемся в равновесии с гидроксидом, составляет ничтожно малую величину, порядка 10-14 моль/л. Из раствора такой концентрации очень трудно "вылавливать" ионы железа. В сыворотке крови, в яичном белке, в молоке, в желудочном соке и других жидкостях и тканях организма были найдены особые белки, отличающиеся способностью активно связывать железо в форме ионов Fe3+. Эти белки получили общее название трансферринов ("переносчики железа"); некоторые ученые делят их на классы: лактоферрины (содержатся в молоке), кональбумин (из яичного белка), сывороточный трансферрин (из крови) и др. Их белковые составные части немного отличаются друг от друга (особенно по содержанию гистидина и аргинина). Молекулярные массы трансферринов лежат в пределах от 77100 до 82000. Эти белки не имеют субъединиц и представляют собой частицы, состоящие из одной полипептидной цепи.
Каждая молекула трансферрина связывает два иона железа(III), причем получается продукт красного цвета. Было доказано, что в реакции связывания принимает участие ион бикарбоната, а ионы железа вытесняют шесть ионов водорода на одну молекулу белка. Поэтому реакцию можно схематически представить так:

Каждая молекула трансферрина связывает два иона железа(III)
Предполагается, что ион бикарбоната увеличивает прочность связи между ионом железа и белком трансферрина. Самым замечательным свойством трансферрина является то, что этот белок "знает", по какому адресу надо доставить ионы железа. Каким-то образом трансферри-новые частицы отличают ретикулоциты от всех других клеток и отдают железо именно клеткам, производящим гемоглобин.
Сначала, по-видимому, трансферрин прочно связывается (адсорбируется) на поверхности ретикулоцита, затем связь между ними упрочняется, и железо переносится в клетку. Возможно, что повышение прочности связи и сопровождается внедрением трансферрина внутрь клетки. Прочность связи ретикулоцит - трансферрин зависит от содержания железа в последнем. Как только железо отдано, связь сразу ослабляется, и белок трансферрина выходит из клетки.
Почти полмиллиона молекул трансферрина может быть размещено на поверхности ретикулоцита. Что происходит дальше и как именно строится молекула гемоглобина в ретикулоцитах, пока еще не выяснено...
Заметим, что кональбумин, содержащийся в яичном белке, играет роль антимикробного фактора и защищает куриные яйца от порчи. Дело в том, что, энергично соединяясь с железом, содержащимся в микроорганизмах, кональбумин прекращает их жизнедеятельность. Так природа экономно использует одно и тоже вещество, применяя его для решения множества разнообразных задач.
Гемэритрин. Химические машины, работающие в организмах, не всегда были такими, какими их сейчас видят биохимики в высокоорганизованных организмах. По мере постепенного развития и усложнения форм жизни изменялись и совершенствовались механизмы обмена веществ. В организмах некоторых беспозвоночных (например, морских червей) функции переноса кислорода выполняет соединение железа - гемэритрин, совершенно не похожее на гемоглобин и не содержащее порфиринового кольца. В этом соединении ионы железа связаны с аминокислотными остатками полипептидной цепи белка, причем для того, чтобы присоединить одну молекулу кислорода, требуется два иона железа (а в гемоглобине - один). Удалось установить, что в гемэритрине пара ионов железа окружена аминокислотными остатками гистидина (четыре остатка) и тирозина (два остатка); предполагают, что и другие аминокислоты (глутаминовая, аспарагиновая кислоты, метионин) участвуют в образовании группировки, окружающей ионы железа.
Свойства железа в таком соединении необычны: при связывании кислорода резко падает магнитная восприимчивость и изменяется окраска гемэритрина - бесцветное соединение становится розово-красным.
Применение наиболее мощных, современных методов исследования (спектроскопия Мессбауера) позволило сделать вывод, что ионы железа в активном центре гемэритрина находятся в различном положении и связаны через кислородный мостик сильным электронным взаимодействием. Возможно следующее расположение ионов железа:
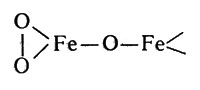
Ионы железа в активном центре гемэритрина находятся в различном положении и связаны через кислородный мостик сильным электронным взаимодействием
Молекула кислорода, по-видимому, присоединяется к мостиковой группе. Возможно, что в результате присоединения кислорода железо(II) переходит в железо(III).
Крупная молекула гемэритрина имеет молекулярную массу около 108000 и состоит из восьми субъединиц (по два атома Fe в каждой). Биологическая роль гемэритрина заключается не только в переносах, но и в резервном хранении связанного кислорода, чем этот белок существенно отличается от гемоглобина. Гемэритрин, по-видимому, выполняет функции и гемоглобина, и миоглобина в организмах беспозвоночных.
В организмах обнаружен ряд белков, способных прочно связывать железо(III). Так, в яичном желтке содержится фосвитин, подавляющий всасывание железа при употреблении яиц в пищу. В желудочном соке найден белок, названный гастроферрином, также прочно соединяющийся с ионами железа. Биологическая роль таких белков не вполне ясна, но высказывается предположение, что они служат в качестве регуляторов поступления железа в клетки. Слишком большой приток ионов железа может оказать вредное действие на клеточные механизмы, поэтому регулирующий аппарат необходим для наиболее эффективной работы биологических машин.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'