
Медь. Медьсодержащие оксидазы
Кроме ионов железа, функцию переноса кислорода и переноса электронов способны выполнять и ионы других металлов, в частности ионы меди.
Соединение, называемое гемоцианином, представляет собой белок, содержащий медь в ионном состоянии. Еще в 1847 г. Харлес, исследуя голубую кровь улитки, пришел к выводу, что голубой цвет обусловлен содержа нием в крови улитки меди вместо железа. Греческое слово "гемоцианин" и означает "синекровный". Гемоцианины различных видов были найдены в моллюсках и членистоногих (в крабах, осьминогах, кальмарах и т. д.), в паукообразных, ракообразных и даже в сороконожках.
Молекулярная масса гемоцианинов колеблется в широких пределах - от 36000 до 825000. Молекула гемоцианина состоит из нескольких равных частей - субъединиц, число которых неодинаково у гемоцианинов различного происхождения. Молекулярная масса наименьших субъединиц равна 36700 (у членистоногих), при содержании меди 0,173%, и 25100 (у моллюсков), при содержании меди 0,253%.
В составе гемоцианина медь находится в степени окисления +1. Предполагается, что два иона меди связывают одну молекулу кислорода: Cu+ - О2 - Cu+, причем возможны состояния Cu2+ - O2- - Cu+ и Cu+ - O2- Cu2+ Медь, несомненно, связана с какими-то лигандами, но их точный состав не известен. Возможно, что лигандами являются аминогруппы или дисульфидные мостики белка.
Число активных центров гемоцианина, т. е. пар ионов меди, связывающих одну молекулу кислорода, колеблется от 6 до 200, смотря по тому, из каких организмов получен гемоцианин.
Гемоцианин - отнюдь не единственное природное соединение меди. В крови и различных органах животных (почки, печень), а также в тканях растений (огурцы, кабачки, лаковое дерево) и грибов найдена медь, находящаяся там в виде комплексных ионов. Насколько можно судить, комплексообразование происходит между ионами меди и различными участками полипептидной белковой цепи; установлено, что медь часто выполняет те или иные биохимические функции совместно с соединениями железа.
Широкая распространенность в природе белков, связанных с ионами меди, и важность сочетании железо - медь в биохимических реакциях, сопровождающих переносы электронов и окисление пищевых веществ, стимулировали исследования роли меди в процессах жизнедеятельности. Но, несмотря на всю мощь современных физико-химических средств анализа, до сих пор не удалось охарактеризовать медь с такой полнотой, какая достигнута по отношению к соединениям железа.
Установлено, что медьсодержащие белки (например, стеллацианин, получаемый из лакового дерева) служат переносчиками электронов. Ионы меди в белках катализируют реакции гидроксилирования и окисления. Последние особенно важны.
Ферменты, ускоряющие реакции окисления, - оксидазы - довольно многочисленны и содержат ионы меди в различных состояниях. Мы рассмотрим некоторые типичные примеры.
Оксидазы, в молекуле которых содержится не менее четырех атомов меди на молекулу фермента, ускоряют восстановление кислорода до воды. Их синяя окраска настолько интенсивна, что эту группу оксидаз иногда называют "синие оксидазы", в отличие от другой группы оксидаз, в молекуле которых всего один-два атома меди ("несиние оксидазы"). Они окрашены менее ярко и катализируют восстановление кислорода до пероксида водорода.
К синим оксидазам относится церулоплазмин - медьсодержащий белок, найденный в плазме крови человека и многих позвоночных (свиньи, лошади, коровы, олени, собаки, кошки и др.). Церулоплазмин плазмы человека содержит всего 0,3 масс. % меди, имеет молекулярную массу 151000. Вероятно, в его молекуле - четыре полипептидные цепочки, две из которых обладают сравнительно небольшой длиной (масса их около 16000) и две длинные (молекулярная масса около 60000). Церулоплазмин удалось получить также в виде кристаллов. Доказано наличие в этом белке и небольшого количества углеводов (8%). Церулоплазмин катализирует окисление ионов железа(II) в ионы железа(III), что может служить объяснением механизма совместного действия обоих этих ионов в процессах переноса электронов и активизации железа. Каталитически ускоряются церулоплазмином реакции окисления полиаминов и полифенолов - обычных составных частей обмена веществ в организмах.
Медь связана с белком церулоплазмина очень прочно, и, по-видимому, на одну молекулу белка приходится шесть атомов меди. Действие ионов меди в реакциях окисления сводится к попеременному окислению и восстановлению, т. е. к переходам типа:
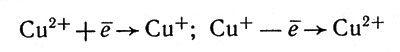
Действие ионов меди в реакциях окисления сводится к попеременному окислению и восстановлению
Имеются данные, показывающие, что только половина атомов меди находится в степени окисления +2; эти ионы окисляются и восстанавливаются по указанной схеме, обратимо. Ионы меди в степени окисления +1 окисляются очень трудно и только при разрушении белковой части фермента. Ионы меди(I) тоже не вполне одинаковы - два из четырех связаны с атомами серы. Пока не ясно, все ли атомы меди принимают участие в указанных выше реакциях окисления-восстановления.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'