
Как строится молекула воды
Вспомним, что вероятностное нахождение электрона по отношению к ядру определяется электронным облаком, т. е. совокупностью всех точек пространства, через которые может пробежать электрон. Это воображаемое облако называют орбиталью. Установлено: на одной орбитали не может находиться одновременно более двух электронов.
Единственный электрон атома водорода (1 s1) имеет орбиталь в виде сферы. Такая форма орбитали соответствует минимально возможному уровню энергии атома.
В атоме кислорода все гораздо сложнее. Атом кислорода имеет два слоя электронов. Внутренний (слой К.) укомплектован двумя s-электронами, вращающимися по сферической орбитали (условное обозначение этих электронов 1 s2, где 1 - номер слоя, s - энергетическое состояние - орбиталь, 2 - количество электронов на орбитали).
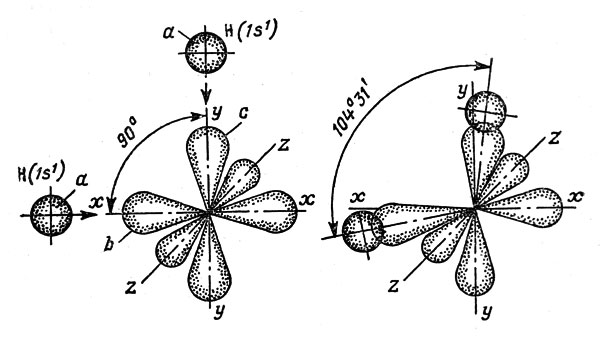
Рис. 10. Схема образования молекулы Н2О. Сферические электронные облака атомов водорода захватываются р-орбиталями вис атома кислорода. Получившие дополнительный отрицательный заряд орбитали вис отталкиваются на угол 104°31'
Внешний слой h имеет шесть электронов (их условное обозначение 2 s2p4, где 2 - номер слоя, s и р - орбитали, индексы 2 и 4 - соответственно количество электронов на орбиталях). В этом слое, как видно из условного обозначения, два s-электрона имеют одну и ту же сферическую орбиталь. Четыре р-электрона вынуждены расположиться на трех взаимно перпендикулярных орбиталях, имеющих в плане формы восьмерок. Восьмерки пересекаются в центре атома, как показано на рис. 10. Обратите внимание: 4 р-электрона на трех орбиталях. Здесь ключ к пониманию всех событий.
Орбиталь, вытянутая вдоль оси г, служит пристанищем для двух электронов. Она укомплектована, и ворота ее на прочном запоре. На орбиталях же х и у по одному электрону и, значит, по одному изготовленному "капкану".
Итак, действующие лица охарактеризованы. Начинается действие.
Вот атом водорода оказался в опасной близости от атома кислорода, и единственный его электрон тотчас же будет захвачен непарной (недоукомплектованной) р-орбиталью. Поскольку у кислорода две непарные орбитали, он способен пленить два атома водорода. При атом сферическое облако водородного s-электрона належится на яйцеобразную ветвь р-орбитали (см. рис. 10).
Между атомами Н и О возникает связь, которая получила название ковалентной. Итогом этой связи и будет возведение весьма своеобразного архитектурного сооружения, известного как Н2О. Своеобразие же образовавшейся молекулы состоит в следующем.
Во-первых, перекрытие электронных облаков приведет к уплотнению области перекрытия и, значит, к росту отрицательного заряда в этой части пространства.
Расположись атомы водорода по обе стороны от ядра атома кислорода под углом 180°, и возникшие уплотнения зарядов никак не отразились бы на электрическом равновесии образовавшейся системы, т.е. центры положительных и отрицательных зарядов по-прежнему находились бы в одной точке - в центре атома кислорода. Но р-орбитали, захватившие водородные электроны, расположены под углом 90°, и поэтому уплотнения в них вызовут смещение центра тяжести отрицательного заряда относительно центра тяжести положительного заряда. Образовавшаяся молекула коды стала одновременно маленьким микромагнитом или, как принято говорить в молекулярной физике, диполе м, способным ориентироваться в магнитном поле.
Во-вторых, ветви р-орбиталей, получившие дополнительные отрицательные заряды, получат и дополнительную силу взаимного отталкивания. Они подальше отодвинутся друг от друга, и угол между ними вместо 90° станет 104°31. Увеличение угла еще более усугубит несимметричность распределения зарядов. В связи с этим дипольный момент молекулы достигнет такой величины, какой не имеют молекулы никаких других веществ на Земле.
И, наконец, в-третьих, сгущение сферического облака s-электрона водородного атома в месте наложения его на р-орбиталь атома кислорода приведет к разрежению этого облака с диаметрально противоположной стороны. Протон водорода, до того равномерно прикрытый сферическим электронным облаком, после "пленения" атомом кислорода окажется оголенным с внешней стороны. Однако ему представляется возможность "прикрыть свою наготу" за счет электронного облака соседней молекулы Н2О. И он сделает это, вцепившись в "одежду" (облако) чужого атома кислорода с силой, которая значительно превзойдет силу, удерживающую его собственный электрон. Эта сила связи с "чужим" атомом кислорода и будет представлять собой так называемую водородную связь.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'