
Глава VII. Медь - древнейший металл
Медь в истории человечества
Вероятно, первый металл, с которым познакомился человек еще во времена нового каменного века (около 6 тыс. лет назад на Древнем Востоке и около 4 тыс. лет назад в Европе), была медь. Она встречается в природе В самородном состоянии в виде пластинок, губчатых и сплошных масс, а также кристаллов. Самый крупный из найденных самородков весил 420 т. Медные самородки гораздо больше распространены в природе, чем самородки других металлов. Поэтому естественно, что в поисках подходящих пород для изготовления орудий человек в первую очередь встретился именно с медными самородками. Эта встреча знаменовала собой начало медного века.
Надо полагать, человек довольно быстро оценил преимущества нового материала. Возраст предметов из самородной меди достигает 6 тыс. лет. Особенно крупные самородки находили в Северной Америке на берегах Гудзонова залива и Верхнего озера. Первые орудия человека были сделаны из камня, поэтому первые медные изделия появились на свет в результате обработки медных самородков каменными топорами. Длительное время затем каменные и медные орудия применялись совместно. В этот период человек на примере меди постигал основы металлургии и металловедения.
Обработка медных самородков с помощью каменного топора имела, конечно, ограниченные возможности. Холодной ковкой самородков пластинчатой формы можно было изготовить небольшие по величине предметы - булавки, крючки, наконечники стрел и т. п. Получить же листовую медь холодной ковкой невозможно - материал растрескивается. Также невозможно изготовить холодной ковкой предметы сложного профиля: сосуды, сковороды и др. К тому времени человек уже уверенно управлял огнем. Лагерный костер с температурой 700-800 °С сменили печи, где достигалась более высокая температура - 1000-1200 °С. На территории Египта, например, были найдены керамические сосуды, датированные 5 тыс. лет до н. э., обжиг которых был проведен при 1100-1200 °С. Медь плавится при температуре 1084 °С, поэтому, естественно, что следующим шагом в металлургической практике человека явилось, получение расплавленной меди. Это существенно расширило ассортимент изготовляемых из меди изделий.
Однако самородная медь встречается редко, и ее было явно недостаточно, чтобы удовлетворить стремительно растущие потребности в этом металле. На следующем этапе человек начал получать медь восстановительной плавкой ее руды. Медные руды - природные минералы, агрегаты, содержащие медь в таких количествах и соединениях, при которых извлечение металла экономически выгодно. В настоящее время известно свыше 170 медьсодержащих минералов, из них только 10-15 имеют практическое значение. К важнейшим минералам относятся: халькопирит CuFeS2 (30 % меди), халькозин - "медный блеск" Cu2S (79,8% меди), ковелин CuS (64,4% меди), малахит CuCО3·Cu(OH)2 (57,4% меди), азурит 2CuCО3·Cu(OH)2 (55,5 % меди), куприт Cu2О (81,8% меди). Руды современных промышленных месторождений почти никогда не бывают сложены только одними минералами меди. Обычно медьсодержащие минералы срастаются с нерудными минералами (кварц, барит и др.) и некоторыми рудными минералами железа и цветных металлов (пирит, пирротин и др.).
Месторождения медных руд распространены гораздо шире, чем месторождения крупных медных самородков, и были известны человеку с глубокой древности. Сейчас трудно выяснить, как именно была открыта выплавка меди из руд и произошло ли это существенно позже, чем человек встретился с самородной медью. Имеются данные, что уже за 7 тыс. лет до н. э. на Ближнем Востоке употреблялась металлургическая медь. Добыча самородной меди и выплавка меди из руд - операции, существенно отличающиеся в техническом и технологическом отношениях, по-видимому, в разных районах мира осваивались человеком одновременно.
Первоначально использовались окисленные руды. Они не требуют предварительного обжига в отличие от сульфидных руд, для которых такая обработка необходима, чтобы удалить химически связанную серу. Восстановительная плавка малахитовых руд проводилась в примитивных печах. Они представляли собой глиняные тигли, наполненные рудой и углем, которые помещались в неглубокую ямку. Поверх насыпали слой древесного угля.
Уголь, сгорая, образует оксид углерода (II), который взаимодействует с малахитом, восстанавливая химически связанную медь до металла:
CO + CuCО3 = 2CО2+Cu
Крытое устройство печей обеспечивало изоляцию реакционной среды от избытка кислорода воздуха, который окисляет оксид углерода (II) в оксид углерода (IV) и тем самым мешает восстановлению меди. Неизвестно, как человек пришел к мысли, что медь надо выплавлять именно так, но, очевидно, у него для экспериментов было много времени и упорства. Имеются свидетельства очень раннего знакомства человека с металлургической выплавкой меди. В Египте, например, обработка медных руд Синайского полуострова велась уже в IV тысячелетии до н. э. С глубокой древности были известны медные руды на острове Кипр. Предполагается, что слово "купрум", научное название меди, произошло от наименования острова Кипр, где находились медные рудники древних римлян.
В Европе древние медные копи найдены в Австрии на Миттерберге. Там же обнаружены каменные орудия, которыми эти копи разрабатывались. Предки древних славян, жившие в бассейне Дона и Преднепровье, использовали небогатые месторождения меди, находившиеся в районе нынешнего Донбасса и затопленных Днепровских порогов. Они применяли медь для изготовления оружия, предметов домашнего обихода, украшений.
По мнению некоторых ученых, русское слово "медь" произошло от слова "смида", которое у некоторых древних племен, живших на европейской части современной территории СССР, обозначало вообще металл. На рубеже XVII-XVIII вв. начало промышленной переработки меди в России было положено Никитой Демидовым. В музее Тагила имеется огромный раскладной медный стол, на котором сделана надпись: "Сия первая в России медь отыскана в Сибире... Никитою Демидовиче.м Демидовым по грамотам великого Государя Императора Петра Первого в 1702 и 1706 и 1709 годах, а из сей первовыплавленной меди сделан оный стол в 1715 году".
После того как человек научился получать и обрабатывать медь, несколько тысячелетий наряду с камнем она являлась основньш твердым материалом древности (рис. 12). Уже первобытные металлурги пытались повысить твердость этого в чистом виде довольно мягкого металла. Первоначально, по-видимому, случайное образование сплава меди с оловом, которое могло произойти при обработке некоторых руд, содержащих вместе олово и медь, определило направление поисков улучшения механических свойств меди. Удачное соединение меди с оловом воспроизводилось человеком уже сознательно.
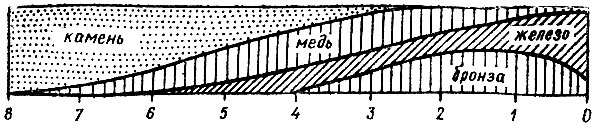
Рис. 12. Основные твердые материалы древности
Естественно, что испытывались композиции меди и с другими металлами (цинк, мышьяк, никель и др.). Сплав меди с цинком получали, например, в Древнем Иране. Медно-мышьяково-никелевая четырехгранная приколка, найденная в Азербайджане, имеет возраст более 5 тыс. лет. Предметы, изготовленные из медно-никелевых сплавов, найдены в Германии, Испании, Португалии и относятся примерно к тому же периоду.
Особое место в практической деятельности человека занимает бронза - сплав меди с оловом. Бронза превосходит медь по твердости, хорошо поддается обработке, очень устойчива к окислению. Период истории приблизительно с начала III тысячелетия до н. э. до начала I тысячелетия до н. э. называют бронзовым веком. В это время появились новые, более разнообразные орудия и предметы вооружения, сделанные из бронзы (топоры, ножи, серпы), появилась бронзовая утварь - кубки, чаши, котлы и т. п. Изделия из бронзы отливались у египтян, индусов, ассирийцев. Широко использовалась бронза для изготовления украшений, статуй и других предметов художественного творчества.
Статуя высотой 32 м, созданная в 290 г. до н. э. в честь бога солнца Гелиоса - Колосс Родосский, была отлита из бронзы и поставлена на самом восточном острове Эгейского моря - Родосе, у входа в порт. В Японии в 749 г. была отлита и помещена в храм Тодайдзи четырехсоттонная статуя Будды. О большом распространении бронзы в искусстве древнего мира можно судить по дошедшим до нас статуям (Дискобол, Спящий сатир, Марк Аврелий и др.). Само слово "бронза" имеет относительно позднее происхождение и связано с названием итальянского торгового городка на берегу Адриатического моря Бридзини, где продавались разнообразные изделия из бронзы.
По мере того как человечество накапливало технический и технологический опыт, наряду с бронзой появились и другие сплавы меди, обладающие различными ценными свойствами. В настоящее время известно большое количество сплавов, которые медь образует с другими элементами: Zn, Sn, Al, Ni, Pb, Mn, Be, Fe, Mg, Hg, Ag, Au, Si. Широкое распространение медных сплавов объясняется тем, что разные группы их имеют разные достоинства. К этим достоинствам можно отнести антифрикционность, коррозийную стойкость, пластичность, хорошие литейные свойства, красивый внешний вид и т. п. Сплавы меди с цинком называются латунями и по составу делятся на красные латуни (меньше 20% Zn), обладающие хорошей текучестью; желтые латуни (20-50% Zn); хрупкие белые латуни (50-80% Zn) и специальные латуни, которые наряду с медью и цинком содержат Ni, Mn, Fe, Sn и Al.
Бронзой раньше называли только сплав меди с оловом. Из-за дефицитности олова сплавы с аналогичными свойствами стали получать, добавляя к меди другие металлы. Теперь, помимо оловянных, широко используются алюминиевые, свинцовые, кремниевые, кадмиевые и другие бронзы. Все эти сплавы содержат небольшие количества легирующих компонентов, которые улучшают те или иные их качества. Из-за большого разнообразия, свойств применение медных сплавов издавна было весьма широким. Из бронзы состава 90% меди и 10% олова отливались артиллерийские орудия. Сплав, состоящий из 76-82 % меди, 16-22 % олова и до 4 % свинца, использовался для отливки колоколов. Из такого колокольного металла сделаны один "часовой" и 10 "четвертных" колоколов Спасской башни Московского Кремля. Эти колокола отлиты в XVII-XVIII вв. и весят: "часовой" - 2160 кг, "четвертные" - от 300 до 350 кг.
Для изготовления художественных изделий пользуются сплавом, содержащим 70-80 % меди, до 10 % цинка, 5-8 % олова и 3 % свинца. Это так называемая художественная бронза. В 1863 г. на одном из островов (Мас-а-Тьерре) в 600 км от побережья Чили была установлена отлитая из художественной бронзы мемориальная доска шотландскому моряку Александру Селкирку - прототипу знаменитого Робинзона Крузо. В Московском Кремле в Успенском соборе находится выполненный в 1625 г. из художественной бронзы шатер ажурного литья - образец высочайшего мастерства русских умельцев. История литья статуй из бронзы в России начинается с эпохи Петра I. В 1714 г, была отлита первая статуя Самсона для фонтана в Петергофе. Труднейшее литье в один прием знаменитого "Медного Всадника" - монумента Петру I, провели по проекту скульптора Э. Фальконе в 1775 г. При Академии художеств в Петербурге в 1764 г. был основан "Литейный дом", в котором выполнялись из бронзы многочисленные предметы для украшения дворцов, а также скульптурные работы.
Производство меди. Медьсодержащие минералы в чистом виде в промышленных масштабах не встречаются. В кусках руд тесно переплетены между собой минералы, содержащие разные элементы. Они срастаются, образуют небольшие вкрапления. Обычно медные руды содержат от 0,5 до 2 % меди. Только в Конго встречаются месторождения, содержание меди в которых доходит до 20 %. Малая концентрация меди в рудах затрудняет ее добычу, и производство меди становится сложным многоступенчатым процессом.
Из сульфидных руд медь добывается, главным образом, пирометаллургическим путем, а из окисленных - гидрометаллургическим. Пирометаллургическим способом в настоящее время получают 75 % всей добываемой меди. Этот способ основан на частичном окислении сернистых руд до оксидов меди, которые восстанавливаются избытком сульфида до металлической меди:
2Сu2О + Cu2S = 6Cu + SО2
Малая концентрация меди в рудах, естественно, затрудняет ее извлечение. Поэтому перед тем, как добытую руду пускают на переплавку, ее обогащают - искусственно увеличивают процентное содержание меди. Для того чтобы провести обогащение, руду измельчают до таких размеров, которые позволяют выделить зерна с процентом содержания меди, большим, чем в исходной руде. Затем такие "богатые" зерна отделяют от остальных, используя то обстоятельство, что зерна различного состава обладают различными свойствами. К числу таких свойств относятся: цвет, блеск, масса, электрическая и магнитная восприимчивость, смачиваемость.
Самым распространенным сейчас способом обогащения является флотация (рис. 13). В металлургии флотация применяется, в основном, для отделения сульфидных минералов от пустой породы, а также для разделения частиц руд различных металлов. Метод основан на различии адсорбционных
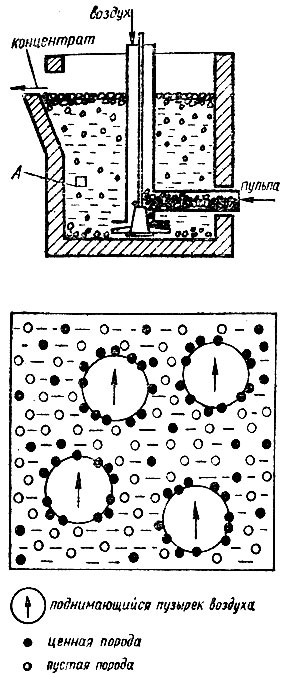
Рис. 13. Схема флотационного способа обогащения руд
свойств поверхности частиц сернистых металлов и пустой породы силикатного типа. Флотация медных руд осуществляется следующим образом. К суспензии тонкоизмельченной руды (0,05-0,5 мм) в воде, называемой пульпой, добавляют какое-нибудь полярное органическое вещество с длинной углеводородной цепью - собиратель. Собиратель обладает способностью полярными концами избирательно сорбироваться на поверхности частиц медной руды. При этом его углеводородный конец остается в водной фазе. Таким образом, в результате сорбции поверхность частицы оказывается покрытой и углеводородной "щетко", уменьшает ее смачиваемость. Частицы пустой породы, обладающие полярной поверхностью, смачиваются хорошо.
Далее пульпу при интенсивном перемешивании продувают воздухом, который образует пузырьки. Известно, что неполярные молекулы, помещенные в воду, в первую очередь стремятся расположиться на границе раздела вода - воздух. Точно так же ведут себя неполярные концы собирателя, покрывающие частицу руды. Для них самой доступной границей раздела вода - воздух является поверхность пузырьков. В результате частицы руды прилипают к пузырькам и вместе с ними всплывают на поверхность в виде пены. Пустая же порода - "хвосты" - остается в пульпе. Пену снимают, обезвоживают и получают концентрат, а хвосты сбрасывают в отвал. Полученный концентрат содержит уже до 55 % меди. Это верхний предел. В большинстве случаев после флотации содержание меди в концентрате находится в пределах 11-35 %. Наряду с медью там имеются сера, железо, цинк, оксиды кремния, алюминия, кальция, а также в небольших количествах благородные металлы - золото, серебро, платина. Сульфидные руды часто содержат много пирита, поэтому и в концентрате существенная часть железа и серы приходится на его долю.
Чтобы получить чистую медь, от примесей необходимо избавиться. Это удается сделать не сразу, а в несколько этапов. Первым из них является обжиг концентрата. Концентрат подвергают обжигу для того, чтобы снизить в нем содержание серы. Кроме того, в результате обжига получается оксид серы (IV) в таких концентрациях, что его можно в дальнейшем использовать для производства серной кислоты. Комплексное использование сырья приводит к уменьшению загрязнения атмосферы отходами производства.
Обжиг ведут при температуре 600-700 °С в многоподовых печах. Печь загружают концентратом в смеси с флюсами (кварц, известняк), необходимыми для последующего этапа - выплавки штейна. Во время обжига наряду с окислением серы происходит целый ряд процессов: разложение сложных сульфидов, прямое окисление минерала, образование ферритов примесных металлов и др. Как уже говорилось, в концентрате, подвергающемуся обжигу, содержится значительное количество пирита (40-50 %). Его горение при обжиге, в зависимости от доступа воздуха, описывается уравнениями:
3FeS2 + 8О2 = Fe3О4 + 6SО2 + 2349 кДж
4FeS2+11О2 = 2Fe2О3 + 8SО2 + 3282 кДж
Эти реакции сопровождаются выделением значительного количества тепла. В результате обжиг проходит самопроизвольно, без затрат топлива. Достаточно только в начале процесса временными топками нагреть шихту до температуры воспламенения сульфидов. В процессе обжига из руды удаляется не вся сера. После обжига в шихте остаются сульфиды меди, железа, устойчивые оксиды - Cu2О, Fe2О3, Fe3О4, ZnO, PbO, a также флюсы.
Следующий этап производства меди - выплавка из обожженного концентрата штейна и отделение его от шлака.
Штейн - это сплавы Cu2S с FeS с примесями некоторых сульфидов (Zn, Pb, Ni) и оксидов (Fe, Si, Al, Ca)
Содержание меди в штейне колеблется от 10 до 79,9% (чистый Cu2S). Шлаки - сплавы силикатов различных металлов. В металлургии меди это, в основном, силикаты железа. Плавка на штейн производится в отражательных печах (рис. 14), куда помещается прошедшая обжиг шихта. Топливом служит угольная пыль, мазут или природный газ. Температура зависит от расстояния, от места ввода топлива и лежит в пределах 1200-1600 °С.
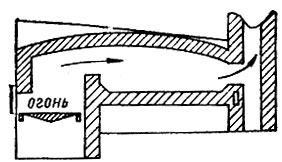
Рис. 14. Схема отражательной печи
Основным химическим процессом, который происходит на этом этапе, является переход железа в шлак:
FeS + 3F3O4 + 5SiO2 = 5Fe2SiO4 + SO2
Часть сульфида железа расходуется на обменную реакцию с оксидом меди:
Cu2O + FeS=Cu2S + FeO
FeO в присутствии кварца также связывается в силикат. Жидкие сплавы сульфидов и силикатов взаимно нерастворимы и различаются по плотности. Это обстоятельство используется для их разделения. Шлак располагается в верхнем слое, нижний - сплав сульфидов Cu2S·FeS - штейн. Их разделяют, выпуская по мере накопления через расположенные на разных уровнях специальные выпускные отверстия.
Само слово штейн происходит от немецкого слова - камень. Это связано с тем, что застывший сплав сульфидов меди и железа внешне очень похож на камень. Дальнейшая переработка штейна производится в продуваемом воздухом конверторе и целью своей имеет уже получение черновой меди. В конвертор заливают жидкий штейн (температура 1200 °С), туда же загружают измельченный (6-20 мм) кварц. В продувке воздуха через штейн можно выделить два этапа, отличающиеся химизмом происходящих в них процессов. На первом окисляется сульфид железа и образуется шлак:
2FeS+3О2 + SiО2 = Fe2SiО4+2SО2+966кДж
Эта реакция является основным источником тепла для конверторных процессов.
Оксид меди (I), который также получается на этом этапе:
Cu2S + О2=Cu2О + SО2
сразу же переводится обратно в сульфид по реакции:
Cu2О + FeS = Cu2S + FeO
Далее FeO, связываясь с кварцем, переходит в шлак. Накопившийся шлак сливают через горловину, наклоняя конвертор. После слива шлака в конвертор загружают новую порцию штейна и процедуру продувки повторяют до тех пор, пока в конверторе не накопится достаточного количества богатого медью расплава. Таким образом на этом этапе продувки происходит отделение железа от меди: железо удаляется со шлаком, медь остается в конверторе в виде расплава.
На втором этапе из расплава сульфида меди получают металлическую медь. После окисления железа и слива шлака окислению в конверторе подвергается Cu2S:
2Cu2S + 3О2 = 2Cu2О + 2SО2
Так как в отличие от первого этапа в реакционной среде отсутствует сульфид железа, оксид меди реагирует уже с избытком сульфида меди. В результате получается черновая медь:
Cu2S + 2Cu2О = 6Cu + SО2
Суммарно процесс, происходящий в конверторе на втором этапе продувки, можно описать следующей реакцией:
Cu2S + О2 = 2Cu + SО2 + 215 кДж
Черновая медь, слитки которой называют штыками (от немецкого Stück - штука), содержит 1 % примесей (Fe, S, О2, As, Ni, Zn и др.) и, кроме того, включает все примеси благородных металлов, которые Содержались в исходной руде и флюсах. Многие примеси ухудшают механические свойства металла, снижают его электрическую проводимость, делают менее пластичным. Для того чтобы избавиться от примесей, а также извлечь представляющие ценность благородные металлы, черновую медь подвергают очистке - рафинированию.
Рафинирование осуществляют двумя способами: огневым (вдувание воздуха при температуре 1150°С) и электролитическим. Первым способом удается избавиться от примесей путем перевода их в нерастворимые в меди оксиды:
4Cu + О2 = 2Cu2О
Me + Cu2О = MeO + 2Cu
Оксиды примесей всплывают на поверхность и шлакуются кварцевым флюсом. Образующийся оксид меди (I) восстанавливается продуктами сухой перегонки дерева. Для этого в печь, где проводится рафинирование, после удаления шлаков вводят сырое дерево (жерди, бревна). Выделяющиеся пары воды и углеводороды, перемешивая медь, способствуют удалению из нее газов и переводят в металлическую медь:
4Сu2О + СН4 = СО2 + 2Н2О + 8Сu
Однако огневой способ не позволяет извлечь из меди благородные металлы. Это удается сделать, подвергая медь электролитическому рафинированию. Смысл его заключается в анодном растворении очищаемой меди и высаживании чистой меди на катоде. Для этого из меди, прошедшей предварительную очистку огневым способом, отливают аноды. Они имеют особую форму, удобную для подвешивания (рис. 15). Их масса 250-320 кг. В качестве катодов используют листы чистой меди. Электроды помещают в электролитической ванне, представляющей собой обложенные свинцовыми пластинами бетонные чаны, наполненные соответствующим раствором и серной кислотой. Ванны имеют несколько метров в длину (от 3 до б м) и содержат до сотни электродов. Из соображений экономии ванны соединяют между собой в блоки (рис. 16). При пропускании через такую систему тока на катодах выделяется чистая медь:
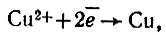
а аноды растворяются:
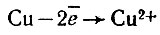
При этом примеси, содержащиеся в медном аноде, в зависимости от их свойств либо переходят в электролит (Zn, Fe, Sn, Ni), либо выпадают в осадок (Ag, Au, Pt), откуда их потом извлекают. Процесс растворения анодов продолжается около 20 суток. Катоды меняют через 6-8 суток. Их извлекают, сушат, переплавляют и разливают медь в слитки. Чистота получаемой электролитическим способом меди достигает 99,95-99,96 %.
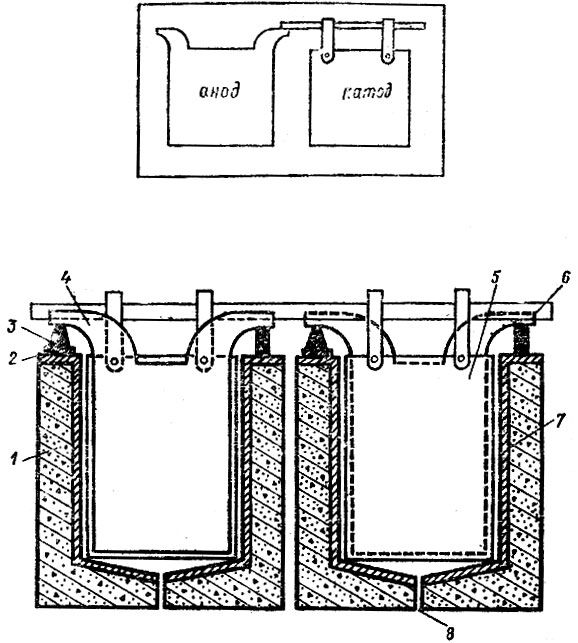
Рис. 15. Железобетонная ванна для электролитического получения меди: 1 - ванна, 2 - изоляция, 3 - медная шина, 4 - анод, 5 - катод, 6 - катодная штанга, 7 - ограничитель из винипласта, 8 - отверстие для выгрузки шлака
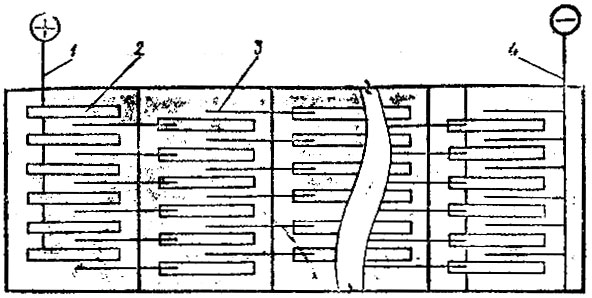
Рис. 16. Схема электрической цепи ванны: 1 - анодная шина, 2 - анод, 3 - катод, 4 - катодная шина
Как мы видим, процесс добычи меди из руд состоит из нескольких этапов. Цель каждого из них - отделение меди от сопутствующих примесей. Иногда в зависимости от качества руды, технических возможностей, экономических соображений из производства исключают флотацию или обжиг концентрата. Несколько отличаются на разных заводах условия производства. В самом общем виде схема выплавки меди пирометаллургическим способом изображена на рис. 17. Химические процессы этого способа можно описать суммарной реакцией:
2CuFeS2 + 5О2 + SiО2 = 2Cu + Fe2SiО4 + 4SО2
Характерной особенностью пирометаллургии является использование высоких температур.
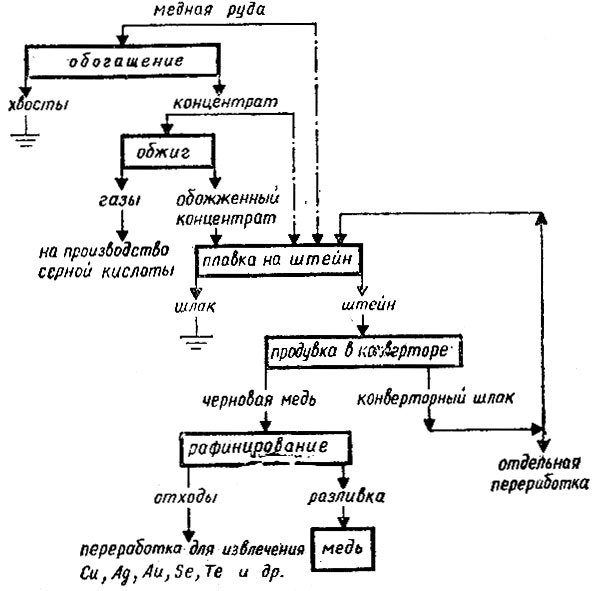
Рис. 17. Общая схема выплавки меди: сплошной линией плавка сырой руды, штрихпунктирной - плавка сырых концентратов
Гидрометаллургический способ, которым сейчас добывают около 25 % всей меди, не связан с использованием высоких температур. Этот способ применяют для извлечения меди главным образом из бедных окисленных руд, но он также может быть использован и для переработки сульфидных и смешанных руд. В ходе гидрометаллургической переработки меди ее труднорастворимые соединения переводятся в растворимые действием различных реагентов. Такими реагентами могут быть: H2SО4, NH4OH, NaCN, Fe2(SО4)3. Затем из раствора медь извлекают тем или иным способом. Например, обработка руды, содержащей медь в виде оксида СиО, разбавленной серной кислотой переводит медь в раствор в виде сульфата:
CuO + H2SО4 = CuSО4 + H2О
Извлечь медь из полученного раствора можно электролизом или вытеснением с помощью железа:
CuSО4 + Fe = Cu + FeSО4
Преимуществом гидрометаллургического метода является то, что получать металлы можно, не извлекая руду на поверхность. В настоящее время этот метод является весьма перспективным.
Естественно, что за многие тысячелетия, которые насчитывает металлургия меди и медных сплавов, менялись задачи, стоявшие перед металлургами, менялись условия труда, совершенствовалась технология, менялась область применения продуктов производства.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'