
3. Реакция полимеризации. Важнейшие мономеры, используемые для синтеза полимеров
В основе синтеза высокомолекулярных соединений лежат два типа химических реакций - реакции полимеризации и поликонденсации.
Реакция полимеризации, как нам уже известно из курса органической химии, - это соединение молекул вещества в более крупные молекулы.
Уравнения реакций полимеризации упрощенно могут записываться в том виде, как мы это делали при изучении этилена:
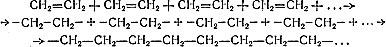
Или сокращенно:
nCH2=CH2→(-CH2-CH2-)n
Сокращенное уравнение показывает, что из п молекул низкомолекулярного вещества образуется одна молекула полимера. Число элементарных звеньев п, входящих в состав макромолекулы, называется степенью полимеризации. Степень полимеризации зависит от природы полимеризующегося вещества и от условий полимеризации.
Например, полимеризацией этилена при одних условиях можно получить вязкую жидкость со степенью полимеризации около 20; при других - мягкое воскообразное вещество, степень полимеризации которого будет около 100; изменяя условия далее, можно получить твердый продукт со степенью полимеризации 1000.
Во всех этих случаях степень полимеризации представляет некоторую среднюю величину, поскольку в каждом процессе полимеризации образуются молекулы различной величины и веса.
Пользуясь понятием степени полимеризации, можно в кратком виде записывать структурные формулы полимеров. Для этого достаточно обозначить строение элементарного звена и указать на его многократное повторение в молекуле. Такова именно вышеприведенная структурная формула полиэтилена (-СН2-СН2-)n. Структурная формула полихлорвинила будет 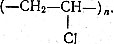
Какие же вещества могут вступать в реакцию полимеризации?
Сопоставляя известные нам реакции получения полиэтилена и полихлорвинила, мы замечаем, что строение молекул исходных веществ характеризуется наличием двойной связи между атомами углерода. Это не случайно. Для образования высокомолекулярного вещества необходимо, чтобы каждая молекула исходного вещества могла соединяться не менее чем с двумя другими молекулами. Если молекула будет соединяться только с одной молекулой, т. е. проявлять одну единицу валентности, то после соединения с другой такой же молекулой образовавшаяся молекула будет уже не способна к дальнейшему росту, высокомолекулярное вещество не получится.
Молекулы, которые могли бы реагировать с двумя другими молекулами, и имеют вещества с двойной связью. Действительно, если в такой молекуле разорвется одна из связей, то за счет образующихся двух единиц валентности такая молекула может соединиться с двумя другими молекулами. Вновь образовавшаяся молекула может соединиться с другими молекулами и т. д.
Низкомолекулярные вещества, вступающие в реакцию образования полимеров, называются мономерами.
Из мономеров с двойной связью в молекулах, кроме известных нам этилена СН2 = СН2 и хлористого винила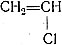 , большое применение для синтеза высокомолекулярных веществ находят следующие.
, большое применение для синтеза высокомолекулярных веществ находят следующие.
Пропилен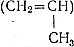 - газ, являющийся ближайшим гомологом этилена СН2 = СН2 и имеющий сходные с ним химические свойства.
- газ, являющийся ближайшим гомологом этилена СН2 = СН2 и имеющий сходные с ним химические свойства.
Тетрафторэтилен (CF2 = CF2) - газ, имеющий строение, аналогичное этилену, и отличающийся от него тем, что содержит вместо атомов водорода такое же число атомов фтора.
Стирол, или винилбензол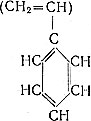 ,- бесцветная жидкость со слабым характерным запахом. Стирол является одновременно и ароматическим и непредельным углеводородом.
,- бесцветная жидкость со слабым характерным запахом. Стирол является одновременно и ароматическим и непредельным углеводородом.
Метилметакрилат, или метиловый эфир метакриловой кислоты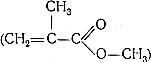 ,- бесцветная жидкость, обладающая приятным эфирным запахом. Это соединение можно рассматривать как производное акриловой кислоты
,- бесцветная жидкость, обладающая приятным эфирным запахом. Это соединение можно рассматривать как производное акриловой кислоты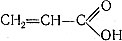 , являющейся начальным членом гомологического ряда непредельных одноосновных карбоновых кислот. Метилакриловая, или метакриловая, кислота
, являющейся начальным членом гомологического ряда непредельных одноосновных карбоновых кислот. Метилакриловая, или метакриловая, кислота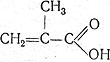 является гомологом акриловой кислоты и отличается от нее наличием в углеводородном радикале группы СН3 взамен атома водорода. Метакриловая кислота, как и другие кислоты, может давать со спиртами сложные эфиры. Одним из таких эфиров является метиловый эфир метакриловой кислоты.
является гомологом акриловой кислоты и отличается от нее наличием в углеводородном радикале группы СН3 взамен атома водорода. Метакриловая кислота, как и другие кислоты, может давать со спиртами сложные эфиры. Одним из таких эфиров является метиловый эфир метакриловой кислоты.
Акрилонитрил, или нитрил акриловой кислоты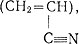 ,- бесцветная жидкость. Акрилонитрил может рассматриваться как производное акриловой кислоты (см. выше), в молекуле которой карбонильный кислород и гидроксильная группа заменены трехвалентным атомом азота.
,- бесцветная жидкость. Акрилонитрил может рассматриваться как производное акриловой кислоты (см. выше), в молекуле которой карбонильный кислород и гидроксильная группа заменены трехвалентным атомом азота.
Все эти вещества подобно этилену содержат в молекулах двойную связь между атомами углерода и сравнительно легко полимеризуются.
Этим же свойством обладают и вещества с двумя двойными связями в молекулах - диеновые углеводороды, например бутадиен (дивинил) СН2 = СН-СН = СН2 и его гомолог изопрен
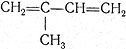
Диеновые соединения, как и выше рассмотренные соединения, широко используются в промышленности для синтеза полимеров.
Вопросы и упражнения
10. Составьте уравнение полимеризации пропилена подобно тому, как оно изображено выше для этилена. Выразите строение полипропилена структурной формулой.
11. Приведите структурную формулу бутадиенового каучука подобно тому, как она дана выше для полиэтилена и полихлорвипила (стр. 12).
12. Вычислите средний молекулярный вес различных видов полиэтилена по данным, приведенным на странице 12.
13. Стирол обесцвечивает бромную воду. Составьте уравнение этой реакции.
14. Как объяснить, почему начальный член гомологического ряда непредельных одноосновных кислот (акриловая кислота) не может содержать менее трех атомов углерода в молекуле?
15. В какие реакции, по вашему мнению, может вступать акриловая кислота? Приведите уравнения двух-трех реакций.
16. Составьте уравнение реакции образования метилметакрилата из метакриловой кислоты и метилового спирта.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'