
4. Механизм реакции полимеризации
До сих пор мы с помощью структурных формул и уравнений изображали лишь упрощенные схемы реакций полимеризации, но не изображали их механизма, т. е. тех процессов, которые протекают при этом в действительности.
Механизм многих реакций полимеризации заключается в том, что растущая молекула полимера от начала своего образования и до окончания роста представляет собой радикал, т. е. весьма реак-ционноспособную частицу, которая присоединяет к себе все новые и новые молекулы мономера. Радикалы, с которых начинается реакция, образуются под воздействием света, тепла или специальных веществ - инициаторов.
Рассмотрим процесс полимеризации непредельного соединения типа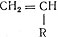 (где R - атом или группа атомов, замещающая в этилене атом водорода) в присутствии инициатора.
(где R - атом или группа атомов, замещающая в этилене атом водорода) в присутствии инициатора.
Инициаторы - это неустойчивые соединения, способные распадаться с образованием свободных радикалов. В качестве инициатора часто используют перекисные соединения*. Обозначим одновалентный радикал, образующийся при распаде перекисного соединения, через А-. Такой радикал, обладая свободной единицей валентности, соединяется с молекулой мономера, образуя более крупный радикал:
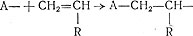
*(Строение перекисей характеризуется наличием в их молекулах "кислородных мостиков" -О-О-. Такой "мостик" неустойчив и легко разрывается. Часто для проведения реакций полимеризации применяют перекись водорода Н-О-О-Н или перекись бензоила , которые соответственно распадаются на радикалы НО- и С6Н5OO-.)
, которые соответственно распадаются на радикалы НО- и С6Н5OO-.)
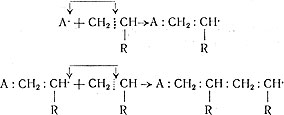
Этот радикал в свою очередь соединяется с новой молекулой мономера:
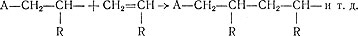
Процесс роста молекулы идет, однако, не бесконечно. Он прекращается, когда растущий радикал сталкивается с другим радикалом (возникшим при полимеризации или образовавшимся из перекиси). Тогда за счет взаимного насыщения свободных единиц валентности радикалы соединяются, и образующаяся молекула оказывается неспособной к дальнейшему росту:
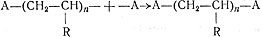
Части молекулы инициатора (его радикалы) входят в состав макромолекул полимера в качестве концевых групп; таким образом, инициатор в отличие от катализатора расходуется в процессе реакции.
Реакции, механизм которых показан выше, называют реакциями цепной полимеризации (по аналогии с тем, как образуются цепи путем последовательного наращивания звеньев). Механизм цепных реакций открыт и детально изучен академиком Н. Н. Семеновым, удостоенным за свои научные труды Нобелевской премии.
Зная электронное строение атомов, мы можем объяснить механизм цепной полимеризации следующим образом. Двойная связь в молекуле мономера, как известно, осуществляется двумя парами электронов, причем одна из связей менее прочная и сравнительно легко разрывается. Свободная единица валентности у радикала - это не что иное, как непарный электрон. Когда радикал сталкивается с молекулой, имеющей двойную связь, непарный электрон его действует на менее прочную электронную пару так, что она разрывается и электрон радикала образует пару с одним из электронов двойной связи (устанавливается прочная простая связь), а второй электрон бывшей двойной связи остается свободным, в результате чего вся частица снова становится радикалом:
Подобный процесс протекает и дальше, пока свободный электрон радикала не образует устойчивую пару с электроном другого радикала.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'