
Нейтрализация
Это реакция кислот с основаниями, приводящая к образованию солей:
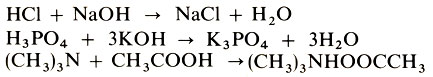
Реакцию нейтрализации обычно проводят титрованием - постепенным добавлением раствора одного из реагентов к раствору другого, например раствора соляной кислоты НСl к раствору гидроксида натрия NaOH. За прохождением реакции можно наблюдать по изменению окраски индикатора. В растворе NaOH фиолетовая лакмусовая бумажка синеет, а по мере того как малыми порциями подливается раствор соляной кислоты НСl, лакмус снова становится фиолетовым. Отсюда можно сделать вывод, что в результате данной реакции раствор стал нейтральным, т.е. в нем нет ни щелочи (иначе индикатор приобрел бы синий цвет), ни кислоты (в этом случае лакмус окрасился бы в красный цвет).
Реакции нейтрализации помогают определять в лаборатории свойства растворимых гидроксидов: если они вступают в реакцию нейтрализации со щелочами, их относят к кислотам; если реагируют с кислотами, то относят к основаниям.
Амфотерные соединения, обладающие свойствами и кислот, и оснований, например аминокислоты, способны к взаимной нейтрализации групп одной молекулы. При этом образуются так называемые внутренние соли:
H2NCH2COOH ↔ H3N+CH2COO-
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'