
8. Дисперсные системы. Основы коллоидной химии
Вещества, растворы которых имеют определенное осмотическое давление, проникают через полупроницаемые перепонки и выделяются из растворов в виде кристаллов. Такие вещества английский ученый Т. Грэм (1805 - 1869) назвал кристаллоидами, а их растворы - истинными, в отличие от растворов коллоидных. У коллоидных растворов осмотическое давление незначительно, или его нет совсем, и вещества, растворенные в этих растворах, не проникают через полупроницаемые перепонки и не кристаллизуются, т. е. после испарения растворителя остаются в виде бесформенной массы (принимая форму сосуда). Самым известным из таких веществ является клей (по-гречески - колла); поэтому они и были названы коллоидами.
Позднее было обнаружено, что некоторые нерастворимые в воде вещества, будучи очень тонко распыленными (усиленным дроблением, или же под влиянием особых причин при их выделении), образуют смеси с такими же свойствами, как и коллоидные растворы; кристаллоиды же при подборе подходящего растворителя также дают коллоидные растворы. Поэтому в настоящее время название коллоид (кристаллоид) применяется только к веществам, известным лишь в коллоидном (кристаллоидном) состоянии. В иных случаях мы говорим скорее о коллоидном состоянии вещества, а не о коллоидных веществах.
Часть химии, занимающаяся веществами в коллоидном состоянии, называется коллоидной химией. Ее основу мы лучше всего поймем на примере. Графит не растворяется в масле. Если же мы размешаем в масле порошок графита, то образуется смесь, суспензия, которая по истечении некоторого времени разделится, т. к. графит осядет на дно сосуда. Если графит, размельченный до пылевидного состояния (в так наз. коллоидной мельнице), рассеян в масле, он не даст осадка, т. е. получится коллоидный рacтвор графита в масле. Таким же образом можно жил кость (напр. масло) рассеять в другой жидкости (напр в воде) в эмульсию, которая хотя и разделится через некоторое время, однако при определенных условиях становится коллоидным раствором масла в воде.
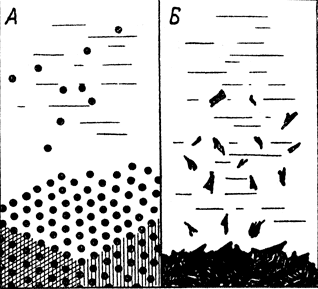
Рис. 19. Схема выделения: А. кристаллоида в правильных кристаллах, Б. коллоида в неправильных частичках
Общее название суспензии, эмульсии, коллоидных и истинных растворов - дисперсоиды (дисперсные системы); раздробленное вещество зовется дисперсной фазой системы, жидкость - дисперсионной средой. Известны также дисперсоиды твердые и газообразные, как это видно из разделения дисперсоидов по группам дисперсионной среды:
I. Дисперсоиды газообразные: дым, туман (твердые вещества или жидкости, рассеянные в газовой среде);
II. Дисперсоиды жидкие:
а) пирозоли (устойчивы при высокой температуре), напр. рассеянные металлы в расплавленных солях,
б) криозоли (устойчивы при низкой температуре), напр. лед в хлороформе,
в) лиозоли (устойчивы при обыкновенной температуре), напр. коллоидные растворы (суспенсоиды и эмульсоиды);
III. Дисперсоиды твердые: цветное стекло, опалы и некоторые сплавы металлов.
В химической практике чаще всего мы встречаемся с лиозолями, которые по степени дисперсности делятся на:

Коллоидные растворы составляют переход между суспензиями (эмульсиями) и истинными растворами. Всё зависит здесь от величины частичек дисперсной фазы, т. е. от степени дисперсности (рассеивания) дисперсной фазы. Микроскопическими измерениями было установлено, что величина рассеянных частиц колеблется в пределах от 10-4до 10-8 см, как это видно из схемы:
грубые лиозоли суспензии и эмульсии → тонкие лиозоли коллоидные растворы → истинные растворы (молекулярные и ионные)
менее 10-4 см (0,1 μ) → от 10-4 до 10-7 см; от 0,1μ до 1μμ → 10-7 до 10-8см; меньше 1μμ*
*(μ = 0,001 мм (10-4 см) = микрон, μμ = 0,001 ц (10-7 см) = миллимикрон.)
Таким образом коллоидность не является свойством каких-либо определенных веществ, но общим свойством всех веществ, ибо каждое вещество (твердое, жидкое или газообразное) можно привести в коллоидное состояние в подходящей среде и при достаточном размельчении. Так напр. поваренная соль NaCl - кристаллоид (образует с водой истинный раствор). Коллоидный раствор NaCl можно получить при достаточном рассеянии NaCl в бензоле.
Для получения коллоидных растворов применяются физические методы (измельчение в коллоидных мельницах или резкое встряхивание) и химические методы (получение коллоидных растворов металлов из их солей под действием соединений - восстановителей). Коллоидные растворы золота, серебра или платины можно получить методом Бредига: между двумя электродами соответствующего металла под водой образуется электрическая дуга.
Дисперсные системы неустойчивы. Уменьшением степени дисперсности, т. е. увеличением размера частичек, наступающим напр. в результате повышения температуры или прибавления какой-либо соли, коллоидное состояние нарушается и взвешенные частицы оседают. Мы говорим тогда, что коллоидный раствор коагулирует, т. е. образуется суспензия или гель (желатиновое вещество, связывающее большую часть дисперсной среды, т. е. растворителя).
Мы различаем:
а) Коллоиды обратимые (реверсивные, лиофильные). При коагуляции они выделяют гель, который снова можно обратить в коллоидный раствор, прибавив растворителя. Обратимые коллоиды устойчивы, мало чувствительны к прибавкам солей, в ультрамикроскоп не видно броуновского движения, а также не появляется катафорез. Самые распространенные лиофильные коллоиды - это белки (желатин), крахмал и т. д.
б) Коллоиды необратимые (иреверсивные, лиофобные). При коагуляции они выделяют осадок, который нельзя снова обратить в коллоидный раствор прибавлением к нему растворителя. Они весьма не устойчивы и коагулируют от прибавления даже незначительного количества соли, причем превращаются в суспензию. У них отчетливо проявляется катафорез и броуновское движение; их взвешенные частички можно наблюдать в ультрамикроскоп. К ним относятся коллоидные растворы металлов, гидрат окиси железа, трехсернистый мышьяк и т. д.
Так как коллоидные растворы содержат частички очень незначительных размеров, их общая поверхность очень велика. Если мы примем взвешенные частицы вещества коллоидного раствора за кубики с длиной ребра в 1 см, то получим их общие поверхности, указанные в табл. 10.
Таблица 10
| Длина ребра куба | Число кубиков в см3 | Общая поверхность |
| 1 см | 1 | 6 см2 |
| I мм | 103 | 60 см2 |
| 0,1 мм | 106 | 600 см2 |
| 0,01 мм | 109 | 6 000 см2 |
| 1 μ | 1012 | 6 м2 |
| 0,1 μ | 1015 | 60 м2 |
| 0,01 μ | 1018 | 600 м2 |
| 1 μμ | 1021 | 6 000 м2 |
| 0,1 μμ | 1024 | 60 000 м2 |
| 0,01 μμ | 1027 | 600 000 м2 |
| 0,001 μμ | 1030 | 6 км2 |
Огромная поверхность частичек в небольшом количестве коллоидного раствора является причиной того, что распыленные коллоидные частицы становятся сильными катализаторами. С огромной поверхностью дисперсной фазы связана также так наз. адсорбция, т. е. концентрация веществ на поверхности тонко распыленной материи. Напр. активированный уголь задерживает на своей поверхности красители. В некоторых случаях адсорбционная способность дисперсной фазы так велика, что образуются так наз. адсорбционные комплексы. Примером таких комплексов является, напр., иодный крахмал, или адсорбционные комплексы, образуемые из таннида и кожи животных при дублении, или, наконец, взаимодействие волокна и красителя при окраске текстиля.
Характерные коллоидные признаки проявляются напр. при затвердевании цемента, при обработке пород в керамической промышленности, в молочном производстве, при приготовлении теста, при вулканизации каучука, при производстве клея и желатина, смол и экстрактов и т. д. Наибольшее значение имеют так наз. биоколлоиды, которые являются основой крови, растительного сока, животных тканей и т. д., так что все жизненные процессы проходят в самых разнообразных дисперсных системах.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'