
Органические производные фтора
Современная техника с ее необычными условиями эксплуатации двигателей нового типа предъявляет высокие требования к конструкционным материалам. Здесь особое место занимают прочность, невоспламеняемость, теплоустойчивость, стойкость к коррозии. Часто для создания той или иной конструкции не находится подходящего материала, и его приходится создавать. Химическая природа фторуглеродов открывает широкие возможности для получения таких веществ. Фторорганические соединения обладают рядом свойств, делающих этих вещества незаменимыми конструкционными материалами. К их числу относятся невоспламеняемые гидравлические жидкости, пластические массы и покрытия, стойкие к высокой температуре и агрессивным средам, пламягасящие вещества и материалы для электронного оборудования.
Высшие фторуглероды с успехом применяются в авиации и ракетной технике как сальниковые и прокладочные материалы. Вещества из класса фторуглеродов начинают широко использовать как реакционные среды. Для окисления энергичными окислителями часто бывает трудно подобрать достаточно стойкий растворитель, не реагирующий с окислителем. В этом отношении фторуглероды, обладающие исключительной стабильностью, незаменимы.
До последнего времени исследования соединений фтора охватывали преимущественно область неорганических веществ. Число работ по изучению органических соединений фтора измерялось буквально единицами. Только сравнительно недавно были созданы методы и процессы, при помощи которых появилась возможность получать органические соединения фтора и начать их детальное изучение.
Химические и физические свойства фторуглеродов оказались поистине замечательными. Например, фторуглероды имеют очень низкие температуры кипения и гораздо более летучи, чем углероды одинакового с ними молекулярного веса. Фторуглероды кипят при температуре более высокой, чем температура кипения инертных газов того же молекулярного веса. Этот факт свидетельствует о слабом действии межмолекулярных сил во фторуглеродах. На рисунке 1 изображены кривые зависимости температуры кипения от молекулярного веса (по Саймонсу и Блоку) для инертных газов, углеводородов и фторуглеродов. Кривая фторуглеродов лежит вблизи кривой инертных газов.
Обычно с увеличением молекулярного веса наблюдается рост температуры кипения веществ. При переходе от углеводородов и частично фторированных углеводородов к сполна фторированным углеводородам это правило не соблюдается.
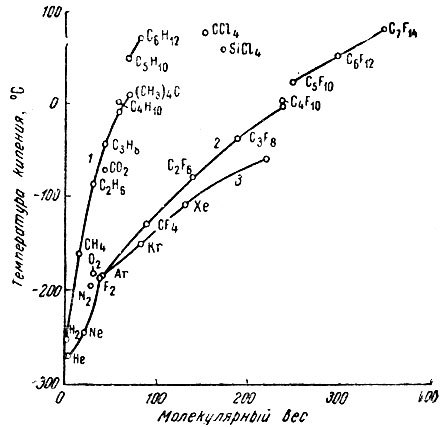
Рис. 1. Кривые зависимости температуры кипения вещества от его молекулярного веса: 1 - углеводороды; 2 - фторуглероды; 3 - инертные газы
Только первые четыре представителя фторуглеродов ряда CnF2n+2кипят при несколько более высокой температуре, чем соответствующие углеводороды, для всех остальных представителей этого ряда наблюдается обратное явление. Следует отметить, что замещение фтора на хлор во фторуглеродах приводит к повышению температуры кипения.
Снижение температуры кипения фторированных углеводородов представляет собой удивительное явление, так как их молекулярный вес намного превосходит молекулярный вес аналогичных парафинов. Так, нормальный гептан (мол, вес 100) кипит при +98°С, перфторгептан (мол. вес 338) - при +82°С, перфтороктан (мол. вес 438) - при +104°С.
Аналогичное изменение температуры кипения наблюдается при полном замещении атомов водорода на фтор в ряде однофункциональных производных простейших углеводородов. Так, введение атома фтора в нитрилы, спирты, кетоны, кислоты и многие другие производные парафинов вначале повышает температуру кипения, однако дальнейшее введение фтора вызывает резкое снижение температуры кипения, которая в случае исчерпывающего замещения падает иногда на 100°С и более. Это находит свое объяснение в том, что взаимодействие между молекулами ослабляется и устраняются условия для образования водородных связей. Снижение температуры кипения при исчерпывающей замене атомов водорода на фтор показано в табл. 2.
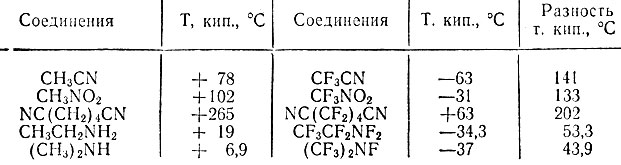
Таблица 2
Плотность фторуглеродов, естественно, выше плотности аналогичных углеводородов. Жидкие фторуглероды с высокой плотностью используются в гироскопических приборах, манометрах.
Одна из интересных особенностей жидких фторуглеродов - необычайно малое поверхностное натяжение, значительно меньшее, чем у соответствующих углеводородов. Низкое поверхностное натяжение фторуглеродов и их производных дает возможность применять эти соединения в качестве поверхностно-активных веществ. Например, разбавленные растворы перфокарбоновых кислот с длинной цепью снижают поверхностное натяжение воды сильнее, чем любые другие вещества, Введение фторуглеродных кислот или их солей (в количестве менее 1%) уменьшает поверхностное натяжение воды примерно с 72 до 20 дин/см. Перфторкарбоновые и моногидроперфторкарбо,новые кислоты используют в качестве эмульгирующих и диспергирующих агентов, в частности для получения водных дисперсий политетрафторэтилена.
Очень компактная и плотная структура атома фтора объясняет малое значение его атомной поляризуемости и атомной рефракции. Значение последней для фтора гораздо ближе, чем для любого другого галоида, к атомной рефракции водорода:
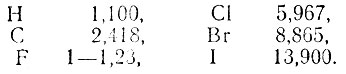
Атомная рефракция фтора во фторорганических веществах не постоянна, она зависит от числа атомов фтора в молекуле соединения и достигает наибольшего значения (1,23) в полностью фторированных углеводородах.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'