
Конформаций молекул в твердом состоянии веществ
При затвердевании вещества молекулярного состава, когда жидкость (расплав) или газ охлаждается до каких-то низких температур, оно может переходить в стеклообразное (аморфное); или кристаллическое состояние. Первое характеризуется неупорядоченным, а второе упорядоченным относительным расположением молекул. Как и в случае атомных или ионных кристаллов, молекулы в кристаллическом веществе находятся в каких-то строго определенных местах ячеек кристаллической решетки, но, кроме того, они определенным образом ориентированы в пространстве. Молекулярные кристаллы строятся по принципу наиболее плотной упаковки частиц, т. е. молекулы укладываются в твердой фазе так, чтобы незаполненное ими пространство оставалось минимальным. Отсюда ясно, что структура кристалла; число частиц в повторяющейся ячейке кристаллической решетки, ее размеры и симметрия, а также свойства твердого вещества тесным образом связаны с пространственной формой, т. е. со строением самих молекул.
Если иметь в виду внутреннее вращение молекул в газовой и жидкой фазах и возможность появления в результате этого различных конформаций, т. е. различных пространственных форм молекул какого-либо соединения, то, очевидно, возникает вопрос, все ли эти конформаций или какие из них остаются в твердой фазе вещества. Интересно также, зависит ли, и если да, то как, характер твердой фазы вещества от реализующихся в ней конформаций молекул.
Анализ экспериментальных данных, полученных при изучении указанных вопросов на целом ряде органических соединений, уже позволил вскрыть некоторые закономерности и сделать определенные выводы. Оказалось, что кристаллизующиеся органические вещества по их поведению при затвердевании, связанному с конформационным составом, можно разделить на три группы. К одной группе, назовем ее группой А, относятся соединения, которые в газообразном и жидком состояниях представляют равновесные смеси нескольких конформаций молекул (обладают поворотной изомерией), а в кристаллическом состоянии у них остается только какая-то одна из этих конформаций, все же остальные оказываются неустойчивыми и при кристаллизации переходят в нее. Оче-видно, что единственная устойчивая в кристаллическом состоянии таких веществ конформаций молекул имеет какие-то преимущества формы перед другими конформациями в смысле возможности образования наиболее упорядоченной, плотной упаковки молекул в кристалле. У соединений этой группы" кристаллическую решетку образует обычно конформаций наиболее "удобной", правильной формы, имеющая какие-либо элементы симметрии и часто более симметричная, чем другие возможные конформаций молекул данного соединения. Так, например, у 1, 2-дизамещенных этана, первичных галоидных алкилов, нормальных предельных углеводородов и т. п. в кристаллическом состоянии единственно устойчивыми оказываются транс-поворотные изомеры, представляющие максимально вытянутую зигзагообразную цепочку тяжелых ядер молекулы, хотя в жидком и газообразном состояниях не у всех этих соединений именно такая форма молекул находится в преобладающей концентрации. Мы уже говорили выше, что у галоидных пропилов в парах и жидком состоянии меньшей энергией обладает гош-конформация молекул; в случае нормальных предельных углеводородов и их производных (при замещении у первого атома углерода или вообще у крайних атомов), чем длиннее цепь молекулы, тем меньше в парах и жидкостях концентрация вытянутой зигзагообразной формы молекул, так как в результате внутреннего вращения меньше вероятность одновременного осуществления транс-конформации всех звеньев. В кристалле внутреннего вращения таких молекул нет, и решающую роль играют так называемые энтропийные факторы, связанные с требованием наибольшей упорядоченности расположения молекул и плотной их упаковки; транс-поворотные изомеры, имеющие более высокую симметрию, чем гош-изомеры, и более удобную для упаковки в кристалле вытянутую, форму (см. рис. 7), лучше удовлетворяют этим требованиям. Таким образом, устойчивые кристаллы соединений группы А представляют сугубо индивидуальные вещества в самом строгом физическом смысле слова, так как все молекулы такого кристаллического вещества имеют одну и ту же равновесную ядерную конфигурацию. Убедительное доказательство этого отличия кристаллического состояния соединений группы А от газообразного и жидкого состояний дают, например, колебательные спектры. На рис. 9 показаны (в сравнении) инфракрасные спектры поглощения жидких и кристаллических 1, 2-дихлорэтана и 1, 4-дибробутана. Бросается в глаза резкое упрощение спектров, т. е. уменьшение числа полос поглощения при переходе от жидкости к кристаллу, связанное с тем, что ИК-спектр жидкости получается в результате наложения колебательных частот не-скольких различных конформаций молекул указанных соединений, а спектр кристалла - это колебательный спектр только одной конформаций молекул.
Имея в виду найденную закономерность поведения соединений группы А при кристаллизации, можно с достаточной уверенностью относить к этой группе многие соединения без дополнительных экспериментальных исследований. Действительно, если, рассматривая возможные конформаций молекул какого-то соединения, мы можем выделить одну из них как имеющую заведомо более правильную форму или более высокую симметрию по сравнению с другими конформация-ми, то можно заранее предсказать, что соединение относится к группе А, и в кристаллическом состоянии вещества устойчивой будет только эта выделенная конформация молекул.
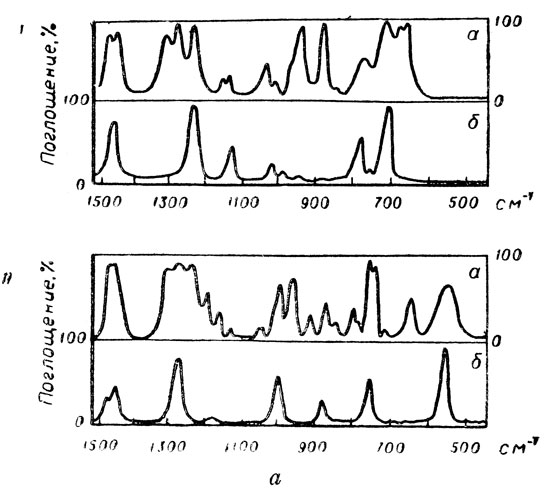
Рис.9. Инфакрасные спектры поглощения: а - жидких и б - кристаллических 1,2 - дихлорэтана (I) и 1,4 - дибромбутана (II)
К другой группе, В, мы относим соединения, у которых, хотя и можно ожидать по общим соображениям асимметрия узлов возможность поворотной изомерии, на деле во всех aгрегатных состояниях вещества оказывается устойчивой только одна конформация молекул. Исключительная устойчивость только одной конформаций целиком определяется в этом случае внутримолекулярными энергетическими факторами. В результате каких-то сильных взаимодействий несвязанных атомов или групп атомов в молекуле на кривой потенциальной энергии внутреннего вращения минимумы, которые могли бы соответствовать другим предполагаемым конформациям молекул этих соединений, сглаживаются, т. е. или пренебрежимо малы по сравнению с минимумом энергии основной (реально существующей) конформаций, или вообще отсутствуют. Одним из примеров является 2-метилбутан [(СН3)2СНСН2СН3], у которого конформация б практически неустойчива во всех фазах вещества. Изучено много, в том числе значительно более сложных соединений, относящихся к этой группе. Физические методы исследования всегда показывают для них наличие только одной равновесной ядерной конфигурации молекул во всех агрегатных состояниях. Эти вещества легко кристаллизуются, так как имеется единообразие формы всех молекул, которые могут поэтому определенным образом упаковываться в ячейки регулярной кристаллической решетки. Отличие этих соединений от соединений, группы А состоит в том, что по конформационному составу они одинаковы во всех агрегатных состояниях соответствующих веществ, а у соединений группы А конформационный состав в различных агрегатных состояниях вещества отличается. К группе В формально можно отнести также все соединения, у которых собственно поворотная изомерия молекул принципиально невозможна, т. е. соединения с одноузловыми молекулами (аммиак, метан и т. п.), этан, пропан и т. д.

Обнаружена, по-видимому, также третья группа соединений, С, правда более малочисленная по сравнению с первыми двумя группами, представители которой характеризуются тем, что у "их сохраняется сложный конформационный состав (несколько конформаций) во всех агрегатных состояниях вещества, включая и кристаллическое. Молекулы этих соединений, как правило, достаточно просты, имеют "глобульную" форму и обычно только одно звено, допускающее при внутреннем вращении появление поворотных изомеров, а. последние не отличаются друг от друга каким-либо преимуществом формы для образования регулярной наиболее плотной упаковки в кристалле и не имеют элементов симметрии. Приме-ром соединений этой группы являются 1,2-дигалогенопропаны (СН2Х-СНХ-СН3) и некоторые другие замещенные этаны, пропаны и бутаны и т. п. Возможно, что некоторые из простых соединений группы С образуют так называемые пластические кристаллы, в которых осуществляется вращение молекул в целом относительно определенных осей, задаваемых формой молекулы. В таких случаях возможно также и внутреннее вращение молекул в твердой фазе, так что иногда можно предполагать в отношении веществ группы С наличие некоторого конформационного равновесия в кристаллическом состоянии вещества. Так или иначе, физические методы исследования обнаруживают в кристаллическом состоянии веществ группы С так же, как в их жидком и газообразном состоянии, наличие нескольких равновесных ядерных конфигураций молекул.
Структура и свойства молекулярных кристаллов, как и сама возможность образования молекулярной кристаллической решетки, сильно зависят даже от сравнительно мелких деталей строения молекул, поэтому очень широко распространено явление полиморфизма кристаллических веществ молекулярного состава. Полиморфизмом называется возможность существования нескольких кристаллических модификаций данного вещества, различающихся структурой и свойствами кристаллов. Различают два вида полиморфизма: энантиотропизм, когда кристаллические модификации (полиморфные энантиотропные формы) устойчивы в своих определенных интервалах температур и между ними возможен обратимый фазовый переход, и монотропизм, когда одна из полиморфных форм является неустойчивой при всех температурах ниже температуры плавления вещества, но может быть получена, например, при переохлаждении жидкости или газа и существует продолжительное время, однако переход ее в устойчивую кристаллическую модификацию происходит необратимо (монотропный переход).
Возникновение полиморфных форм молекулярных кристаллов может быть связано с различным расположением или ориентацией молекул данного вещества в кристалле, а также, очевидно, и с тем, какими конформациями молекул образована кристаллическая решетка. Явление полиморфизма, связанное с поворотной изомерией молекул, строго говоря, представляет псевдополиморфизм, так как различные конформаций можно рассматривать как молекулы различного строения, а по определению полиморфные формы образуются одними и теми же молекулами. Однако мы сохраняем кристаллохимическую терминологию, тем более что вещества, представляющие в жидком и газообразном состояниях равновесные смеси нескольких конформаций, мы также считаем химически чистыми.
Полиморфизм, связанный с конформационным составом кристаллов, можно ожидать, по-видимому, в случае соединений, не относящихся к описанной выше группе В, представители которой во всех фазах вещества имеют лишь одну кон-формацию молекул. Рассматривая выше соединения группы А, мы не уточняли, что речь шла об устойчивых кристаллических модификациях. Для соединений этой группы можно также получить, например, замораживанием паров при достаточно низких температурах или в случае более сложных соединений, проводя быструю кристаллизацию из пересыщенных растворов, метастабильную (неустойчивую) модификацию, которая образуется различными конформациями молекул, существующими в других агрегатных состояниях вещества. При повышении температуры можно наблюдать монотропный переход этой метастабильной модификации в устойчивую, которая Получается и при медленной равновесной кристаллизации жидкого вещества и образована, как указывалось, только одной конформацией молекул, имеющей преимущество формы перед другими конформациями для наиболее плотной упаковки в кристалле. Таким образом, при указанном монотропном переходе в твердом состоянии осуществляется превращение всех неустойчивых поворотно-изомерных форм в устойчивую, т. е. поворот узлов в молекуле в наиболее выгодное для кристалла положение - с преодолением потенциального барьера внутреннего вращения в кристаллическом состоянии вещества. Такой переход фиксируется, например, по скачкообразному изменению колебательных спектров твердого вещества и рядом других физико-химических методов. В случае рассмотренных выше примеров 1,2-дихлорэтана и 1,4-дибромбутана ИК-спектры поглощения при монотропном фазовом переходе скачкообразно меняются от вида, подобного показанному на рис, 9, а, к виду, изображенному на рис. 9, б.
В научной литературе сообщалось также о возможности получения двух устойчивых полиморфных кристаллических модификаций, например такого вещества, как 1,1,2,2-тетрабромэтан (СНВr2-СНВr2), одна из которых образуется только транс-конформацией молекул:
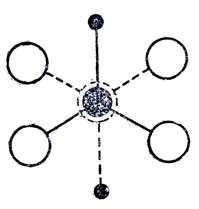
а другая -только гош-конформацией молекул:
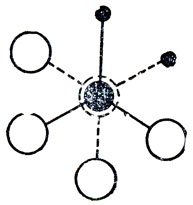
Этот случай полиморфизма пока является весьма исключительным и еще недостаточно изучен.
В С-группе соединений можно предполагать возможность существования различных полиморфных форм кристаллов и фазовых переходов в твердом состоянии, связанных с появлением или исчезновением степеней свободы вращения молекул в целом и внутреннего вращения, а может быть, и со сдвигом конформационного равновесия. Отличие этих соединений от соединений группы А состоит в том, что среди устойчивых конформаций молекул каждого из них ни одна резко не выделяется преимуществом более высокой симметрии или более правильной, удобной формы - для образования плотной упаковки в кристалле.
Наконец, еще одну большую группу соединений, D, образуют вещества, которые при понижении температуры и затвердевании дают только стеклообразное (аморфное) состояние. Молекулы этих соединений сложны, все их возможные конформации не обладают никакой симметрией, и ни одна из "них не отличается от других какой-либо более правильной формой, дававшей бы ей преимущество перед другими для образования регулярной плотной упаковки, т. е. молекулярной кристаллической решетки. Этим выявляется их резкое отличие от соединений группы А. С другой стороны, в отличие от соединений группы С, молекулы рассматриваемой группы - (громоздки и никак не могут быть причислены к "глобульным" молекулам, имеющим форму, близкую к сфероидальной или эллипсоидальной, и способным образовывать пластические или какие бы то ни было кристаллы. От соединений группы В эти соединения отличаются тем, что во всех агрегатных состояниях соответствующих веществ реально существуют несколько различных конформаций молекул, несильно отличающиеся по энергиям (устойчивости) и находящиеся в жидком и газообразном состояниях вещества в подвижном равновесии. Все эти характерные особенности соединений группы D хорошо объясняют большую трудность или даже невозможность кристаллизации таких веществ обычными способами и при обычных условиях. Примерами соединений этой группы являются некоторые типы разветвленных предельных углеводородов, а именно: 3-замещенные и 2, 3-дизамещенные алканы, которые пока еще ни разу не были получены в кристаллическом состоянии, и другие соединения.
Мы видим, таким образом, что характер твердой фазы молекулярных веществ, а следовательно, и свойства таких твердых веществ тесным образом связаны с особенностями пространственного строения молекул, в частности с их конформациями. Анализ рассмотренных здесь закономерностей в подведении веществ при затвердевании в зависимости от их конформационного состава позволяет предсказывать некоторые свойства твердых веществ известного молекулярного строения.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'