
Ядерные уровни и магические числа
Ядра всех атомов состоят из протонов и нейтронов. Правомерен вопрос о распределении нуклонов в ядре: является ли оно хаотичным или подчинено определенным закономерностям?
В конце 40-х годов сформировалась оболочечная теория строения ядра, утверждающая, что нуклоны в ядре закономерно распределяются по ядерным уровням и подуровням.
Подобно электрону в оболочке атома каждый нуклон - протон и нейтрон характеризуется четырьмя квантовыми числами, и, в соответствии с принципом Паули, эти характеристики не могут полностью совпадать у любых двух нуклонов: каждый нуклон имеет свой набор квантовых чисел. Квантовое число n определяет величину энергии ядерного уровня, а квантовое число l, отвечающее вращательному, или орбитальному моменту нуклона, позволяет внести некоторую поправку в величину энергии нуклона.
В отличие от электронных подуровней, в которых максимальное число электронов Хl определяется по формуле Xl = 2 (2l + 1), где l = 0, 1, 2, 3, 4, 5, 6, и которые обозначаются спектроскопическими индексами s, р, d, f, g, h, i, в ядерных уровнях максимальное число нуклонов Хнукл может быть определено по формуле:
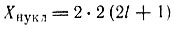
где дополнительный коэффициент 2 указывает на два "сорта" ядерных нуклонов. Ниже приведены числа нуклонов (нейтронов и протонов) в ядерных уровнях:

Так же как и электроны, протоны и нейтроны обладают спином (s), имеющим значение + 1/2 и - 1/2. В отличие от электронов для ядерных частиц характерно сильное спин-орбитальное магнитное взаимодействие, и полный момент количества движения j (третье квантовое число нуклона) определится суммой орбитального и спинового моментов j = l + s. Так как орбитальный и спиновый моменты являются векторами, то в зависимости от их направления (рис. 19) они складываются j = l + 1/2 или вычитаются j = l - 1/2. В поле ядра происходит расщепление нуклонных уровней на подуровни с различным числом нуклонов, а именно: 2l + 2 (при j = l + 1/2) и 2l (при j = l - 1/2). Например, в f-уровне (l = 3) 14 протонов или нейтронов распределяются по подуровням так: 8 (при j = 3 + 1/2 = 7/2) и 6 (при j = 3 - 1/2 = 5/2). Энергия связи нуклонов на подуровнях неодинакова: при данном значении l она больше на том подуровне, для которого значение j наибольшее. Схема расщепления ядерных уровней на подуровни приведена в табл. 46.
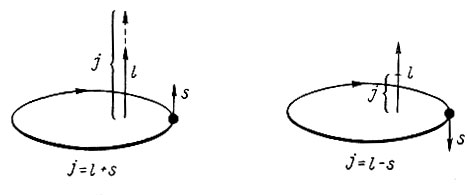
Рис. 19. Значение суммарного момента ядер в зависимости от направления орбитального и спинового момента
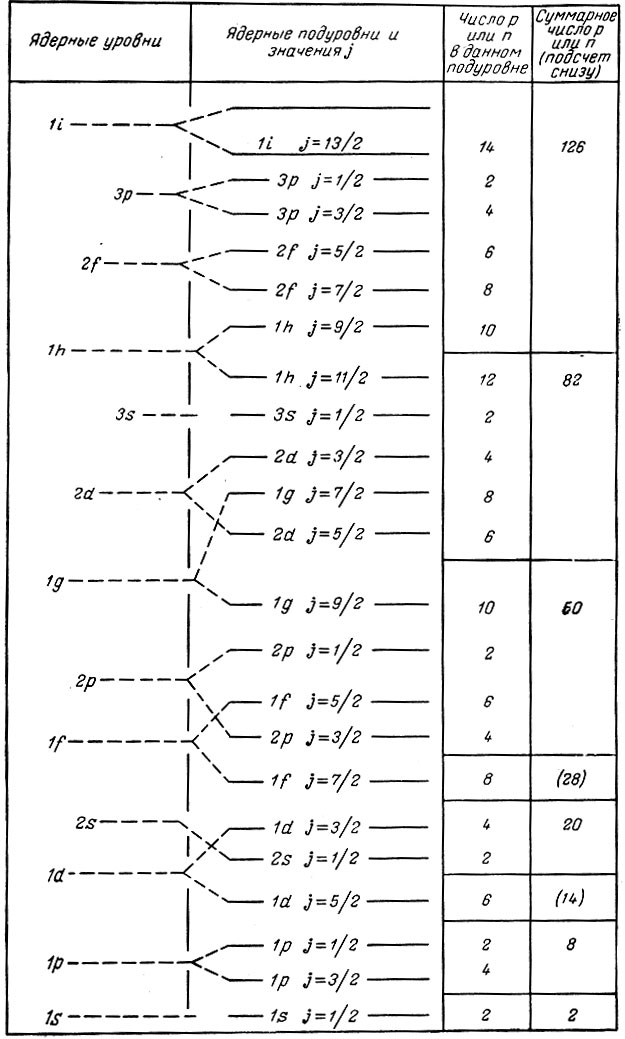
Таблица 46. Схема ядерных уровней и подуровней
Из таблицы видно, что все ядерные уровни, кроме s-уровней (l = 0), расщепляются на два подуровня. Ядерные уровни, содержащие 2, 8, (14), 20, (28), 50, 82 и 126 нуклонов, являются полностью укомплектованными (насыщенными). Эти числа называются магическими (числа 14 и 28 некоторые ученые относят к субмагическим, в табл. 46 они заключены в скобки). Ядра, отвечающие магическим числам, называются магическими ядрами; они заметно отличаются свойствами от соседних ядер, содержащих большее или меньшее число нуклонов.
Магические ядра можно разделить на три типа: 1) магические по числу протонов и нейтронов, или дважды магические; 2) магические по числу протонов; 3) магические по числу нейтронов. Например, ядро 4020Са относится к первому типу (20p, 20n), ядро 11850Sn - ко второму типу (50р, 68n) и ядро 13856Ba - к третьему типу (56p, 82n). Как будет видно из дальнейшего, магические ядра на кривых периодически изменяющихся свойств ядер занимают особое положение.
Из анализа устойчивости ядер, проведенного в 1965 году, следует, что ядра с числом протонов 114 и 126 и числом нейтронов 184, несмотря на их радиоактивность, должны быть относительно прочны. Эти числа следует также отнести к магическим.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'