
§ 30. Производство синтетического аммиака
Опираясь на достижения теоретической химии, ученые в первом десятилетии текущего века приступили к глубоким физико-химическим исследованиям и поискам инженерного решения процесса "связывания" молекулярного азота. Исследовались главным образом два пути решения проблемы: синтез окиси азота и синтез аммиака.
Окисление азота происходит при высокой температуре, причем образуется очень мало окиси азота. Поэтому расход энергии (на нагревание воздуха) чрезвычайно велик. Получение из окиси азота азотной кислоты и нитратов затрудняется низкой концентрацией окиси азота в газовой смеси. Промышленные установки для окисления азота, сооруженные в начале текущего века, уже в конце 20-х годов были остановлены. Однако поиск более совершенных способов синтеза окиси азота продолжается.
Экономически целесообразным оказалось связывать азот не с кислородом, а с водородом. В настоящее время синтезируются десятки миллионов тонн аммиака в год. Аммиак стал сырьем для получения всех других азотсодержащих химических продуктов.
При разработке промышленного способа синтеза аммиака химики и инженеры встретились с задачами, которые до тех пор не вставали ни в химической, ни в какой-либо другой отрасли промышленности.
Мы знаем, что реакция азота с водородом протекает только при довольно высоких температурах в присутствии катализаторов и что даже при высоких давлениях образуется немного аммиака. При высоких давлениях и температурах водород диффундирует через обычные стали, азот и аммиак реагируют с ними.
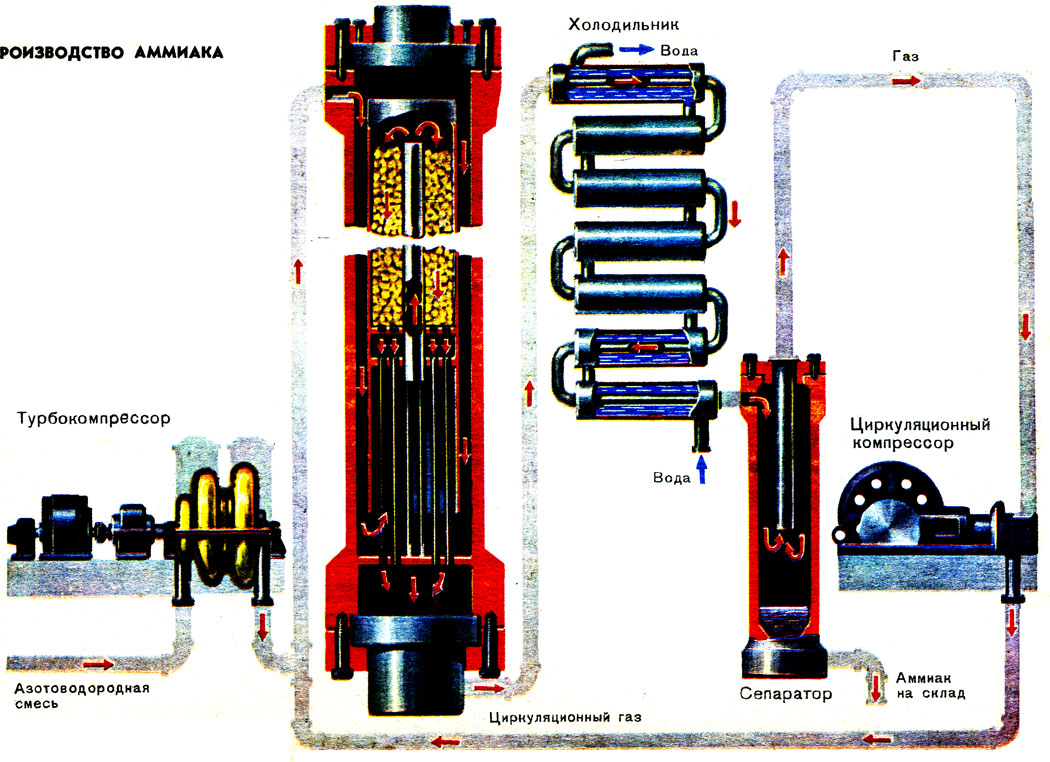
Производство аммиака
Катализатор отравляется сернистыми соединениями, кислородом и кислородными соединениями - водяным паром, окисью углерода.
Как же удалось преодолеть все эти трудности? Каковы оптимальные условия процесса?
В промышленности используют повсеместно дешевый железный катализатор. Для повышения его активности и удлинения срока "жизни" в него вводят добавки, например, окись алюминия и окись калия.
Рассмотрим вопрос о выборе оптимального давления. Казалось бы, следует вести реакцию под возможно более высоким давлением для смещения равновесия в сторону образования аммиака. Но и при высоких давлениях полностью сместить равновесие невозможно. А ведь чем выше давление, тем сложнее устройство машин и аппаратов, тем больше энергии затрачивается на сжатие газовой смеси.
Нужно было искать другой выход. Создатели промышленного процесса синтеза аммиака решили проблему возможно более полного использования азотоводородной смеси иным путем. Из газовой смеси, образующейся в реакционном аппарате - колонне синтеза - и содержащей всего только 10-20% аммиака, его отделяют, охлаждая газ. Непрореагировавшие же азот и водород дополнительно сжимают и направляют обратно в колонну синтеза (рис. I). Применяя циркуляцию азотоводородной смеси, можно ограничиться сравнительно невысокими давлениями. Так, сейчас синтез аммиака проводят на многих заводах под давлением около 300 ат. На установках с новейшим оборудованием применяют и более низкое давление - 150 ат.
Самой трудной инженерной задачей было конструирование колонны синтеза аммиака хотя бы уже по одному тому, что неизвестны были материалы, которые могли в течение длительного времени сохранять прочность при высоких температурах и давлениях. Эту трудность удалось преодолеть. В современных колоннах стенки корпуса, "а которые изнутри давит газ, нагреваются незначительно. Как же этого добились?
Катализатор засыпают в цилиндрическую коробку, диаметр которой несколько меньше, чем внутренний диаметр корпуса колонны. Таким образом, между катализаторной коробкой и ?корпусом образуется щель. Холодная азотоводородная смесь поступает в колонну через эту щель. Поток газа и предохраняет корпус колонны от чрезмерного нагревания.
Мы знаем, что реакция начинается при температуре не ниже 400°С. Следовательно, азотоводородную смесь нужно предварительно подогреть. За счет какого источника теплоты и в каком устройстве?
Ответ на этот вопрос вы можете дать сами, вспомнив, как решается эта задача при производстве серной кислоты. Нужно поместить в колонну синтеза аммиака трубчатый теплообменник, в котором азотоводородная смесь подогревается за счет покидающей катализатор горячей смеси. Теплоты в этом процессе выделяется столько, что внутри колонны синтеза часто помещают и трубки парового котла. Благодаря этому получают одновременно водяной пар и более точно поддерживают оптимальную температуру.
Необходимый для синтеза аммиака азот получают из воздуха. Для этого воздух охлаждают до столь низкой температуры, что он полностью сжижается. Азот отделяют от других веществ, входящих в состав жидкого воздуха, посредством перегонки. Водород получают в настоящее время из природных горючих газов, богатых метаном, а также из газов, образующихся при химической переработке каменного угля и нефти.
Установки для производства аммиака оснащены измерительными приборами, показания которых регистрируются и записываются на общем щите. Здесь же сосредоточено управление процессом. Благодаря автоматизации контроля и управления удается устойчиво поддерживать заданный режим, повысить выход продукта и производительность аппаратов, увеличить производительность труда. На новых установках электронные счетно-решающие устройства рассчитывают режим в соответствии с меняющимися условиями (например, изменением активности катализатора) и выдают показания для управления производством.
- Пользуясь изображенной на рисунке 1 схемой синтеза аммиака, объясните назначение всех аппаратов и общий ход технологического процесса.
- Почему необходим циркуляционный компрессор?
- Проследите и объясните ход газовой смеси в колонне синтеза.
- В 20-х годах суточная производительность колонн синтеза не превышала 6-10 т, сейчас строятся колонны синтеза с производительностью 1000-2000 т аммиака в сутки. Каковы преимущества столь мощных аппаратов по сравнению с небольшими?
- В катализаторной коробке температуру катализатора, после того как она достигнет максимума, постепенно понижают посредством отвода теплоты. Почему поддерживается такой температурный режим? (Для ответа на этот вопрос сравните данный процесс с процессом окисления двуокиси серы.)
- Ученые стремятся найти катализатор, который обеспечивал бы достаточную скорость реакции при относительно низкой температуре. Какое практическое значение имеют эти исследования?
- Почему, несмотря на высокое давление в колонне синтеза аммиака, стенки катализаторной коробки и трубки теплообменника изготовляют из тонкой стали?
- Как объяснить, что катализатор "стареет" и через 4-5 лет его приходится заменять новым?
- Какие общие принципы химического производства используются в промышленном процессе синтеза аммиака?
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'