
§ 33. Кислородные соединения фосфора
При сгорании фосфора образуется густой белый дым, осаждающийся на стенках сосуда в виде белого порошка. Это фосфорный ангидрид Р2О5. Прилив в сосуд воды и взболтав ее, получим сначала мутную жидкость. Но вскоре муть исчезает, и получается прозрачный раствор, окрашивающий синий лакмус в красный цвет.
Реакция присоединения воды к фосфорному ангидриду идет в несколько ступеней. Сначала к молекуле ангидрида присоединяется одна молекула воды, и получается метафосфорная кислота НРО3, затем вторая, и получается ортофосфорная, или фосфорная, кислота Н3РО4:
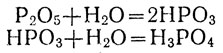
Фосфорный ангидрид энергично присоединяет не только жидкую воду, но и ее пары. Поэтому он применяется для осушения газов.
Фосфорная кислота Н3РО4 имеет структурную формулу
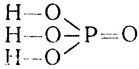
Это твердое вещество, хорошо растворимое в воде. В отличие от азотной, фосфорная кислота нелетуча. В растворе она диссоциирует ступенчато:
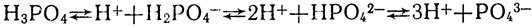
Фосфорная кислота относится к слабым кислотам.
При диссоциации многоосновных кислот каждый последующий ион водорода отщепляется труднее, чем предыдущий, из-за возрастания заряда аниона, притяжение которого ему приходится преодолевать. Поэтому в растворах фосфорной кислоты наряду с нерасщепленными молекулами Н3РО4 много ионов Н2РО4, очень мало ионов PО42- и ничтожно мало ионов РО43-.
Фосфорная кислота взаимодействует только с металлами, расположенными в электрохимическом ряду напряжений левее водорода. Ее средние соли называются фосфатами. В зависимости от количества добавленного к раствору фосфорной кислоты основания в ее молекулах могут заместиться металлом один, два или все три атома водорода:
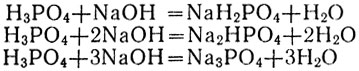
Поэтому с одним и тем же металлом фосфорная кислота может образовывать три разные по составу и свойствам соли. Если в молекулах фосфорной кислоты заместился металлом лишь один атом водорода, а остальные два атома водорода остались связанными с кислотным остатком в одновалентном анионе Н2РО4-, то соль называется дигидрофосфатом (один - два). Если в молекулах кислоты заместились металлом два атома водорода, а с кислотным остатком остался связанным лишь один, образуя ион НРО42-, то соль называется гидрофосфатом. Если же все атомы водорода замещены металлом, то соль называется просто фосфатом. Приведем пример таких солей:
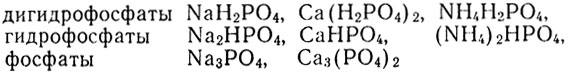
Дигидрофосфаты всех металлов хорошо растворимы в воде. Фосфаты нерастворимы в воде, за исключением фосфатов щелочных металлов. Гидрофосфаты по растворимости занимают промежуточное положение между дигидрофосфатами и средними фосфатами. Все нерастворимые в воде фосфаты растворяются при приливании сильных кислот, так как переходят в кислые соли - дигидрофосфаты, например:
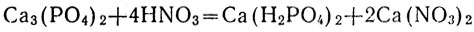
или в ионной форме:
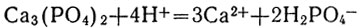
Реактивом на ионы РО43- служит нитрат серебра. При прибавлении его к раствору, содержащему эти ионы, образуется осадок фосфата серебра:
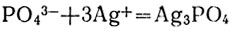
Фосфат серебра ярко-желтого цвета и, как все фосфаты, растворяется при добавлении раствора сильной кислоты.
- Опишите физические и химические свойства: а) фосфорного ангидрида, б) фосфорной кислоты.
- Какие ионы содержатся в растворе фосфорной кислоты?
- Напишите формулы дигидрофосфатов, гидрофосфатов и фосфатов калия и кальция.
- Какие из нижеперечисленных солей фосфорной кислоты хорошо растворимы и какие практически нерастворимы в воде: AlPO4, Mg(H2PO4)2, (NH4)2HPO4, Pb3(PO4)2, Fe3(PO4)2, FePO4, K3PO4? Назовите каждую соль.
- Составьте уравнения реакций фосфорной кислоты: а) с металлами, б) с окислами металлов, в) с основаниями.
- * К раствору гашеной извести приливали порцию за порцией раствор фосфорной кислоты. Сначала получился осадок, который исчез при дальнейшем прибавлении кислоты. Объясните эти явления, составьте уравнения реакций.
- Какие вещества и в какой последовательности будут получаться: а) при пропускании в раствор фосфорной кислоты аммиака, б) при постепенном приливании к раствору фосфорной кислоты раствора едкого кали, в) при постепенном приливании к раствору гидроокиси кальция раствора фосфорной кислоты? Какие явления будут при этом наблюдаться (образование или растворение осадков)? Происходящие реакции изобразите молекулярными и ионными уравнениями.
- * К раствору, содержащему 2 моля фосфорной кислоты, прибавили раствор, содержащий 3 моля едкого кали. Воду выпарили. Каков состав выпавших кристаллов?
- Растворы всех гидрофосфатов окрашивают фенолфталеин в малиновый цвет. Почему? Напишите в ионной форме уравнение реакции между гидрофосфатом и водой. Как называются такие реакции?
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'