
§ 43. Углерод
Химический знак - С. Порядковый номер - 6.
Атомный вес - 12. Строение атома: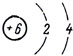
Во внешнем слое атома углерода 4 электрона, а именно два спаренных s-электрона и два неспаренных р-электрона. Судя по числу неспаренных электронов, атом углерода должен быть двухвалентным. Но в атомах спаренные электроны могут разъединяться. Тогда все 4 электрона в атоме углерода окажутся неспаренными, и атом углерода станет четырехвалентным. При этом электронные облака всех четырех электронов приобретают одинаковую вытянутую форму, а их оси оказываются теперь направленными к вершинам тетраэдра (рис. 29). Затрата энергии на разъединение в атоме углерода спаренных s-электронов возмещается за счет выделения энергии при образовании двумя добавочными неспаренными электронами двух новых химических связей с другими атомами, в том числе и с другими атомами того же углерода.
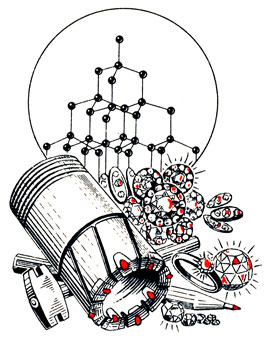
Рис. 29. Строение алмаза и его применение - бриллианты, наконечник бура, алмаз в оправе для резки стекла, алмазный 'карандаш' (кристаллы алмаза выделены красным цветом)
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'