
"Дремучий лес" органической химии
Становилось ясно, что никакой жизненной силы не существует, что вещества, выделенные из организмов растений и животных, могут быть синтезированы искусственным путем, что они имеют ту же природу, что и все прочие вещества. Нужна была теория, которая объясняла бы, как построены органические вещества, почему они гораздо сложнее и много численнее веществ неорганических.
Одна из первых теорий органической химии - теория радикалов - тесно связана с электрохимической теорией уже известного нам Берцелиуса (расцвет ее приходится на 1820-1840 годы). Этот ученый занимался в основном неорганическими соединениями. Подвергая действию электрического тока соли, основания, кислоты, Берцелиус сделал вывод, что все вещества состоят из двух частей, несущих противоположные заряды. И хотя растворы большинства органических соединений электрический ток не проводят, Берцелиус утверждал, что все они также состоят из двух противоположно заряженных частей - радикалов. Радикалы столь же прочны, как и атомы в неорганических соединениях, при химических превращениях они переходят из одной молекулы в другую, не изменяясь. Получалось, что группа атомов - радикал - по своим функциям аналогична одному атому в неорганической химии.
В 1832 г. Либих и Вёлер выполнили классическую работу, которая способствовала укреплению авторитета теории радикалов. Эти ученые исследовали "горькоминдальное масло" (С7H5O). Оказалось, что из него молено получить ряд других соединений, содержащих группу C7H5O (эта группа была названа радикалом бензоилом): С7Н5O-ОН - гидроокись бензоила, С7Н5О-ONa - бензонатриевая соль. (Теперь мы знаем, что "горькоминдальное масло" - это бензойный альдегид, а гидроокись бензоила - это бензойная кислота.)
Заметим, что современные химики широко оперируют самим понятием "радикал" (вспомним, например, радикалы метил СН3, этил С2Н5). Но не стоит забывать, что мы вкладываем в понятие "радикал метил" совсем иной смысл, нежели сторонники этой теории. Так, они считали, что радикалы, как и атомы, могут спокойно существовать в свободном состоянии и что изменить радикал, как и атом, невозможно.
Каково же было замешательство Берцелиуса и его учеников, когда всего через несколько лет французский химик Дюма провел хлорирование уксусной кислоты! По теории радикалов уксусная кислота состоит из радикала ацетила С2Н3О и гидроксильной группы ОН. Дюма нашел, что в уксусной кислоте атом водорода легко замещается на хлор, причем образующаяся хлоруксусная кислота не сильно отличается по свойствам от уксусной:
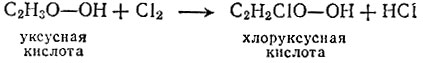
Что же это значит? Радикал ацетил легко изменяется? Берцелиус, Вёлер и другие сторонники теории радикалов не могли смириться с этим открытием. Результат Дюма подвергся сомнению. Но факты - упрямая вещь. От теории радикалов пришлось все-таки отказаться. Ее сменила теория типов, развитая в 1840-1860 годах Жераром и Лораном. По этой теории молекула не состоит из разноименно заряженных частей, а представляет единое целое. При реакции молекулы распадаются на остатки, которые в отличие от радикалов не могут существовать в свободном состоянии. Исходя из реакций, характерных для данных соединений, эти вещества относятся к нескольким типам.
Жерар считал, что все органические соединения можно подразделить на четыре типа:
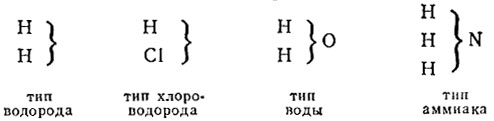
Ангидриды одноосновных органических кислот следовало, таким образом, отнести к типу воды, в молекуле которой оба атома водорода замещены на остатки кислот:
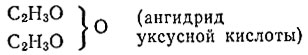
Позже Кекуле предложил новые типы соединений, в том числе и тип метана. К этому типу относились хлорпроизводные метана, нитрометан:
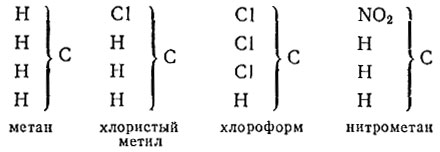
Пока химики имели дело с относительно простыми веществами, все было гладко. Теория типов позволяла даже наглядно и понятно записывать химические реакции. Например, замещение водорода на хлор в метане выглядело таким образом:

Но потом теория типов под натиском новых открытий начала трещать по швам. Вот пример "предсказательной" возможности этой теории: соединение с формулой С6Н6 должно существовать в виде двух изомеров:
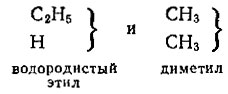
тогда как на самом деле известен лишь один-единственный этан.
Был открыт глицерин, и оказалось, что в его молекуле три гидроксильные группы. Пришлось изобретать "кратные типы". А уже известную нам хлор-уксусную кислоту пришлось отнести к двум типам сразу - к типу воды и к типу хлороводорода:
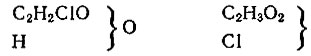
Возникла путаница, и неудивительно, что и Жерар, и Кекуле считали, что формулами можно изобразить превращения веществ, но не их строение, что одному и тому же веществу может соответствовать несколько рациональных формул.
Да, в трудном положении оказались органики первой половины прошлого столетия. Уже известный нам сторонник теории радикалов Фридрих Вёлер писал в 1835 г., что органическая химия представляется ему дремучим лесом, чащей, из которой нельзя выбраться.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'