
Второе дыхание металлоорганической химии
Мы совершили экскурсию по таблице Менделеева и кратко рассмотрели органические производные непереходных металлов (металлоорганические соединения) и некоторых необычных для органической химии элементов (такие соединения называются элементоорганическими). В предыдущих главах мы много говорили о белках, сахарах, нуклеиновых кислотах. Все эти соединения, мало сказать - широко распространены в природе, они составляют основу жизни, Иное дело элементоорганические соединения. Они хотя и оказывают сильнейшее физиологическое действие (вспомните зарин и сальварсан), но в природе, за очень редким исключением, не встречаются, это целиком создание рук человеческих.
А металлоорганические производные переходных металлов? Если бы мы писали нашу книгу в 1950 г., то заявили бы следующее: "переходные металлы за редкими исключениями металлоорганических соединений не образуют" и закончили бы этим главу об элементоорганической химии - области науки, соединившей химию неорганическую и химию органическую. Это в 1950 г. ...
Но вот в 1951 г. одновременно и независимо две группы исследователей получили совершенно необычное соединение, названное ферроценом. В молекуле ферроцена атом железа (типичного переходного металла) зажат между двумя "пятичленными циклопентадиенильными кольцами. Железо связано одновременно с каждым из десяти углеродов ферроцена, формула которого С5Н5FеС5Н5. Связь осуществляется я-электронами колец, поэтому ферроцен относят к классу так называемых π-комплексов. У железа и других переходных металлов одна из внутренних электронных оболочек заполнена не до конца. π-Электроны переходят на свободные электронные орбитали и тем самым связывают атом железа с циклопентадиенильными кольцами,
Открытие ферроцена незамедлительно привело к бурному росту целой области химии - химии металлоорганических производных переходных элементов. До открытия ферроцена считалось, что связь углерод - металл крайне неустойчива, что она быстро и легко разрывается под действием кислорода и влаги, Ферроцен оказался на редкость устойчивым веществом. Он сохраняется даже при кипячении в воде, сопротивляется действию многих агрессивных агентов. Один из первых способов образования ферроцена тоже свидетельствует о чрезвычайной его устойчивости: ферроцен был получен просто путем пропускания паров циклопентадиена через нагретую до 300 °С трубку с железными опилками. В результате в трубке появляется красный налет, похожий на окись железа - это и есть ферроцен. (Позже вспомнили, что на нефтеперерабатывающих заводах давно замечали образование подобного налета при пропускании через железные трубы нефтяных фракций, содержащих циклопентадиен.)
Загадка необычных свойств ферроцена - в его структуре: в ферроцене, как мы уже сказали, атом железа соединен не с одним или двумя атомами углерода, а со всеми десятью. При этом железо сохраняет многие свои свойства: оно легко окисляется и восстанавливается, и обе формы устойчивы:
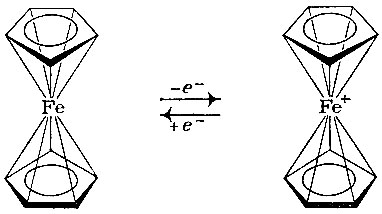
Необычными оказались и свойства органической части молекулы: утратилась способность циклопентадиена вступать в реакции присоединения по двойным связям. Вместо этого появилась склонность к характерным для ароматических соединений реакциям замещения водорода, выраженная даже более сильно, чем у бензола. За это ферроцену было присвоено на звание суперароматической системы. Одно из колец циклопентадиенила оказалось возможным заменить на другие циклические структуры, например, на бензол:
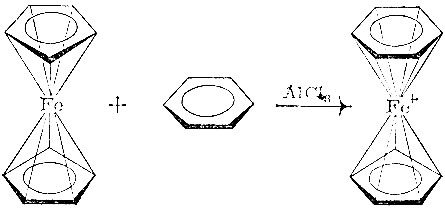
Многие интересные замещенные ферроцены впервые получили советские химики под руководством академика А. Н. Несмеянова. Сегодня известны металоорганические производные всех переходных металлов. Некоторые такие вещества нашли применение как присадки к топливу, красители, биологически активные соединения, многие комплексы применяются в каталитических процессах. И не нужно думать, что устойчивы только достаточно "экзотические" для органической химии π-комплексы переходных металлов. Вот только один пример. Несколько лет назад сотрудники Института химической физики АН СССР изучили новую реакцию: если нагревать или облучать светом платинохлористоводородную кислоту H2PtCl6 (ее получают, растворяя платину в царской водке) с бензолом или толуолом, то атом платины замещает в ароматическом углеводороде один из водородных атомов. И хотя платина - металл переходный, образуется металлоорганическое соединение, похожее на соединение ртути, таллия или свинца. Как видим, химия органических производных переходных элементов оказывается богаче химии металлов непереходных.
С открытием ферроцена, с началом развития химии производных переходных элементов металлоорганическая химия обрела второе дыхание.
* * *
Подведем итоги. Мы рассказали об элементоорганических соединениях, т. е. соединениях, содержащих связь углерода с "необычным" для органической химии элементом - металлом, с фосфором, фтором, кремнием... Значение этих веществ в науке, технике, практике весьма велико. Есть у элементоорганических производных одна особенность - они образуют как бы перешеек, соединяющий два огромных материка, два мира веществ - органических и минеральных" Впрочем, сегодня химия элементоорганических соединений развивается так бурно, что на глазах вырастает в особый огромный континент.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'