
Глава XIII. Органические соединения
1. Предельные углеводороды
764. Вычислить плотность метана по воздуху.
765. Вычислить массу 1 л метана (при н. у.)?
766. Принимая, что в природном газе метан составляет 90 объемных процентов, вычислить, какой объем займет (при н. у.) метан, содержащийся в 1 м3 природного газа, находящегося в магистральном газопроводе под давлением 40 ат и при 0° С. Какова масса этого газа33?
767. Сколько объемов кислорода требуется для сжигания 1 объема метана?
768. Какой объем двуокиси углерода получается при сжигании 100 м3 метана?
769. Написать структурные формулы всех изомеров пентана.
770. Какой член гомологического ряда предельных углеводородов имеет молекулярную массу 142? Написать его формулу34.
771. Вычислить молекулярную массу предельного углеводорода, занимающего 21 место в гомологическом ряду.
772. Во сколько раз плотность пропана больше плотности метана?
773. Сколько объемов кислорода расходуется на сжигание 1 объема пропана?
774. Сколько молей двуокиси углерода получается при сжигании 1 моль октана?
775. Определить, какой объем двуокиси углерода получается при сжигании 1 г гептана.
776. Что представляет собой смесь продуктов, получаемых при хлорировании метана до образования хлористого метила? Как разделить вещества, получаемые при этой реакции? (Галогенозамещенные углеводороды не растворяются в воде.)
777. Сколько хлора и метана (по массе и объему при н. у.) требуются для получения 1 т четыреххлористого углерода?
778. Написать сокращенные структурные формулы двухлорзамещенного этана.
2. Непредельные углеводороды
779. Написать структурные формулы этилена и пропилена.
780. Написать структурные формулы возможных изомеров бутилена.
781. Какое место в ряду этиленовых углеводородов занимает углеводород с молекулярной массой 112?
782. Сколько кислорода расходуется на сжигание 1 моль пропилена?
783. Вычислить объем двуокиси углерода (при н. у.), получаемый при сжигании 2,8 г бутилена.
784. Написать структурные формулы соединений, получающихся в результате присоединения брома к пропилену и бутилену.
785. При пропускании этилена через склянку с бромом масса склянки с содержавшимися в ней веществами увеличилась на 1,4 г. Вычислить, какой объем этилена (при н. у.) прореагировал с бромом.
786. Сколько граммов брома может присоединиться в 3,36 л этилена (при н. у.)?
787. Написать структурную формулу радикала, образованного полимеризацией 5 молекул этилена.
788. Молекулярная масса полиэтилена 1400. Вычислить степень полимеризации.
789. Написать уравнения реакций полимеризации бутиленов, структурные формулы которых СН2 = СН-СН2-СН3; СН3-СН-СН-СН3.
790. Написать уравнение реакции полимеризации изобутилена.
791. Написать структурную формулу элементарного звена полимера бутадиена и уравнение реакции полимеризации бутадиена.
792. Что имеет большую плотность, ацетилен или воздух?
793. Сколько брома может присоединиться к 1,3 г ацетилена?
794. Какой объем кислорода расходуется на сжигание 1 объема ацетилена и сколько объемов двуокиси углерода три этом получается?
795. Какой объем ацетилена (при н. у.) может быть получен из 10 кг карбида кальция, содержащего 15% примесей.
796. Какой объем водорода нужно присоединить к 1 м3 ацетилена, чтобы превратить его в этан?
797. Составить структурную формулу радикала, получаемого отнятием атома водорода от молекулы этилена Как называется этот радикал?
798. Составить уравнение реакции взаимодействия ацетилена с хлористым водородом и определить, какой объем хлористого водорода должен быть присоединен к 1 м3 ацетилена для превращения его в хлористый винил.
799. Составить структурную формулу радикала, образованного полимеризацией 6 молекул хлорвинила.
800. Составить уравнение полимеризации хлорвинила.
801. Средняя молекулярная масса полихлорвинила 100 000. Вычислить степень полимеризации.
802. Как можно установить, что данный полимер полихлорвинил?
803. Вычислить процентное содержание хлора в полихлорвиниле.
804. Определить, сколько изомеров имеет углеводород ацетиленового ряда С4Н6 и составить их структурные формулы.
805. Составить структурные формулы:
- циклобутана;
- этилциклопентана;
- метилциклогексана.
Какими химическими свойствами обладают цикланы?
806. Имеется углеводород, состав которого выражается общей формулой СnН2n, и неизвестно, является ли он углеводородом этиленового ряда или циклопарафином. Как это установить?
3. Ароматические углеводороды
807. Написать формулу дибромбензола и составить структурные формулы его с различным расположение атомов брома в молекуле. Сколько таких структур может быть?
808. Составить уравнение реакции, протекающей при действии смеси концентрированных азотной и серной кислот на бензол. Какую роль в этой реакции играют азотная и серная кислоты?
809. Написать структурные формулы нитробензола, динитробензола и тринитробензола.
810. Какой объем водорода (при н. у.) присоедините к 156 г бензола при его гидрогенизации?
811. Написать структурные формулы метилбензола, диметилбензола, этилбензола и пропилбензола и определить, относятся ли они к одному гомологическому ряду. Написать общую формулу гомологического ряда бензола.
812. Написать структурную формулу стирола и уравнение реакции взаимодействия стирола с бромной водой.
813. Написать структурную формулу радикала, получающегося полимеризацией трех молекул стирола.
814. Написать уравнение полимеризации стирола.
4. Природные источники углеводородов
815. Как можно осуществить следующие превращения:
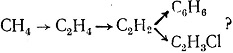
816. Через взятую для испытания пробу нефти был пропущен хлор. Из нефти стал выделяться хлористый водород. О наличии каких углеводородов свидетельствует этот опыт? Ответ мотивировать.
817. Составить уравнения реакций разложения углеводородов состава С12Н26 и С18Н38, происходящих при крекинге нефти.
818. Каким методом осуществляется синтез углеводородов из угля и водорода? Вычислить, не считая потерь в производстве, какой объем метана (при н. у.) получается при этом методе из 1 т угля, содержащего 90 % углерода, и какой объем водорода при тех же условиях расходуется на это.
819. Исходя из состава (Н2 - 60%, СН4 - 25%, СО - 5% и т. д.), вычислить объем коксового газа (при н. у.), который требуется на производство 1 т полиэтилена.
820. Сколько аммиака можно получить из водорода, содержащегося в 100 м3 коксового газа, считая объем при нормальных условиях? Азот дан в избытке.
821. Молекулярная формула углеводорода С5Н8. Составить структурные формулы возможных изомеров. Какой из них называется изопреном?
822. Молекулярная формула углеводорода С4Н6. Сколько двойных связей содержится в его молекуле? Написать его структурную формулу.
823. Составить уравнение реакции дегидрирования бутана с образованием бутадиена и вычислить, какой объем бутана (при н. у.) требуется для производства 1000 т бутадиенового каучука.
824. Составить структурную формулу радикала, образованного соединением двух молекул бутадиена и двух молекул стирола.
825. Допуская, что бутадиенстирольный каучук получается сополимеризацией одинаковых количеств молекул бутадиена и стирола, вычислить, сколько бутана при н. у.) и стирола требуется для производства 1000 т бутадиенстирольного каучука.
826. Изобутилен (диметилэтилен) представляет собой этилен, в котором оба водорода одного звена заменены метальными группами. Составить уравнение реакции полимеризации полимера изобутилена.
827. Считая, что сополимеризация изопрена и изобутилена происходит в одинаковом числе молекул того и другого мономера, составить уравнение реакции для этого процесса.
828. Хлоропрен представляет собой бутадиен, в котором водород одного из средних звеньев замещен хлором. Написать структурную формулу хлоропрена и уравнение реакции, полимеризации его.
5. Спирты, фенолы и альдегиды
829. Написать молекулярную формулу бутилового спирта и структурные формулы возможных его изомеров.
830. Написать молекулярную формулу одноатомного спирта, содержащего 5 атомов углерода в молекуле, и структурные формулы возможных изомеров.
831. Написать уравнения реакций взаимодействия калия с метиловым и пропиловым спиртами.
832. Составить уравнения реакций взаимодействия бромистого водорода с метиловым и пропиловым спиртами.
833. Каким путем можно получить пропилен из пропилового спирта? Указать условия и составить уравнение реакции.
834. Метиловый спирт может быть при определенных условиях получен синтезом из окиси углерода и водорода. Установить, каково отношение объемов окиси углерода и водорода при этом синтезе.
835. Какой объем кислорода (при н. у.) расходуется при сгорании 1 моль этилового спирта?
836. При действии натрия на 0,46 г предельного одноатомного спирта выделилось 112 см3 водорода (при н. у.). Вычислить молекулярную массу этого спирта и установить его формулу.
837. Какими методами может быть получен этиловый спирт из этилена? Вычислить, сколько спирта должно получиться из 112 млн. м3 этилена (при н. у.).
838. Составить уравнение реакции получения дивинила из этилового спирта и вычислить, сколько требуется этилового спирта для получения 10 000 т бутадиенового каучука.
839. Сколько требуется этилового спирта для получения 1 т диэтилового эфира?
840. При взаимодействии фенола с калием выделилось 224 см3 водорода (при н. у.). Сколько было фенола?
841. Сколько гидроокиси натрия может прореагировать с 47 г фенола?
842. Составить уравнения последовательных реакций при синтезе фенола из бензола. Указать условия реакций.
843. Составить уравнение реакции, протекающей в водном растворе между фенолятом натрия и двуокисью углерода.
844. Написать структурные формулы метилового, этилового и пропилового спиртов и указать, как происходит перегруппировка валентных связей при окислении (например, окисью меди) этих спиртов в альдегиды.
845. К какому классу органических соединений относится вещество, состав и структура которого выражается формулой С6Н6СН2ОН?
846. Написать формулу ароматического спирта, производного этилбензола.
847. Сколько формальдегида и воды требуется для приготовления 1 кг 36-процентного раствора формалина?
848. Показать строение элементарного звена фенолоформальдегидной смолы, выразив его структурной формулой.
849. Сколько требуется формальдегида и фенола для получения 10 000 т фенолоформальдегидной смолы реакцией поликонденсации?
6. Карбоновые кислоты
850. Написать структурные формулы изомерных предельных кислот с 4 атомами углерода в молекуле.
851. Написать структурные формулы изомерных предельных кислот с 5 атомами углерода в молекуле.
852. Выразить общей формулой гомологический ряд [предельных карбоновых кислот, поставив карбоксильную группу в конце формулы.
853. Составить общую формулу для нормальных (не Имеющих боковых ответвлений в цепи) предельных карбоновых кислот, обозначив отдельно звенья СН2 и карбоксильную группу. Пользуясь этой формулой, написать сокращенные структурные формулы кислот, содержащих 9, 10, 11 атомов углерода в молекуле.
854. Пользуясь общей формулой для гомологического ряда карбоновых кислот, написать формулы кислот, содержащих 6, 10, 13, 14 и 15 атомов углерода в молекуле.
855. Написать формулы следующих одноосновных карбоновых кислот предельного ряда:
- капроновой нормальной (в молекуле 6 атомов углерода);
- энантной нормальной (в молекуле 7 атомов углерода);
- пеларгоновой (в молекуле 9 атомов углерода);
- пальмитиновой (в молекуле 16 атомов углерода);
- маргариновой (в молекуле 17 атомов углерода).
856. Гидроокись меди окисляет альдегиды в соответствующие кислоты; сам же восстанавливается до гидроокиси меди, (I), который распадается на закись меди и воду. Составить уравнения реакций окисления муравьиного и уксусного альдегидов.
857. Составить структурные формулы натриевых, кальциевых и алюминиевых солей муравьиной, уксусной и пропионовой кислот.
858. Имея в виду, что органические кислоты относятся к слабым электролитам, составить ионные уравнения реакций нейтрализации едким натром муравьиной, уксусной и пропионовой кислот.
859. Составить уравнения последовательно протекающих реакций при получении уксусной кислоты из ацетилена и вычислить, какой объем ацетилена (при н. у.) требуется для получения 10 т уксусной кислоты и сколько расходуется карбида кальция для получения этого количества ацетилена.
860. Составить структурные формулы натриевых и кальциевых солей пальмитиновой, маргариновой и стеариновой кислот.
861. Сколько требуется стеариновой кислоты и гидроокиси натрия для получения 5 т мыла, содержащего 40% воды и других примесей?
862. Вычислить эквиваленты муравьиной и уксусной кислот и определить, сколько нужно взять каждой кислоты, чтобы приготовить по 5 л 0,1 н. раствора.
863. На нейтрализацию 1,2 г одноосновной органической кислоты израсходовано 20 мл 1 М раствора щелочи. Вычислить молекулярную массу кислоты, написать ее формулу.
864. Сколько требуется извести, содержащей 85% окиси кальция СаО, и угля, содержащего 95% углерода, для получения карбида кальция в количестве, необходимом для получения ацетилена, расходуемого на производство 100 т уксусной кислоты? Потери в производстве считать равными 10%.
865. Вывести общую формулу одноосновных ненасыщенных кислот, содержащих в цепи одну двойную связь, записав карбоксильную группу в конце формулы.
866. Написать молекулярные формулы ненасыщенных кислот, содержащих в молекуле 10, 12 и 18 атомов углерода и одну двойную связь.
867. Составить уравнение реакции диссоциации акриловой кислоты.
868. Написать формулы натриевой и кальциевой солей акриловой кислоты.
869. Написать формулы натриевой и кальциевой солей метакриловой кислоты36.
870. Написать формулу калиевой соли олеиновой кислоты.
7. Сложные эфиры. Жиры
871. Составить уравнения реакций:
- метилового спирта с уксусной кислотой;
- этилового спирта с муравьиной кислотой;
- пропилового спирта с уксусной кислотой;
- этилового спирта с акриловой кислотой;
- этилового спирта с метакриловой кислотой;
- метилового спирта с метакриловой кислотой.
872. Составить уравнения реакций взаимодействия метилового спирта с серной и азотной кислотами.
873. Составить уравнение реакции полимеризации метилметакрилата.
874. Написать уравнение реакции омыления уксусно-этилового эфира.
875. Написать формулу глицерида уксусной кислоты36.
876. В состав оливкового и многих других растительных масел входит преимущественно глицерид олеиновой кислоты (С17Н33СООН - с одной двойной связью). Напирать формулу этого глицерида.
877. В состав высыхающих масел входят глицериды линолевой кислоты (С17Н31СООН - с двумя двойными связями) и линоленовой кислоты (С17Н29СООН - с тремя двойными связями). Высыхание олифы, которая готовится из этих масел, происходит за счет окисления по месту двойных связей. Написать формулы глицеридов указанных Кислот.
878. Написать уравнения реакций взаимодействия глицеридов пальмитиновой (C15H31COOH) и стеариновой (С17Н35СООН) кислот с гидроокисью натрия.
879. Написать уравнения реакций взаимодействия линолевой и линоленовой кислот с бромной водой.
880. Написать уравнение реакции гидролиза глицерида стеариновой кислоты.
881. Сколько глицерина и стеариновой кислоты получится из 1 т жира, содержащего 80% глицерида стеариновой кислоты, в результате омыления этого глицерида?
882. Сколько гидроокиси натрия и жира, представляющего собой глицерид стеариновой кислоты, требуется для получения 1 т стеариновокислого натрия, если потери в производстве составляют 20%?
883. Какой объем водорода (при н. у.) требуется для гидрирования 1 т жира, представляющего собой глицерид олеиновой кислоты?
884. Из сложных эфиров, образуемых глицерином и минеральными кислотами, наиболее важным является эфир, образованный глицерином и азотной кислотой и называемый нитроглицерином. Написать структурную формулу нитроглицерина.
885. Сколько глицерина и азотной кислоты расходуется на получение 1 кг нитроглицерина? Вычислить объем газом (при н. у.), получающихся при взрыве 1 кг нитроглицерина:
4C3H5(ONO2)3 → 6N2 + 12CO2 + 10H2O + O2.
8. Углеводы
886. Написать уравнение реакции взаимодействия глюкозы с гидроокисью кальция.
887. Каким методом можно восстановить глюкозу в шестиатомный спирт? Написать уравнение реакции.
888. Выразить уравнением процесс спиртового брожения глюкозы и вычислить, сколько глюкозы расходуется на получение 1 кг спирта. Потерь в производстве не считать.
889. Написать уравнение гидролиза свекловичного сахара (тростникового) и вычислить, сколько глюкозы и фруктозы может быть получено из 1 кг сахара.
890. Написать итоговое уравнение полного гидролиза крахмала и вычислить, сколько глюкозы может быть получено из 1 т картофеля, содержащего 20% крахмала, при выходе 70%.
891. Сколько этилового спирта может быть получено из 1 т пшеницы, содержащей 70% крахмала, если потери в производстве составляют 15%.
892. Какое количество древесных отходов, содержащих 50% клетчатки, расходуется на получение 1 т гидролизного спирта (потери в производстве составляют 30%)? Какое количество картофеля, содержащего 20% крахмала, это сэкономит, если при использовании картофеля потери в производстве будут 15%?
893. Какое количество клетчатки и азотной кислоты "расходуется на получение 1 т тринитроклетчатки, если потери в производстве составляют 12%?
894. Этерификация клетчатки в ацетилцеллюлозу практически производится не уксусной кислотой, а уксусным ангидридом. Имея это в виду, составить уравнение реакции ^взаимодействия клетчатки с уксусным ангидридом с образованием диацетилцеллюлозы.
9. Азотсодержащие органические соединения
895. Написать формулы нитрометана, нитроэтана и нитропропана.
896. Одним из способов получения нитросоединений предельных углеводородов является нагревание их с разбавленной азотной кислотой. Составить уравнение реакции получения нитроэтана по этому способу.
897. В нитросоединениях могут содержаться две и более нитрогрупп. Написать формулы динитробензола и тринитробензола.
898. Написать структурную формулу тринитротолуола тротила), одного из взрывчатых веществ.
899. Вычислить, сколько расходуется толуола и азотной кислоты на получение 100 т тротила.
900. Вычислить, не считая потерь в производстве, сколько требуется бензола для получения 1000 т анилина.
901. При получении анилина из нитробензола на 1 кг анилина расходуется 1,39 кг нитробензола. Вычислить процент выхода продукта.
902. Мочевина в технике получается нагреванием смеси аммиака и двуокиси углерода под давлением. Схема реакции:
NH3 + CO2 → CO(NH2)2.
Исчислить, какие объемы аммиака и двуокиси углерода (при н. у.) расходуются на получение 1 т мочевины.
903. Определить, что является элементарным звеном в мочевиноформальдегидной смоле37.
904. Сколько мочевины и формальдегида требуется для получения 100 т мочевиноформальдегидной смолы? Потери в производстве не считать.
905. Написать сокращенные структурные формулы аминопропионовой кислоты при разном расположении групп NH238.
906. Написать сокращенную структурную формулу аминомасляной кислоты (производной от бутана) при расположении аминогруппы в последнем звене от карбоксила.
907. Написать формулу медной соли аминоуксусной кислоты.
908. При определенных условиях в аминокислотах, начиная от γ-кислот, может происходить химическое взаимодействие между карбоксильной группой и аминогруппой. Это заключается в следующем: атом водорода аминогруппы связывается с гидроксилом карбоксильной группы, образуя воду. Благодаря образующимся свободным связям I обе группы соединяются друг с другом:
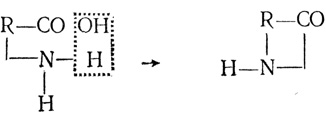
В результате образуется циклическое соединение - лактам. Вывести формулу лактама аминомасляной кислоты.
909. Написать формулу аминокапроновой кислоты (содержащей 6 атомов углерода в молекуле), в которой аминогруппа расположена на противоположном от карбоксила конце, и вывести формулу лактама, образуемого этой кислотой.
910. Капролактам при определенных условиях подвергается поликонденсации. Получаемый продукт называется поликапролактамом. В процессе синтеза его происходит разрыв связи между NH и СО. В результате образуется активный радикал, являющийся элементарным звеном поликонденсата. Составить уравнение поликонденсации капролактама.
911. Исходным веществом для получения капролактама служит фенол. Вычислить, не считая потерь в производстве, сколько фенола расходуется на получение 1000 т капрона.
912. Волокно энант получается из продукта поликонденсации аминоэнантовой кислоты (содержащей 7 атомов углерода в молекуле). Написать формулу этой кислоты, структурную формулу элементарного звена поликонденсата и уравнение реакции поликонденсации аминоэнантовой кислоты.
913. Волокно найлон получается из продукта поликонденсации гексаметилендиамина H2N - (CH2)6 - NH2 и адипиновой кислоты НООС - (СН2)4 - СООН.
- Написать структурную формулу элементарного звена поликонденсата;
- составить уравнение реакции поликонденсации гексаметилендиамина и адипиновой кислоты;
- вычислить, сколько требуется гексаметилендиамина и адипиновой кислоты для получения 1 т поликонденсата.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'