
Предельные КПД и производительности систем биофотолиза воды
В настоящее время на основе известных сведений о механизме и эффективности фотосинтеза можно сделать оценки максимально возможных значений КПД и производительности преобразователей солнечной энергии, основанных на фотосинтетическом получении водорода.
Характерной особенностью фотосинтеза растений и микроскопических водорослей является эффективный процесс окисления воды под действием света с образованием молекулярного кислорода.
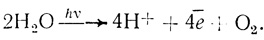 (3.49)
(3.49)При условии, что все четыре электрона, отданных в цепь электронного транспорта фотосинтетического аппарата на конечной, стадии фотосинтеза, удается перевести на протоны с образованием молекулярного водорода:
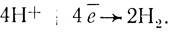 (3.50)
(3.50)КПД систем фотосинтетического получения водорода могут быть оценены по уравнениям [157, 158].
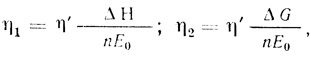 (3.51)
(3.51)где η1, η2 - коэффициент полезного действия по теплоте и свободной энергии соответственно; η' - доля солнечной энергии, поглощаемая фотосинтезирующими системами; ΔН - теплота реакции водорода с кислородом; ΔG - свободная энергия реакции водорода с кислородом; n - квантовый расход на образование одного моля кислорода (или двух молей водорода); Е0 - энергия квантов света с максимальной эффективностью фотосинтеза.
Процесс фотосенсибилизированного переноса электронов от воды в электронотранспортную цепь фотосинтеза происходит весьма эффективно, однако в литературе существуют довольно противоречивые сведения о минимальном квантовом расходе n образования молекулярного кислорода в фотосинтезе. Это связано как с методическими трудностями определения квантовых выходов, так и с тем, что фотосинтетический аппарат растений и водорослей подвержен различного рода регуляторным воздействиям, что накладывает определенный отпечаток на воспроизводимость определяемых величин. В силу этого еще до настоящего времени продолжает дискутироваться вопрос о величине минимального квантового расхода на молекулу О2 в механизме фотосинтеза. В работе [495] собраны данные по определению квантовых расходов на образование кислорода, выполненные в девяти различных лабораториях в период с 1939 по 1957 г.
Всего в указанных лабораториях было сделано около 270 измерений квантовых расходов образования О2, причем найденные величины имеют диапазон изменений от 2 до 18 квантов света на молекулу кислорода. В предположении, что каждое из 270 измерений квантового расхода статистически независимо, проведенный нами анализ дает среднее значение 8,7 со среднеквадратичным отклонением 2,6 [150].
Полученная величина квантового расхода 8,7±2,6 согласуется с изложенной выше двухквантовой схемой переноса электрона и характеризует эффективность первичных стадий механизма фотосинтеза. Окисление воды с образованием молекулярного кислорода связано с переносом четырех электронов. В предположении, что при достаточно эффективной организации темновых стадий процесса четыре электрона удается перенести на протоны с образованием молекулярного водорода, минимальный квантовый расход на образование двух молекул водорода также будет равен восьми.
Реакция использования синтетического топлива, характеризуется следующими термодинамическими параметрами [496]:
2Н2 + O2 = 2Н2O. (3.52)
ΔН = -136,5 ккал/моль; ΔG = -113,4 ккал/моль
(25°С; 1 атмосфера водорода и кислорода, вода в жидком состоянии). Если принять, что оптимальная пороговая длина волны λ0, для которой энергетическая эффективность максимальна, у зеленых растений равна 700 нм [495], то максимальное значение КПД преобразования энергии при освещении светом 700 нм с энергией квантов 40,8 ккал/эйнштейн по аккумуляции внутренней энергии равен 41,8%, по аккумуляции свободной энергии - 34,7%.
Эффективность поглощения зелеными растениями солнечного света по всему спектру солнечного излучения определяется спектральными характеристиками фотосинтетических пигментов и может быть найдена по уравнению
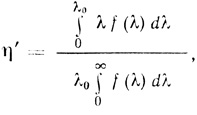 (3.53)
(3.53)где f(λ) - распределение солнечного света по длинам волн. Согласно [495] зеленые растения способны поглощать 40-45% солнечной радиации. С учетом этого теоретическая величина КПД преобразования солнечной энергии при фотосинтетическом получении водорода составляет ∼17% по внутренней энергии и ∼14% по свободной энергии. Эти величины, по-видимому, предельные коэффициенты преобразования энергии путем биофотолиза воды.
На КПД преобразования энергии определенный отпечаток могут накладывать кинетические условия выделения водорода. В реальных системах процесс переноса электрона с переносчика фотосистемы I на протоны конкурирует с параллельными процессами электронного транспорта, в том числе и циклического характера, имеющими место в природном фотосинтезе:
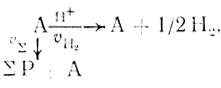 (3.54)
(3.54)где υH2 - скорость образования водорода; υΣ - суммарная скорость конкурирующих параллельных процессов. С учетом кинетических эффектов коэффициент преобразования энергии равен
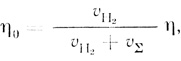 (3.55)
(3.55)где η - термодинамический коэффициент преобразования. Видно, что только в условиях, когда скорость переноса электрона на протоны с образованием водорода существенно превышает суммарную скорость конкурирующих процессов, можно достичь предельный термодинамический коэффициент преобразования световой энергии.
Теоретические значения КПД преобразования энергии путем фотосинтетического получения водорода лежат в интервале КПД фотоэлектрических преобразователей. Так, например, согласно [496, 498], максимальный КПД кремниевых элементов, облучаемых солнечным светом, равен ∼20%, экспериментальные значения лежат в интервале 3-15%. Таким образом, при разработке систем ассимиляции солнечной энергии путем фотосинтетического получения водорода не следует ожидать больших преимуществ этих систем в эффективности преобразования солнечной энергии. Основные преимущества должны быть связаны, по-видимому, с большой доступностью и высокой возобновляемостью такого рода систем.
Представляет интерес оценка предельных скоростей фотосинтеза на основе знания лимитирующей скорости электронного транспорта. Предельная максимальная скорость фотосинтеза определяется концентрацией реакционных центров, поглощающих весь падающий световой поток при насыщающих интенсивностях света. Рассмотрим предельно возможную скорость реакции, которая может реализоваться, если в системе поглощают свет только реакционные центры в отсутствие фотосинтетической антенны. При толщине светопоглощающего слоя в 1 см и среднем коэффициенте молярного поглощения около 104 м-1 см-1 концентрация реакционных центров равна 5⋅10-4 М/л. При освещении поверхности в 1 м2 поверхностная концентрация реакционных центров равна 5⋅10-3 М/м2 (объем системы 10 л). В этих условиях максимальная скорость реакции, которая определяется уравнением
υмакс = kкат[С], (3.56)
где kкат - константа скорости лимитирующей стадии процесса, равна 0,25 М/м2⋅с (лимитирующая стадия электронного транспорта характеризуется константой скорости около 50 с-1, см. выше). При десятичасовом освещении производительность квадратного метра поверхности по кислороду с учетом необходимости переноса восьми электронов равна ∼103 М О2/м2⋅сут. Эта производительность, которая могла бы реализоваться при высоких интенсивностях света в отсутствие фотосинтетической антенны.
В реальных системах необходимо учесть, что концентрация реакционных центров в системе, полностью поглощающей световой поток, будет к 2⋅102 раз меньше (количество молекул пигмента антенны на один реакционный центр). В соответствии с этим предельная максимальная производительность по кислороду равна около 5 М О2/м2⋅сут. Эффективная производительность по водороду равна ∼10 М Н2/м2⋅сут.
В ряде случаев фотосинтезирующие системы удается вывести в режим предельной максимальной скорости. В первую очередь это относится к микробиологическим системам, которые характеризуются высокой эффективностью фотосинтеза. Так, фоторазложение воды, осуществляемое суспензией хлореллы с образованием кислорода, в оптимальных условиях культивирования дает 130-140 л (около 6 М) кислорода с 1 м2 освещаемой поверхности в сутки [499]. При условии, что "восстановительную" силу такой суспензии можно было бы конвертировать в водород, производительность по водороду составляла бы около 12 М/м2 в сутки.
К той же величине предельной производительности водорода с 1 м2 в сутки приводят расчеты, основанные на экспериментальном измерении световых потоков на поверхности Земли. Фотосинтетические системы лимитированы по свету. В пределе в оптимальных условиях проведения процесса скорость образования водорода определяется величиной светового потока. Используя найденный предельный коэффициент преобразования энергии, можно оценить производительность систем фотосинтетического получения водорода. В южных районах уровень фотосинтетически активной радиации составляет около 75 ккал/см2 в год [395].
При КПД поглощенной энергии около 40% (17% от всей солнечной энергии) это дает среднегодовую интенсивность фотосинтетически активной радиации 830 ккал/м2 в сутки. Используя тепловой эффект реакции, обратной фотосинтетическому разложению (140 ккал/моль), можно найти, что с помощью данного потока фотосинтетической радиации получается 6 М О2 (соответственно 12 М Н2). Таким образом, оценки предельной производительности систем биофотолиза воды, сделанные из двух принципиально различных посылок, приводят к выводу, что эта величина составляет 8-12 М водорода/м2 в сутки. К аналогичной оценке приводят расчеты, сделанные в работах [73, 500] из других предпосылок.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'