
Обратимая инактивация гидрогеназ кислородом
Все исследованные нами гидрогеназы (Th. roseopersicina, Pr. aestuarii, Al. eutrophus), а также гидрогеназы, изученные в других лабораториях, не способны катализировать реакции выделении водорода или восстановления органических субстратов в присутствии кислорода. Особые надежды мы возлагали на гидрогеназу из водородокисляющих бактерий Al. eutrophus, которые являются аэробными микроорганизмами, проводящими окисление водорода кислородом. Однако и в этом случае фермент в растворе в присутствии кислорода не катализирует реакцию восстановления органических соединений водородом.
Инактивация гидрогеназ кислородом обратима. Экспериментальным критерием, указывающим на обратимый характер инактивации гидрогеназ кислородом или другими окислителями, является автокаталитический характер восстановления субстратов водородом под действием гидрогеназ [323]. В исходном состоянии гидрогеназы неактивны. При накоплении в среде восстановителей или в присутствии каталитических количеств восстановленных форм субстратов гидрогеназы полностью восстанавливают свою активность:
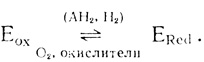 (3.91)
(3.91)Стационарное состояние фермента (в окисленной или восстановленной форме) определяется соотношением скоростей восстановления и окисления активного центра фермента. По-видимому, отношение скоростей восстановления и окисления активного центра зависит от микробиологического источника фермента. Можно думать, что для гидрогеназы из водородокисляющих бактерий Al. eutrophus при прочих равных условиях стационарное состояние смещено в сторону восстановленной формы [301, 302].
Таким образом, при использовании сильных восстановителей гидрогеназы можно "активировать", проводя восстановление активного центра. Если реакция проводится в избытке восстановителя, как это имеет место при исследовании процессов выделения водорода из восстановленных субстратов или в присутствии дитионита натрия, весь фермент находится в каталитически активной Е-форме.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'