
Занятие 6. Закон сохранения веса веществ
(Занятие рассчитано на 1 час и проводится после изучения закона сохранения веса веществ. В случае наличия достаточного времени части прибора а и б (рис. 12) с веществом могут быть взвешены порознь до опыта и после опыта.)
Оборудование: прибор, состоящий из пробирки с основной углекислой медью и хлорокальциевой трубки с натронной известью, соединённых с помощью каучуковой пробки; штатив, спиртовка и спички, весы и разновес (или сухой песок;. 1
Цель работы заключается в том, чтобы доказать, что вес веществ, вступивших в реакцию, равен весу веществ, образовавшихся в результате реакции. В качестве примера будет изучена реакция разложения основной углекислой меди:
углекислая медь = окись меди + вода + углекислый газ.
Для опыта служит прибор, изображённый на рис. 14. В пробирке а - углемедная соль, в хлорокальциевой трубке б - натронная известь, она служит для поглощения воды и углекислого газа.
1. Взвесьте на весах весь прибор и запишите его вес (или уравновесьте прибор с помощью песка).
2. Закрепите прибор в штативе горизонтально; выньте пробку из хлорокальциевой трубки и осторожно нагревайте углемедную соль: при сильном нагревании разложение идёт очень быстро, и натронная известь не успевает поглощать всё количество воды и углекислого газа.
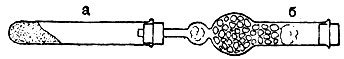
Рис. 14
3. Продолжайте нагревание до разложения всего количества углекислой меди так, чтобы не осталось ни одного зелёного комочка. Не вынимая прибор из штатива, дайте пробирке вполне остыть. В это время зарисуйте прибор. Укажите стрелкой, где поглощаются вода и углекислый газ. Запишите уравнение реакции.
4. Остывший прибор закройте пробкой и снова взвесьте. Если вся работа выполнена хорошо, то вы должны получить полное подтверждение закона сохранения веса веществ. Запищите в тетради результаты вашего опыта. Кроме того, ответьте письменно на следующие вопросы:
а) Что в этом опыте подтверждает закон сохранения веса веществ?
б) Как изменится вес, если нагревать углекислую медь в открытой пробирке? Почему?
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'