
Занятие 31. Углеводы
(Работа рассчитана на 2 часа. Каждый учащийся выполняет по указанию учителя половину описанных здесь опытов. )
Оборудование: железный штатив, спиртовка, асбестовая сетка, стеклянная вата (не обязательно), стеклянная палочка, фильтровальная бумага, воронка, стойка с пробирками, химический стакан, держатель для пробирок, раствор глюкозы (10%), толчёный сахар (сахароза), раствор сахарозы (20%), известковое молоко, концентрированный раствор NaOH, раствор H2SO4 (1 : 5), раствор НСl, раствор CuSO4, крахмал, раствор йода в спирте, кусочек чёрного хлеба, сырой картофель, вата.
На столе общего пользования: аммиачный раствор окиси серебра, медно-аммиачный раствор, аппарат Киппа заряженный на СО2.
Опыт 1. Восстановление аммиачного раствора окиси серебра глюкозой (реакция серебряного зеркала).
1. К аммиачному раствору окиси серебра, взятому в чистую пробирку, прилейте половинное количество раствора глюкозы.
2. Нагревайте смесь осторожно на спиртовке, обнося пробирку вокруг пламени, чтобы нагрев был равномерным и медленным.
3. Составьте уравнение реакции, зная, что глюкоза здесь окисляется в глюконовую кислоту
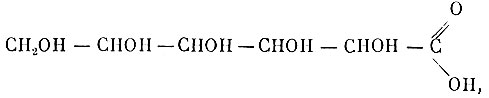
а Ag2O восстанавливается до металлического серебра.
Опыт 2. Изменение сахара при нагревании.
1. Насыпьте в пробирку (на 1/4 её высоты) толчёного сахара (сахарозы). Нагревайте медленно в пламени спиртовки.
2. При 160 сахар плавится в прозрачную жидкость. При дальнейшем нагревании (200°) сахар окрашивается в жёлтый, затем в желто-бурый цвет.
3. Отлейте часть расплавленной массы на сложенный в несколько раз лист чистой бумаги. По остывании образуется аморфная масса - "карамель".
4. Оставшуюся часть продолжайте нагревать. Сахар темнеет, обугливается и выделяет белый дым. Происходит сухая перегонка. Выделяющиеся газообразные продукты можно зажечь, если поднести пламя к отверстию пробирки.
Опыт 3. Образование сахарата.
1. В стаканчик налейте около 20 см3 20% раствора сахара и добавьте такое количество известкового молока (смесь Са(ОН)3 с водой), чтобы часть извести осталась не растворённой. Перемешивайте содержимое стакана. Образуются растворимые в воде сахараты кальция.
2. Отфильтруйте часть раствора в пробирку.
3. В раствор, находящийся в пробирке пропускайте углекислый газ. При этом образуется осадок карбоната кальция, сахар же остаётся в растворе. Составьте уравнение реакции.
Проведённый опыт показывает наличие гидроксильных групп в молекуле сахарозы и иллюстрирует производственные процессы дефекции (действие извести на сок, содержащий сахар с примесями) и сатурации (действие СO3 на раствор сахарата).
Опыт 4. Гидролиз сахарозы.
1. Раствор сахарозы не восстанавливает гидрата окиси меди.
В пробирку налейте раствор едкого натра и добавьте несколько капель раствора CuSO4 (NaOH непременно должен быть в избытке). Прилейте затем туда же раствор сахара и нагревайте. Восстановления гидрата окиси меди в закись меди не происходит.
2. Раствор сахара при гидролизе образует моносахариды, восстанавливающие Сu(ОН)2 в Сu2O.
Налейте в чистую пробирку немного раствора сахара, добавьте туда 2-3 капли разбавленной H2SO4 и прокипятите смесь в течение нескольких минут.
В другой пробирке получите осадок Сu(ОН)2 способом, какой был указан выше (NaOH должен быть в значительном избытке), добавьте к нему раствор сахара, подвергавшегося гидролизу, и смесь нагрейте.
Происходит образование сперва жёлтого осадка СuОН, а затем красного - Сu2O.
3. Составьте уравнения реакций гидролиза сахарозы и окисления глюкозы гидратом окиси меди.
Опыт 5. Приготовление крахмального клейстера; йодная проба на крахмал.
1. Вскипятите воду в химическом стаканчике.
2. В пробирку возьмите около 1 см3 хорошо растёртого крахмала, прилейте туда же воды и хорошо взболтайте.
3. Вылейте смесь медленно в горячую воду и прокипятите. Образуется крахмальный клейстер.
4. К небольшому количеству крахмального клейстера в пробирке прибавьте 1-2 капли раствора йода в спирте (йодной настойки). Образуется характерное синее окрашивание.
5. Нагрейте полученную смесь. Окраска исчезает. Дайте пробирке остыть; окраска появляется вновь.
Окрашенное соединение крахмала с йодом неустойчиво при высоких температурах.
Опыт 6. Гидролиз крахмала.
1. Крахмал, являясь полисахаридрм, не восстанавливает Сг(ОН)2 в Сu2O. Убедитесь в этом, нагревая в пробирке крахмальный клейстер с свежеосаждённым гидратом окиси меди. Образования Сu2O не происходит.
2. Разжуйте хорошо кусочек чёрного хлеба. Смоченный таким образом слюной хлеб поместите в пробирку прибавьте туда раствор NaOH и несколько капель CuSO. Нагрейте смесь. Образуется СuОН, а затем Сu2O.
Крахмал, содержащийся в хлебе, под действием птиалина слюны подвергается гидролизу. Продукты гидролиза дали реакцию с Сu(ОН)2.
3. При наличии времени проведите гидролиз крахмала с помощью минеральной кислоты.
В пробирку налейте 3-4 см3 раствора крахмала и 1 - см раствора H2SO4. Смесь прокипятите в течение 5 минут, затем охладите, нейтрализуйте и проведите реакцию с Сu(ОН)2. Образуется осадок Cu2O.
Опыт 7. Растворение клетчатки в медно-аммиачном растворе.
Свойство клетчатки растворяться в медно-аммиачном растворе и, обратно, выделяться из него при подкислении лежит в основе так называемого медно-аммиачного способа производства искусственного шёлка.
1. В пробирку с медно-аммиачным раствором* поместите кусочек ваты и помешивайте стеклянной палочкой, пока вата не растворится.
* (Раствор готовится для всех учащихся до урока (состав его должен быть разъяснен в классе). В химический стаканчик наливают 20-30 концентрированного раствора CuSO4 и прибавляют к нему такое же количество раствора NaOH. Дают осадку Cu(OH)2 отстояться и раствор декантируют. Промывают осадок декантацией 3-4 раза. Затем растворяют его в концентрированном (25%) растворе аммиака. Образуется ярко синий раствор.)
2. Если растворение произошло не полностью, слейте прозрачный раствор в другую пробирку.
К фильтрату прибавьте раствора соляной кислоты. Окраска раствора меняется и вновь выделяется клетчатка в виде хлопьевидного осадка.
В промышленности этот осадок получают в виде нитей.
Задачи.
1. Докажите на опыте, что картофель (лучше свежий) и неспелое яблоко содержат крахмал.
2. Мороженый картофель приобретает сладкий привкус. Яблоко, созревая, становится сладким. Как объяснить эти явления?
3 Смешайте немного крахмального клейстера в пробирке со слюной. Через некоторое время прибавьте туда раствор йода. Появляется ли характерное синее окрашивание? Дайте объяснение.
4. Проверьте, прошёл ли гидролиз в выданном вам растворе сахарозы?
5. Определить опытным путём, в какой из двух выданных пробирок находится глицерин и в какой - крепкий раствор сахарозы.
6. Определить опытным путём, в какой из трех выданных пробирок находится раствор крахмала, где - раствор тростникового сахара и где раствор глюкозы.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'