
Искусственные элементы
Если спросить ученых, какие из открытий XX в. важнейшие, то едва ли кто-нибудь забудет назвать искусственный синтез химических элементов. За короткий срок - менее 40 лет- список известных химических элементов увеличился на 18 названий. И все 18 были синтезированы, приготовлены искусственным путем.
Слово "синтез" обычно обозначает процесс получения из простого сложного. Например, взаимодействие серы с кислородом есть химический синтез двуокиси серы SO2 из элементов.
Синтез элементов молено понимать таким лее образом: искусственное получение из элемента с меньшим зарядом ядра, меньшим порядковым номером элемента с большим порядковым номером. А сам процесс получения называется ядерной реакцией. Ее уравнение записывается так же, как и уравнение обыкновенной химической реакции. В левой части реагирующие вещества, в правой - получающиеся продукты. Реагирующие вещества в ядерной реакции - это мишень и бомбардирующая частица.
Мишенью может служить любой элемент периодической системы (в свободном виде или в виде химического соединения).
Роль бомбардирующих частиц играют α-частицы, нейтроны, протоны, дейтроны (ядра тяжелого изотопа водорода), а также так называемые многозарядные тяжелые ионы различных элементов - бора, углерода, азота, кислорода, неона, аргона и других элементов периодической системы.
Чтобы произошла ядерная реакция, необходимо столкновение бомбардирующей частицы с ядром атома мишени. Если частица обладает достаточно большой энергией, то она может настолько глубоко проникнуть к ядру, что сольется с ним. Так как все перечисленные выше частицы, кроме нейтрона, несут положительные заряды, то, сливаясь с ядром, они увеличивают его заряд. А изменение значения Z и означает превращение элементов: синтез элемента с новым значением заряда ядра.
Чтобы найти способ ускорять бомбардирующие частицы, придавать им большую энергию, достаточную для их слияния с ядрами, изобрели и сконструировали специальный ускоритель частиц- циклотрон. Затем построили специальную фабрику новых элементов - ядерный реактор. Его прямое назначение- вырабатывать ядерную энергию. Но поскольку в нем всегда существуют интенсивные потоки нейтронов, то их легко использовать для целей искусственного синтеза. Нейтрон не имеет заряда, и потому его не надо (да и невозможно) ускорять. Напротив, медленные нейтроны оказываются более полезными, чем быстрые.
Химикам пришлось изрядно поломать голову и проявить подлинные чудеса изобретательности, чтобы разработать способы отделения ничтожных количеств новых элементов от вещества мишени. Научиться изучать свойства новых элементов, когда в наличии были считанные количества их атомов...
Трудами сотен и тысяч ученых в периодической системе было заполнено восемнадцать новых клеток.
Четыре - в ее старых границах: между водородом и ураном.
Четырнадцать - за ураном.
Вот как все это происходило...
Технеций, прометий, астат, франций... Четыре места в периодической системе долго оставались пустыми. Это были клетки № 43, 61, 85 и 87. Из четырех элементов, которые должны были занять эти места, три предсказаны Менделеевым: экамарганец - 43, экаиод - 85 и экацезий - 87. Четвертый - № 61 - должен был принадлежать к редкоземельным элементам.
Эти четыре элемента были неуловимы. Усилия ученых, направленные на их поиски в природе, оставались безуспешными. С помощью периодического закона давно уже были заполнены все остальные места в таблице Менделеева - от водорода до урана.
Не один раз в научных журналах появлялись сообщения об открытии этих четырех элементов. Экамарганец "открывали" в Японии, где ему дали имя "ниппоний", в Германии назвали "мазурий". Элемент № 61 "открывали" в разных странах по крайней мере трижды, он получал имена "иллиний", "Флоренции", "цикл оний". Экаиод находили в природе также неоднократно. Ему давали имена "алабамий", "гельвеций". Экацезий, в свою очередь, получал названия "Виргинии", "Молдавии". Некоторые из этих названий попадали в различные справочники и даже проникали в школьные учебники. Но все эти открытия не подтверждались: каждый раз точная проверка показывала, что допущена ошибка, и случайные ничтожные примеси были приняты за новый элемент.
Долгие и трудные поиски привели наконец к открытию в природе одного из неуловимых элементов. Оказалось, что экацезий, который должен занимать в периодической таблице 87-е место, возникает в цепочке распада природного радиоактивного изотопа урана-235. Это короткоживущий радиоактивный элемент.
Элемент № 87 заслуживает того, чтобы о нем рассказать подробнее.
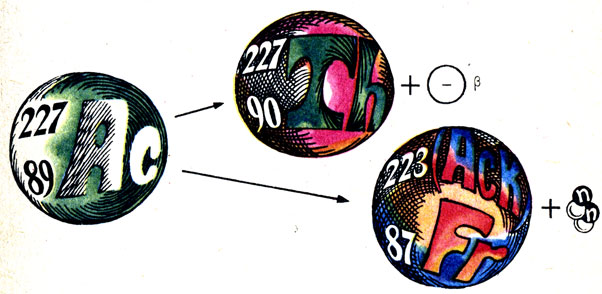
Схема образования элемента № 87 - франция. Некоторые радиоактивные изотопы могут распадаться двумя путями, например посредством и α- и β-распада. Такое явление называется радиоактивной вилкой. Все природные радиоактивные семейства содержат вилки
...Теперь в любой энциклопедии, в любом учебнике по химии читаем: франций (порядковый № 87) открыт в 1939 г. французским ученым Маргаритой Перей. Кстати сказать, это третий случай, когда честь открытия нового элемента принадлежит женщине (раньше Мария Кюри открыла полоний и радий, Ида Ноддак - рений).
Как Перей все лее удалось поймать неуловимый элемент? Вернемся на много лет назад. В 1914 г. три австрийских радиохимика - С. Мейер, В. Гесс и Ф. Панет - занялись изучением радиоактивного распада изотопа актиния с массовым числом 227. Было известно, что он входит в семейство актиноурана и испускает β-частицы; следовательно, продукт его распада торий. Однако у ученых мелькали смутные подозрения, что актиний-227 в редких случаях испускает и α-частицы. Иными словами, здесь наблюдается один из примеров радиоактивной вилки. Легко сообразить: в ходе такого превращения должен образовываться изотоп элемента № 87. Мейер и его коллеги действительно наблюдали α-частицы. Требовались дальнейшие исследования, но они были прерваны первой мировой войной.
Маргарита Перей шла по тому же пути. Но в ее распоряжении были более чувствительные приборы, новые, усовершенствованные методы анализа. Поэтому-то ей и сопутствовал успех.
Франций относят к числу искусственно синтезированных элементов. Но все-таки сначала элемент был обнаружен в природе. Это изотоп франций-223. Его период полураспада составляет всего 22 минуты. Становится понятным, почему франция так мало на Земле. Во-первых, из-за своей недолговечности он не успевает концентрироваться в сколь-либо заметных количествах, во-вторых, сам процесс его образования отличается невысокой вероятностью: всего 1,2% ядер актиния-227 распадается с испусканием α-частиц.
В связи с этим франций выгоднее приготовлять искусственным путем. Уже получено 20 изотопов франция, и самый долгоживущий из них - франций-223. Работая с совершенно ничтожными количествами солей франция, химики сумели доказать, что по своим свойствам он чрезвычайно похож: на цезий.
Элементы № 43, 61 и 85 оставались неуловимыми. В природе их никак не удавалось найти, хотя ученые уже владели могучим методом, безошибочно указывающим путь для поиска новых элементов, - периодическим законом. Все химические свойства неизвестного элемента благодаря этому закону были известны ученым заранее. Так почему же были безуспешны поиски этих трех элементов в природе?

Схема синтеза элемента № 85 - астата
Изучая свойства атомных ядер, физики пришли к выводу: у элементов с атомными номерами 43, 61, 85 и 87 не могут существовать стабильные изотопы. Они могут быть только радиоактивными, с короткими периодами полураспада и должны быстро исчезать. Поэтому все эти элементы были созданы человеком искусственно. Пути для создания новых элементов были указаны периодическим законом. Попробуем с его помощью сами наметить путь синтеза экамарганца. Этот элемент № 43 был первым искусственно созданным.
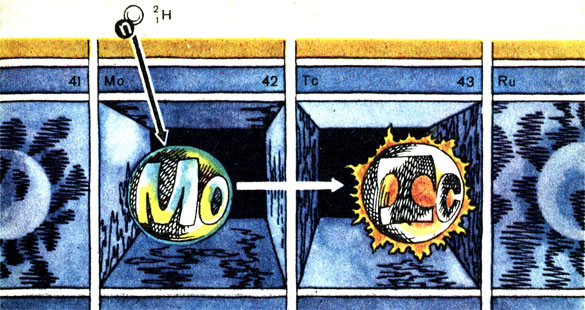
Схема синтеза элемента № 43 - технеция
Химические свойства элемента определяются его электронной оболочкой, а она зависит от заряда атомного ядра. В ядре элемента № 43 должно быть 43 положительных заряда, и вокруг ядра должны вращаться 43 электрона. Как же можно создать элемент с 43 зарядами в атомном ядре? Как можно доказать, что такой элемент создан?
Рассмотрим внимательно, какие элементы в периодической системе располагаются у пустого места, предназначенного для элемента № 43. Оно находится почти в середине пятого периода. На соответствующих местах в четвертом периоде стоит марганец, а в шестом - рений. Поэтому химические свойства 43-го элемента должны быть похожи на свойства марганца и рения. Недаром Д. И. Менделеев, предсказавший этот элемент, назвал его экамарганцем. Слева от 43-ей клетки находится молибден, занимающий клетку 42, справа, в 44-й - рутений.
Следовательно, чтобы создать элемент № 43, необходимо увеличить число зарядов в ядре атома, имеющего 42 заряда, еще на один элементарный заряд. Поэтому для синтеза нового элемента № 43 нужно взять в качестве исходного сырья молибден. У него в ядре как раз 42 заряда. Одним положительным зарядом обладает самый легкий элемент- водород. Итак, можно ожидать, что элемент № 43 может быть получен в результате ядерной реакции между молибденом и водородом.
Свойства элемента № 43 должны быть сходными с химическими свойствами марганца и рения, и, для того чтобы обнаружить и доказать образование этого элемента, нужно воспользоваться химическими реакциями, аналогичными тем, с помощью которых химики определяют присутствие малых количеств марганца и рения. Вот каким образом периодическая система дает возможность наметить путь для создания искусственного элемента.
Точно таким же путем, который мы только что наметили, и был создан в 1937 г. первый искусственный химический элемент. Он получил знаменательное имя- технеций - первый элемент, изготовленный техническим, искусственным путем. Вот как был осуществлен синтез технеция. Пластинка молибдена подвергалась интенсивной бомбардировке ядрами тяжелого изотопа водорода - дейтерия, которые были разогнаны в циклотроне до огромной скорости.
Ядра тяжелого водорода, получившие очень большую энергию, проникли в ядра молибдена. После облучения в циклотроне пластинка молибдена была растворена в кислоте. Из раствора было выделено с помощью тех же реакций, которые необходимы для аналитического определения марганца (аналог элемента № 43), ничтожное количество нового радиоактивного вещества. Это и был новый элемент- технеций. Вскоре были подробно изучены его химические свойства. Они точно соответствуют положению элемента в менделеевской таблице.
Теперь технеций стал вполне доступным: он образуется в довольно больших количествах в атомных реакторах. Технеций хорошо изучен, уже практически используется. С помощью технеция исследуют процесс коррозии металлов.
Метод, каким был создан 61-й элемент, очень похож на метод, которым получают технеций. Элемент №61 должен быть редкоземельным элементом: 61-я клетка находится между неодимом (№ 60) и самарием (№ 62). Новый элемент впервые был получен в 1938 г. в циклотроне бомбардировкой неодима ядрами дейтерия. Химическим путем 61-й элемент был выделен лишь в 1945 г. из осколочных элементов, образующихся в ядерном реакторе в результате деления урана.
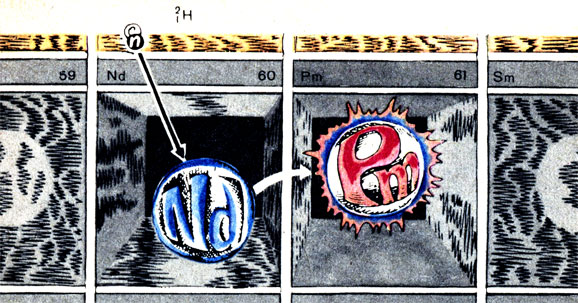
Схема синтеза элемента № 61 - прометия
Элемент получил символическое имя прометий. Это название было дано ему неспроста. Древнегреческий миф рассказывает о том, что титан Прометей похитил с неба огонь и передал его людям. За это он был наказан богами: его приковали к скале, и громадный орел ежедневно терзал его. Название "прометий" не только символизирует драматический путь похищения наукой у природы энергии ядерного деления и овладения этой энергией, но и предостерегает людей от страшной военной опасности.
Прометий теперь получают в немалых количествах: его используют в атомных батарейках- источниках постоянного тока, способных действовать без перерыва несколько лет.
Аналогичным путем был синтезирован и самый тяжелый галоген- экаиод- элемент № 85. Он впервые был получен бомбардировкой висмута (№ 83) ядрами гелия (№ 2), ускоренными в циклотроне до больших энергий.
Ядра гелия, второго элемента в периодической системе, обладают двумя зарядами. Поэтому для синтеза 85-го элемента был взят висмут - 83-й элемент. Новый элемент назван астатом (неустойчивый). Он радиоактивен, быстро исчезает. Его химические свойства также оказались точно соответствующими периодическому закону. Он похож: на иод.
Трансурановые элементы.
Много труда положили химики, разыскивая в природе элементы тяжелее урана. Не раз в научных журналах появлялись торжествующие извещения о "достоверном" открытии нового "тяжелого" элемента с атомной массой большей, чем у урана. Например, элемент № 93 "открывали" в природе многократно, он получал имена "богемий", "секваний". Но эти "открытия" оказывались следствием ошибок. Они характеризуют трудность точного аналитического определения ничтожных следов нового неизвестного элемента с неизученными свойствами.
Результат этих поисков был отрицательным, потому что элементов, соответствующих тем клеткам таблицы Менделеева, которые должны быть расположены за 92-й клеткой, на Земле практически нет.
Первые попытки искусственно получить новые элементы тяжелее урана связаны с одной из замечательных ошибок в истории развития науки. Было замечено, что под влиянием потока нейтронов многие элементы становятся радиоактивными и начинают испускать β-лучи. Ядро атома, потеряв отрицательный заряд, сдвигается в периодической системе на одну клетку вправо, и его порядковый номер становится на единицу больше - происходит превращение элементов. Так под воздействием нейтронов обычно образуются более тяжелые элементы.
Попытались подействовать нейтронами и на уран. Ученые надеялись, что так же, как и у других элементов, у урана при этом появится β-активность и в результате β-распада возникнет новый элемент с номером, на единицу большим. Он-то и займет 93-ю клетку в системе Менделеева. Высказывали предположение, что этот элемент должен быть похож: на рений, поэтому его заранее назвали экарением.

Нейтрон, попадая в ядро урана-235, возбуждает его, в нем возникают сильные колебательные движения, похожие на колебания капли воды
Первые опыты, казалось, сразу же подтвердили такое предположение. Даже больше- обнаружилось, что при этом возникает не один новый элемент, а несколько. Были опубликованы сообщения о пяти новых элементах тяжелее урана. Кроме экарения были "обнаружены" экаосмий, экаиридий, экаплатина и эказолото. И все открытия оказались ошибкой. Но то была амечательная ошибка. Она привела науку к величайшему из достижений физики за всю историю человечества- к открытию деления урана и овладению энергией атомного ядра.

Возбужденное ударом нейтрона ядро урана-235 раскалывается на две части. Получаются два ядра-осколка. Обычно у них разная масса и разные заряды. Так возникают радиоактивные изотопы элементов, находящихся в середине периодической системы. При делении ядра урана-235 из него вылетают два-три новых нейтрона. Каждый из них может вызвать деление нового ядра урана-235
Никаких трансурановых элементов в действительности не было найдено. У странных новых элементов тщетно пытались найти предполагаемые свойства, которыми должны были обладать элементы от экарения да эказолота. И вдруг среди этих элементов неожиданно были обнаружены радиоактивный барий и лантан. Не трансурановые, а самые обычные, но радиоактивные изотопы элементов, места которых находятся в середине периодической системы Менделеева.
Прошло немного времени, и этот неожиданный и очень странный результат был правильно понят.
Почему из атомных ядер урана, стоящего в конце периодической системы элементов, при действии нейтронов образуются ядра элементов, места которых находятся в ее середине? Например, при действии нейтронов на уран возникают элементы, соответствующие следующим клеткам периодической системы:

Много элементов было найдено в невообразимо сложной смеси радиоактивных изотопов, образующихся в уране, облученном нейтронами. Хотя они оказались старыми, давно знакомыми химикам элементами, в то же время это были новые вещества, впервые созданные человеком.
В природе нет радиоактивных изотопов брома, криптона, стронция и многих других из тридцати четырех элементов - от цинка до гадолиния, возникающих при облучении урана.
В науке часто так бывает: самое загадочное и самое сложное оказывается простым и ясным, когда оно разгадано и понято. Когда нейтрон попадает в ядро урана, оно раскалывается, расщепляется на два осколка - на два атомных ядра меньшей массы. Эти осколки могут быть различного размера, поэтому-то и образуется так много различных радиоактивных изотопов обычных химических элементов.
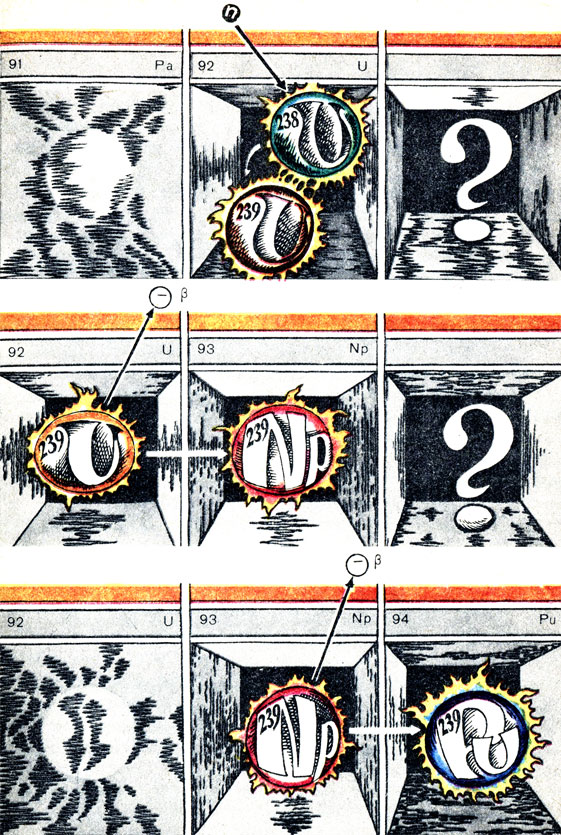
Нейтрон, попавший в ядро урана-238, остается в ядре. Образуется новый изотоп урана - уран-239. Такого урана в природе нет. Это короткоживущий атом, обладающий β -радиоактивностью. При потере одной β-частицы уран-239 превращается в элемент № 93 - нептуний - трансурановый элемент. Нептуний, теряя β-частицу, превращается в плутоний
Одно атомное ядро урана (92) распадается на атомные ядра брома (35) и лантана (57), осколки при расщеплении другого могут оказаться атомными ядрами криптона (36) и бария (56). Сумма атомных номеров образующихся осколочных элементов будет равна 92.
Это было началом цепи великих открытий. Вскоре обнаружили, что под ударом нейтрона возникают из ядра атома урана-235 не только осколки - ядра с меньшей массой, но и вылетают два-три нейтрона. Каждый из них, в свою очередь, способен снова вызвать деление ядра урана. А при каждом таком делении выделяется очень много энергии. Это и стало началом овладения человеком внутриатомной энергией.
Среди огромного множества продуктов, возникающих при облучении ядер урана нейтронами, был впоследствии обнаружен остававшийся долгое время незамеченным первый настоящий трансурановый элемент № 93. Он возникал при действии нейтронов на уран-238. По химическим свойствам он оказался весьма сходным с ураном и совсем не был похож: на рений, как это ожидали при первых попытках синтезировать элементы тяжелее урана. Поэтому его и не могли сразу обнаружить.
Первый созданный человеком элемент, лежащий за пределами "естественной системы химических элементов", был назван нептунием по имени планеты Нептун. Его создание расширило для нас границы, определенные самой природой. Так же и предсказанное открытие планеты Нептун расширило границы наших знаний о Солнечной системе.
Вскоре был синтезирован и 94-й элемент. Он был назван в честь последней планеты. Солнечной системы.
Его назвали плутонием. В периодической системе Менделеева он следует по порядку за нептунием, аналогично "последней планете Солнечной* системы Плутону, орбита которой лежит за орбитой Нептуна. Элемент № 94 возникает из нептуния при его β-распаде.
Плутоний - единственный из трансурановых элементов, который теперь получают в атомных реакторах в очень больших количествах. Так же как и уран-235, он способен делиться под действием нейтронов и применяется как топливо в атомных реакторах.
Элементы № 95 и № 96 носят названия америций и кюрий. Их также получают теперь в атомных реакторах. Оба элемента обладают очень большой радиоактивностью - испускают α-лучи. Радиоактивность этих элементов настолько велика, что концентрированные растворы их солей нагреваются, закипают и очень сильно светятся в темноте.
Все трансурановые элементы - от нептуния до америция и кюрия- были получены в достаточно больших количествах. В чистом виде это металлы серебристого цвета, все они радиоактивны и по химическим свойствам в чем-то похожи друг на друга, а в чем-то заметно различаются.
Был выделен в чистом виде и 97-й элемент - берклий. Для этого пришлось поместить чистый препарат плутония внутрь ядерного реактора, где он целых шесть лет находился под действием мощного потока нейтронов. За это время в нем накопилось несколько микрограммов элемента № 97. Плутоний извлекли из атомного реактора, растворили в кислоте и из смеси выделили наиболее долгоживущий берклий-249. Он сильно радиоактивен - за год распадается наполовину. Пока удалось получить только несколько микрограммов берклия. Но этого количества хватило ученым, чтобы точно изучить его химические свойства.
Очень интересен элемент № 98 - калифорний, шестой после урана. Калифорний впервые был создан посредством бомбардировки мишени из кюрия α-частицами.
Увлекательна история синтеза двух следующих трансурановых элементов: 99-го и 100-го. Впервые они были найдены в облаках и в "грязи". Чтобы изучить, что образуется при термоядерных взрывах, самолет пролетал сквозь взрывное облако, и на бумажные фильтры были собраны пробы осадка. В этом осадке и были найдены следы двух новых элементов. Чтобы получить более точные данные, на месте взрыва собрали большое количество "грязи" - измененной взрывом почвы и горной породы. Эту "грязь" переработали в лаборатории, и из нее выделили два новых элемента. Их назвали эйнштейнием и фермием, в честь ученых А. Эйнштейна и Э. Ферми, которым человечество в первую очередь обязано открытием путей овладения атомной энергией. Эйнштейну принадлежит закон эквивалентности массы и энергии, а Ферми построил первый атомный реактор. Теперь эйнштейний и фермий получают и в лабораториях.
Элементы второй сотни.
Еще не так давно едва ли кто мог поверить, что в таблицу Менделеева будет включен символ сотого элемента.
Искусственный синтез элементов сделал свое дело: на короткое время фермий замкнул список известных химических элементов. Помыслы ученых были теперь устремлены вдаль, к элементам второй сотни.
Но на пути оказался барьер, преодолеть который было нелегко.
До сих пор физики синтезировали новые трансурановые элементы в основном двумя способами. Либо они обстреливали мишени из трансурановых элементов, уже синтезированных, α-частицами и дейтронами. Либо они бомбардировали уран или плутоний мощными потоками нейтронов. В результате образовывались очень богатые нейтронами изотопы этих элементов, которые после нескольких последовательных β-распадов превращались в изотопы новых трансуранов.
Однако в середине 50-х годов обе эти возможности себя исчерпали. В ядерных реакциях удавалось получить невесомые количества эйнштейния и фермия, и потому из них нельзя было изготовить мишени. Нейтронный метод синтеза также не позволял продвинуться дальше фермия, так как изотопы этого элемента подвергались спонтанному делению с гораздо большей вероятностью, чем β-распаду. Понятно, что в таких условиях не имело смысла говорить о синтезе нового элемента.
Поэтому очередной шаг физики сделали только тогда, когда им удалось накопить минимально необходимое для мишени количество элемента № 99. Это случилось в 1955 г.
Одним из самых примечательных достижений, которым по справедливости может гордиться наука, следует назвать создание 101-го элемента.
Этот элемент получил имя великого творца периодической системы химических элементов Дмитрия Ивановича Менделеева.
Менделевий был получен следующим образом. На листочек тончайшей золотой фольги нанесли невидимое покрытие, состоящее приблизительно из одного миллиарда атомов эйнштейния. Альфа-частицы с очень большой энергией, пробивая золотую фольгу с обратной стороны, при соударении с атомами эйнштейния могли вступать в ядерную реакцию. В результате образовались атомы 101-го элемента. При таком соударении атомы менделевия вылетали с поверхности золотой фольги и собирались на другом, расположенном рядом тончайшем золотом листочке. Таким остроумным путем удалось выделить в чистом виде атомы 101-го элемента из сложной смеси эйнштейния и продуктов его распада. Невидимый налет смывался кислотой и подвергался радиохимическому исследованию.
Поистине это было чудом. Исходным материалом для создания 101-го элемента в каждом отдельном опыте служил приблизительно один миллиард атомов эйнштейния. Это очень малозначительно меньше одной миллиардной доли миллиграмма, а получить эйнштейний в большем количестве было невозможно. Заранее подсчитали, что из миллиарда атомов эйнштейния при многочасовой бомбардировке α-частицами может прореагировать всего только один-единственный атом эйнштейния и, следовательно, может образоваться только один атом нового элемента. Нужно было не только суметь его обнаружить, но и сделать это так, чтобы выяснить по одному лишь атому химическую природу элемента.
И это было сделано. Успех опыта превзошел расчеты и ожидания. Удалось заметить при одном эксперименте не один, а даже два атома нового элемента. Всего в первой серии опытов было получено семнадцать атомов менделевия. Этого оказалось достаточно, чтобы установить и факт образования нового элемента, и его место в периодической системе и определить его основные химические и радиоактивные свойства. Оказалось, что это α-активный элемент с периодом полураспада около получаса.
Менделевий - первый элемент второй сотни - оказался своеобразной вехой на пути синтеза трансурановых элементов. До сих пор он остается последним из тех, которые были синтезированы старыми методами - облучением α-частицами. Теперь на сцену вышли более могучие снаряды - ускоренные многозарядные ионы различных элементов. Определение химической природы менделевия по считанному числу его атомов положило начало совершенно новой научной дисциплине - физикохимии единичных атомов.

Схема синтеза тяжелых трансурановых элементов с Z≥lOl
Символ элемента № 102 No - в периодической системе взят в скобки. И в скобках этих заключена долгая и сложная история этого элемента.
О синтезе нобелия сообщила в 1957 г. интернациональная группа физиков, работавших в Нобелевском институте (Стокгольм). Впервые для синтеза нового элемента были применены тяжелые ускоренные ионы. В их качестве выступили ионы 13С, поток которых направлялся на кюриевую мишень. Исследователи пришли к выводу, что им удалось синтезировать изотоп 102-го элемента. Ему дали название в честь основателя Нобелевского института изобретателя динамита Альфреда Нобеля.
Прошел год, и опыты стокгольмских физиков были воспроизведены почти одновременно в Советском Союзе и США. И выяснилась удивительная вещь: результаты советских и американских ученых не имели ничего общего ни с работами Нобелевского института, ни между собой. Никому и нигде более не удалось повторить эксперименты, проведенные в Швеции. Такая ситуация породила довольно грустную шутку: "От нобелия остался один No" (No - в переводе с английского означает "нет"). Символ, поспешно помещенный в менделеевскую таблицу, не отражал действительного открытия элемента.
Достоверный синтез элемента № 102 совершила группа физиков из Лаборатории ядерных реакций Объединенного института ядерных исследований. В 1962-1967 гг. советские ученые синтезировали несколько изотопов элемента № 102 и изучили его свойства. Подтверждение этих данных было получено в США. Однако символ No, не имея на то никакого права, до сих пор находится в 102-й клетке таблицы.
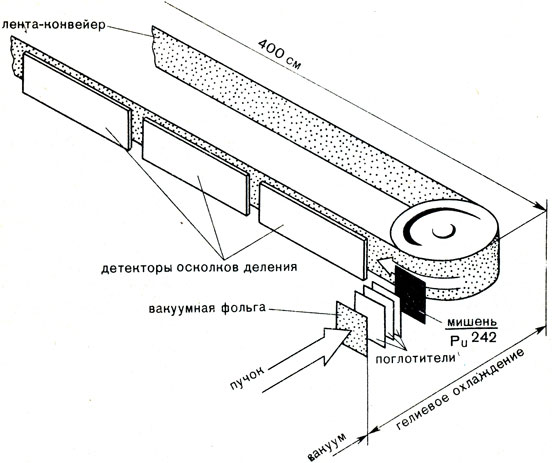
Схема устройства, применявшегося в опытах по синтезу курчатовия
Лоуренсий, элемент № 103 с символом Lw, названный так в честь изобретателя циклотрона Э. Лоуренса, был синтезирован в 1961 г. в США. Но здесь не меньшая заслуга и советских физиков. Они получили несколько новых изотопов лоуренсия и впервые изучили свойства этого элемента. Лоуренсий также появился на свет благодаря использованию тяжелых ионов. Мишень из калифорния облучалась ионами бора (или америциевая мишень - ионами кислорода).
Элемент № 104 впервые был получен советскими физиками в 1964 г. К его синтезу приводила бомбардировка плутония ионами неона. 104-й элемент получил название курчатовия (символ Ки) в честь выдающегося советского физика Игоря Васильевича Курчатова.
105-й и 106-й элементы также впервые удалось синтезировать советским ученым - в 1970 и в 1974 гг. Первый из них- продукт бомбардировки америция ионами неона- был назван нильсборием (Ns) в честь Нильса Бора. Синтез другого осуществлялся следующим образом: мишень из свинца бомбардировалась ионами хрома. Синтезы 105-го и 106-го элементов были осуществлены также и в США.
А что дальше? Будут ли получены элементы с большими порядковыми номерами? Имеет ли предел искусственный синтез новых элементов?
Вы узнаете об этом в следующей главе, а настоящую мы завершим кратким рассказом о том,
как изучают свойства элементов второй сотни.
Фантастически трудная задача стоит перед экспериментаторами.
Вот ее исходные условия: даны считанные количества (десятки, в лучшем случае сотни) атомов нового элемента, причем атомов весьма короткоживущих (периоды полураспада измеряются секундами, а то и долями секунды). Требуется доказать, что эти атомы - атомы действительно нового элемента (т. е. определить значение Z, а также величину массового числа А, чтобы знать, о каком изотопе нового трансурана идет речь), и изучить его важнейшие химические свойства.
Считанные атомы, ничтожная продолжительность жизни...
На помощь ученым приходят быстрота и высочайшая изобретательность. Но современный исследователь - специалист по синтезу новых элементов - должен не только уметь "подковать блоху". Он должен и в совершенстве владеть теорией.
Проследим за теми основными шагами, посредством которых производят идентификацию нового элемента.
Важнейшей визитной карточкой в первую очередь служат радиоактивные свойства- это может быть испускание α-частиц или спонтанное деление. Каждое α-активное ядро характеризуется специфическими величинами энергии α-частиц. Это обстоятельство позволяет либо опознать известные ядра, либо сделать вывод о том, что обнаружены новые. Например, изучая особенности α-частиц, ученые сумели получить достоверное доказательство синтеза 102-го и 103-го элементов.
Энергичные осколочные ядра, образующиеся в результате деления, обнаружить значительно легче, чем α-частицы, вследствие гораздо большей энергии осколков. Для их регистрации употребляются пластинки, сделанные из стекла специального сорта. Осколки оставляют на поверхности пластинок чуть заметные следы. Затем пластинки проходят химическую обработку (травление), и их внимательно рассматривают под микроскопом. Стекло растворяется в плавиковой кислоте.
Если стеклянную пластинку, обстрелянную осколками, поместить в раствор плавиковой кислоты, то в местах, куда попали осколки, стекло будет растворяться быстрее и там образуются лунки. Их размеры в сотни раз больше первоначального следа, оставленного осколком. Лунки можно наблюдать в микроскоп со слабым увеличением. Другие радиоактивные излучения наносят поверхности стекла меньшие повреждения и не просматриваются после травления.
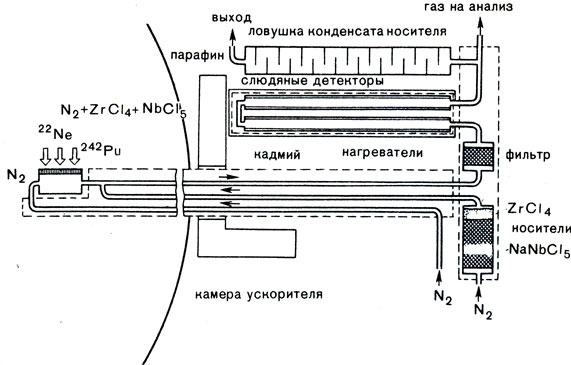
Схема установки, позволяющей изучать химическую природу единичных атомов. На этой установке было показано, что курчатовий - аналог гафния, а нильсборий - тантала
Вот что рассказывают авторы синтеза курчатовия о том, как происходил процесс опознания нового элемента: "Идет опыт. Сорок часов беспрерывно бомбардируют ядра неона плутониевую мишень. Сорок часов лента несет синтетические ядра к стеклянным пластинкам. Наконец циклотрон выключен. Стеклянные пластинки переданы на обработку в лабораторию. С нетерпением ждем результата. Проходит несколько часов. Под микроскопом обнаружено шесть треков. По их положению вычислили период полураспада. Он оказался в интервале времени от 0,1 до 0,5 с.
А вот как те же исследователи рассказывают об оценке химической природы курчатовия и нильсбория. "Схема исследования химических свойств элемента № 104 такова. Атомы отдачи выходят из мишени в струю азота, тормозятся в ней, а затем хлорируются. Соединения 104-го элемента с хлором легко проникают через специальный фильтр, а все актиноиды не проходят. Если 104-й принадлежал бы к актиноидному ряду, то и он бы задержался фильтром. Однако исследования показали, что 104-й элемент - это химический аналог гафния. Это важнейший шаг к заполнению таблицы Менделеева новыми элементами.
Затем в Дубне были изучены химические свойства 105-го элемента. Оказалось, что его хлориды адсорбируются на поверхности трубки, по которой они движутся от мишени при температуре более низкой, чем хлориды гафния, но более высокой, чем хлориды ниобия. Так могли бы вести себя только атомы элемента, близкого по химическим свойствам к танталу. Посмотрите на таблицу Менделеева: химический аналог тантала - элемент № 105! Поэтому опыты по адсорбции на поверхности атомов 105-го элемента подтвердили, что его свойства совпадают с предсказанными на основе периодической системы".
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'