
Соли
К учебным задачам преподавания по данной теме относятся: 1) приведение в систему знаний, полученных учащимися о солях на предыдущих занятиях; 2) закрепление знаний и умений читать формулы солей и составлять эти формулы, если известны валентности металлов и кислотных остатков; 3) изучение химических свойств солей.
Так как учащиеся знают, что называется кислотным остатком, то представляется возможным формулировать определение солей так: соли - сложные вещества, молекулы которых состоит из атомов металлов, соединенных с кислотными остатками. В качестве упражнения в усвоении названия и составлении формул солей можно предложить учащимся выполнить самостоятельную работу по следующему заданию: "Прочитайте § 57 о составе солей и напишите названия и формулы солей четырех кислот, указанных в таблице, и трех металлов: калия, кальция и алюминия. Запись сделайте в форме таблицы".

Таблица14. Состав и название солей
Химические свойства солей. Изучение химических свойств солей можно начать с реакций разложения и замещения солей. Например, разложение углекислого магния учащиеся выполняют без затруднений, а с разложением углекислого кальция учащиеся знакомятся при изучении производства извести.
Примером реакции замещения может служить известная им реакция, происходящая между сернокислой медью и железом. Опыт легко организовать с целью получения более или менее значительных количеств железного купороса.
В связи с разбором механизма этой реакции учащиеся знакомятся с электрохимическим рядом напряжений металлов. В заключение этой работы учащиеся решают текстовые задачи на развитие умений применять эти знания для осуществления реакций замещения, происходящих в растворах.
Классификация и генетическая связь. Большое значение для усвоения пройденной темы имеет правильное повторение и упражнения в применении знаний. Повторение в данном случае особенно эффективно проходит, если применяется самостоятельная работа. Учащимся предлагают составить таблицу, а затем заполнить ее, пользуясь учебником и записями в своих тетрадях - отчетами.
Выявление генетической связи между элементами, окислами, - кислотами, основаниями и солями целесообразно провести методом беседы с демонстрациями опытов - окисление металла, гидратация окисла, горение неметалла, гидратация окисла. Затем следует анализ соответствующей таблицы - схемы генетической связи. Чтобы эти знания приобрели большую научную и практическую значимость, необходимо решить ряд химических задач, требующих предвидения фактов на основе этих знаний, например:
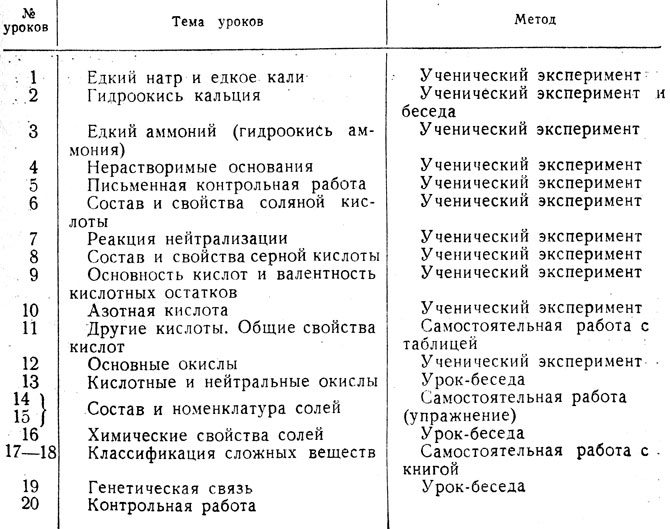
Таблица 15. План обучения по теме 'Окислы. Основания. Кислоты. Соли'
1. На раствор неизвестного вещества подействовали едким кали. После выпаривания получили вещество, имеющее формулу КСl. С какими из указанных ниже веществ это вещество должно реагировать: Сu, Mg, CaO, SiО2, NaOH?
2. Неизвестный окисел реагирует с серной кислотой. К какому классу относится его гидрат? С какими из указанных веществ он реагирует: HNО3, КОН, CuO? Напишите уравнение реакций.
3. Окисел ХО растворяется в воде. Лакмус в этом растворе имеет синий цвет. С какими из указанных веществ этот окисел может реагировать: Са(ОН)2, H2SО4, НСl, NaCl? Напишите уравнения реакций.
4. Зная валентность магния, напишите формулы его окиси, гидроокиси и сернокислого магния.
5. Вещество, имеющее формулу Н3ВО3, - кислота. Напишите формулу ее ангидрида и натриевой соли.
На основании многолетнего опыта учителей можно рекомендовать другой план и другие методы обучения по рассмотренной теме.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'