
Пневматическая ванна и газовый анализ
Анализ с помощью паяльной трубки сыграл важную роль в накоплении химических знаний в конце XVIII в.- в фазе, которая привела к формированию "классической химии". Однако значение газового анализа для развития химии было несравнимо больше. При работе с газами ученые испытывали значительные трудности: газы были осязаемы, но неуловимы. Некоторое время их пытались изучать с помощью сосудов для перегонки и сублимации, где вещества небольшое время находились в газообразном состоянии, прежде чем перейти в жидкое. Но лишь в XVIII в., когда была открыта пневматическая ванна, началось систематическое исследование газообразных веществ. На основе этих экспериментов Лавуазье получил много новых данных о протекании окислительных превращений, переосмыслил уже известные факты и пришел к созданию кислородной теории горения.
Некоторые историки считают, что приверженностью химиков XVII-XVIII в. учению о четырех первичных элементах Аристотеля можно объяснить, почему исследователи практически не занимались установлением природы и выяснением свойств газов. Ведь воздух считался одним из первичных, неделимых элементов. Это рассуждение можно отнести также и к "воде", и к "земле". Вода была изучена, пожалуй, раньше всех других веществ, но различные свойства железистых, сернистых или кальциевых минеральных вод отнюдь не мешали химикам вплоть до середины XVIII в. рассматривать воду как самостоятельный "элемент".
Нельзя забывать, что понятие "элемент" в те времена было совсем иным, чем сейчас, и уже в античности элемент характеризовался определенной совокупностью качеств (горючий, воздухоподобный, твердый, жидкий). Поэтому широкая трактовка понятия "элемент" едва ли была препятствием для изучения газообразных веществ. Так, античные натурфилософы, называя воздухом газообразные вещества, тем не менее различали по свойствам разнообразные виды воздуха. В то время ремесленники хорошо знали свойства таких газообразных веществ, как сернистый газ, углекислый газ, образующийся при брожении продуктов или при горении извести, а также при смешивании уксуса и мела. Было известно, что при вдыхании угарного газа наступает удушье, нередко приводящее к смерти. Каждому виноделу в древности было известно, что в подвалах, где хранят вино, гаснут свечи, а кошки не могут ловить мышей. Еще Плиний различал два вида воздуха в зависимости от свойств, проявляемых по отношению к огню: один из видов воздуха усиливал горение, другой гасил огонь.
С тех пор как в лабораториях начали применять неорганические кислоты, были открыты новые свойства газов. Например, еще Парацельс заметил, что, если добавить концентрированную серную кислоту к железу, появляются пузырьки "воздуха", как при кипении. Парацельс, для которого воздух был символом хаотического состояния материи, назвал его "хаос". Поэтому иатрохимик Ван Гельмонт, который много занимался исследованиями газообразных веществ, предложил для их общего наименования термин "газ". Ван Гельмонт (1577-1644) отмечал трудности, с которыми столкнулся при изучении газообразных веществ: газы легко улетучивались и испарялись. Поэтому Ван Гельмонт исследовал лишь углекислый газ и описал появление этого вещества при горении, а также брожении. Это же вещество, по мнению Ван Гельмонта, выделяется из минеральных вод и из организма человека.
Задолго до начала систематического исследования газов в XVIII в. свойства газов стали широко известны в результате опытов над атмосферным воздухом, проведенных Эванджелиста Торричелли (1608-1647), Отто Герике (1602-1686), Робертом Бойлем (1627-1691) и Эдмом Мариоттом (1620-1684). В 1643 г. Торричелли доказал, что воздух производит давление, и измерил величину этого давления. В 1641 г. Герике изобрел воздушный насос, а в 1654 г. он продемонстрировал перед городским советом Регенсбурга свой знаменитый опыт с "магдебургскими полушариями", доказав громадную силу воздушного давления. В 1662 г. Бойль обнаружил существование зависимости между объемом воздуха и изменением его давления. В 1679 г. Мариотт выразил эту зависимость формулой pv = const. Так появился известный закон Бойля - Мариотта.
Однако опыты, выполненные Бойлем, не привели его к мысли, что воздух и газы могут участвовать в химических процессах. Наблюдаемое Бойлем увеличение веса [массы] металлов при прокаливании (окислении) навело его на мысль о существовании "огненных частиц", тогда как еще до опытов Бойля Жан Рей в 1630 г. и позднее Джон Мэйоу (1645-1679), а в XVIII в. М. В. Ломоносов пришли к предположению о существовании "воздушных частиц". Неверное допущение, будто воздух или газы, понимаемые как воплощение некоего "духа", не могут участвовать в реакциях, способствовало тому, что даже такой выдающийся ученый, как Георг Эрнст Шталь, объяснял процессы восстановления и окисления с помощью гипотетического вещества - "флогистона". Лишь во второй половине XVIII в. исследователи пришли к выводу, что газы, подобно другим жидким и твердым веществам, могут участвовать в различных реакциях.
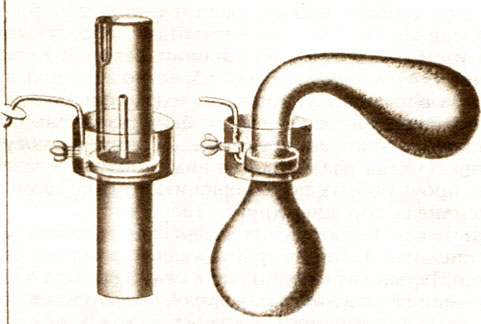
Первый аппарат для перегонки в вакууме, сконструированный Р. Бойлем (XVII в.)
В свое время Роберт Бойль и Джон Мэйоу описывали один из видов пневматической ванны - заполненную смесью воды и серной кислоты стеклянную колбу, в которой помещены железные гвозди. Для улавливания выделяющихся при реакции газов перевернутая стеклянная колба погружается в сосуд с водой.
Другие ученые, например Христофер Врен (1632-1679) и позже Карл Вильгельм Шееле (1742-1786), использовали для улавливания газов дыхательные пузыри крупных рыб. Лишь необычайные способности Шееле к проведению экспериментов позволили ему с помощью этой примитивной техники совершить такие выдающиеся открытия, как обнаружение кислорода (1772 г.), хлора (1774 г.), сероводорода (1776 г.).
Важнейшим "инструментом" для проведения газового анализа была пневматическая ванна, описанная С. Гейлсом в 1727 г. В пневматической ванне Гейлс получал газы из угля, жира, оксидов, известняка. При этом его интересовала не природа образующихся газов, а лишь горючесть этих веществ. Только Джозеф Блэк (1728-1799) смог впервые отличить углекислый газ от атмосферного воздуха. Блэк называл этот газ "фиксированным" (т. е. связанным) воздухом, так так получил его (в 1755 г.) из карбоната магния. Блэк открыл также реакцию поглощения углекислого газа "известковой водой". Отсюда возникло представление, что благодаря определенным воздействиям можно выделить отдельные газы из их смесей. Этот опыт явился важнейшей предпосылкой для возникновения газового анализа. Кроме того, Блэк обнаружил возможность определения веса [массы] газообразных веществ при рассмотрении их соединений, находящихся в твердом состоянии.
Джозеф Пристли (1733-1804) превратил пневматическую ванну в незаменимое устройство для химического исследования, после того как открыл способность некоторых газов поглощаться водой. (Торберн Бергман тоже обнаружил, что углекислый газ может растворяться в воде и имеет кислый характер, почему и называл этот газ "воздушной кислотой".) С помощью усовершенствованной им пневматической ванны (с ртутным затвором) Пристли после Шееле (1772 г.), но независимо от него открыл кислород, а, кроме того, в 1773-1776 гг. изучил "веселящий газ", хлороводород, сернистый газ и аммиак.
В 1766 г. Генри Кавендиш (1731-1810) открыл водород*, а в 1772 г. Даниэль Резерфорд (1749-1819) - азот. В книге "Эксперименты с воздухом" (1784 г.) Кавендиш описал и другие свои достижения в области экспериментальной химии: разработанные им способы определения плотности газов, в частности углекислого газа и водорода, выяснение состава атмосферного воздуха и воды. Таким образом, было сделано важнейшее в истории химии открытие - показано, что при соединении водорода и кислорода, содержащегося в воздухе, может образовываться вода, которую в то время многие ученые еще считали "элементом". (Лишь десятью годами ранее на основе эксперимента Лавуазье удалось опровергнуть считавшееся непреложным утверждение, будто воду можно превратить в землю!)
* (Поскольку Кавендиш не смог понять природу изученного им в то время газа, некоторые историки химии не приписывают ему открытие водорода. См. Трифонов Д. Н., Трифонов В. Д. Как были открыты химические элементы.- М.: Просвещение, 1980, с. 37-39.- Прим. перев.)
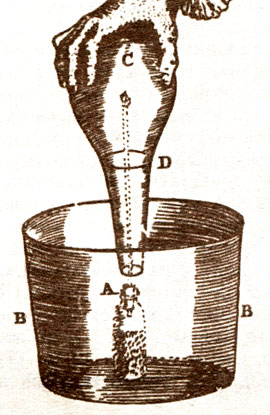
Сгорание водорода (полученного при смешивании железных или цинковых опилок с серной кислотой) в закрытом объеме воздуха
В своих исследованиях Кавендиш применил новый метод, который значительно обогатил "экспериментальное искусство",- действие электрического разряда на смеси газов, в частности на смесь водорода и кислорода. При этом образовывалась вода. При пропускании электрических разрядов через атмосферный воздух Кавендиш использовал изогнутую стеклянную трубку, концы которой были погружены в стеклянные сосуды ("рюмки") со ртутью*. В 1785 г. Кавендиш обратил внимание на пузырьки "остаточного воздуха" (1/120 первоначального объема), который не изменялся под действием электричества. Лишь в 1894 г. Уильям Рэлей установил, что "остаточек ных воздух" - это инертный газ.
* (При этом получались также оксиды азота, свойства которых изучал Кавендиш. Впоследствии такой способ получения оксидов азота широко использовался в лабораторной практике.- Прим. перев.)
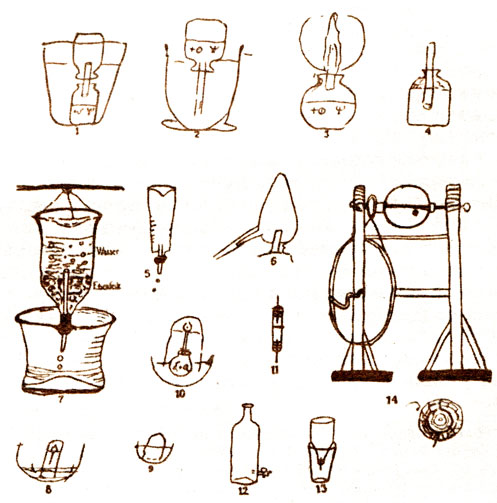
Химические аппараты (из рукописей К. В. Шееле)
Факты, полученные при изучении газообразных веществ, легли в основу созданных Антуаном Лораном Лавуазье новых представлений о протекании окислительно-восстановительных процессов. Лавуазье был не только выдающимся теоретиком, но и замечательным экспериментатором. В 1770-х - начале 1780-х гг. он определял количества оксида углерода, образующиеся при сгорании угля и углеродсодержащих "горючих тел". В 1784 г. Лавуазье показал, что при пропускании водяного пара через раскаленную железную трубку образуется водород. Практически одновременно Кавендишу удалось осуществить синтез воды из элементов, а Лавуазье разработал способ ее разложения.
Совершенно неверным является утверждение некоторых историков химии будто для создания своей антифлогистонной теории Лавуазье использовал данные экспериментов лишь других исследователей. Кроме открытий Лавуазье, о которых мы рассказывали, следует подчеркнуть еще одну сторону его творчества, оказавшую громадное влияние на развитие химии: ученый систематически применял взвешивание для контроля за протеканием превращений и как "средство познания". При этом наибольшей заслугой Лавуазье в совершенствовании естественнонаучных знаний было окончательное экспериментальное обоснование закона сохранения веса (массы). Вместе с тем не следует утверждать, что лишь Лавуазье ввел весы в экспериментальную химическую практику; они использовались химиками задолго до Лавуазье [93, с. 105 и сл.].
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'