
Вездесущий водород
Подойдя к рубежу термостойкости 450-500° С, исследователи словно бы уперлись в невидимый барьер. Никакие ухищрения - усложнения структуры, замены атомов углерода в главной цепи и т. п. - не помогали. В тщательно продуманных схемах что-то не срабатывало. Пришлось еще более детально, еще более фундаментально заняться изучением механизма, в частности, химизма процессов термической деструкции полимеров. Пришлось синтезировать десятки и сотни новых полимеров, таких, которые вряд ли когда найдут практическое применение, вряд ли дойдут до уровня промышленного производства. Но зато в качестве модельных соединений, в качестве рабочего исследовательского инструмента они незаменимы. Именно синтез и изучение свойств таких моделей и составляют основу любых фундаментальных исследований.
Как правило, побочные результаты таких исследований потом оказываются в умелых руках основой для развития целых новых отраслей. Так было и в этом случае. Изучая проблему термостойкости, ученые порой наталкивались на совершенно новые свойства полимеров, на совершенно новые явления. Например, именно так были обнаружены полимеры со свойствами полупроводников. Так были найдены новые подходы к решению проблемы защиты полимерных материалов от действия огня. Были разработаны некоторые принципиально новые методы синтеза полимеров, например, метод изомеризационной циклизации. Но главное не в этом. Решающим для решения проблемы термостойкости оказалось то, что в ходе этих исследований были разработаны и освоены многие новые методы изучения свойств веществ.
Не надо думать, что исследователям удалось изобрести заново множество новых методов. Речь идет скорее об освоении методического богатства смежных областей. Например, метод хроматографии был изобретен М. С. Цветом в 1903 г. для разделения природных красящих веществ, в первую очередь хлорофиллов. Позже этот метод использовался для анализа жиров, аминокислот, витаминов и т. д. Полимерщикам этот метод помог разобраться в составе продуктов термодеструкции. Метод термогравиметрии был известен в XVII в., еще М. В. Ломоносов пользовался им для опровержения теории флогистона. Полимерщики использовали этот метод для выявления количественных закономерностей Процессов термодеструкции. И так далее.
Только тогда, когда комплекс всех этих методов, включая, конечно, и химический анализ, и математическую обработку результатов исследований на ЭВМ (без чего, например, немыслим метод масс-спектрометрии), был использован при решении проблемы термостойкости, лишь тогда стала выясняться природа этого таинственного 500-градусного порога на пути полимеров к еще большей термостойкости.
Здесь, пожалуй, уместно остановиться на том, как именно исследователи выясняют тайные механизмы сложных реакций. Работа обычно ведется в двух философски противоположных и взаимодополняющих направлениях. Анализ и синтез - основа основ. Если же говорить о механизме процессов термической деструкции полимеров, то тут дело осложняется еще и разнообразием продуктов, образующихся при этом. Уникальна термодеструкция фторопласта-4-политетрафторэтилена - он целиком деполимеризуется до исходного мономера, тетрафторэтилена, F2C-CF2. Почти у всех других полимеров, особенно у термостойких, деструкция приводит к смеси многих разных продуктов. Обычно их разделяют на летучие, низкомолекулярные, и нелетучие, коксовый остаток. Летучие в большинстве случаев удается, по крайней мере это стараются сделать, разделить на индивидуальные вещества, определить точный состав, а затем и химическую структуру каждого. Попутно приходится решать еще более сложный вопрос: как влияют условия проведения процесса деструкции на выход каждого из этих продуктов? Вдобавок при этом приходится учитывать, что многие из образующихся соединений способны вступать в химическое взаимодействие друг с другом. Так что к обширному набору первичных продуктов термодеструкции добавляется еще более обширный набор вторичных.
Коксовый остаток - чаще всего это бурый или черный, неплавкий и ни в чем не растворимый хрупкий порошок или спекшаяся смола непостоянного состава; так же непостоянны и его свойства. Условия проведения процесса влияют и па него; и для него возможны вторичные реакции. И наконец, последняя сложность: и состав, и свойства всех продуктов зависят от того, на каком размере исходного образца, в какой атмосфере, при каком давлении и в какой посуде проводился процесс. Систематический анализ сотен графиков, полученных для одного полимера, - труд титанический, и здесь знаний и опыта мало, нужны еще творческое воображение и даже интуиция.
Фигурально говоря, работа химика-исследователя по сути своей аналогична работе детектива столь любимых широкой публикой - Шерлока Холмса, комиссара Мегрэ, Эркюля Пуаро и других. В химии особенно наглядно проявляется это сходство, когда мы знакомимся с изучением механизмов термодеструкции полимеров. Как в любом детективном романе, здесь с определенного момента становится ясно, что преступление (т. е. разрушение макромолекулы) совершает некий агент (реагент). Сложное переплетение первичных и вторичных химических продуктов, сложные характеры каждого из действующих лиц драмы, непостоянство химического состава летучих и нелетучих продуктов - все это затрудняло поиск главного виновника. Но в то же время с определенного этапа расследования становилось ясно, что косвенных улик уже более чем достаточно, надо только в них разобраться.
Оставалось сесть за стол, закурить любимую трубку, "взять голову в руки" и распутать дело, обобщив и систематизировав все данные. В роли майора Пронина в этой ситуации выступил тогда кандидат химических наук, ныне член-корреспондент АН СССР А. Н. Праведников.
Работа развивалась так. Во-первых, известно, что процессы термодеструкции почти всех полимеров многостадийны. Для тех стадий, которые удалось экспериментально выявить и доказать, энергии активации равны 30-70 ккал/моль, а для процесса в целом они обычно оказывались намного меньшими - 15-25 ккал/моль. Такое поведение характерно для процессов с передачей кинетической цепи. Но кто же в данном случае может служить агентом передачи цепи? Поскольку процесс идет в конденсированной фазе, а развивается довольно быстро в любом микроскопическом объеме материала, этот зловредный агент должен обладать большой проникающей силой с высокой химической активностью.
Большая проникающая сила - значит, наиболее вероятно, - что у агента очень мелкие молекулы. Его самого или продукты его вторичных превращений следует искать среди летучих продуктов.
Высокая химическая активность - значит, до конечных стадий процесса сам агент не дойдет, превратится в нечто более устойчивое, менее реакционноспособное.
Вывод. Чтобы выявить главного виновника цепного характера процессов термической деструкции полимеров, надо сопоставить состав летучих продуктов деструкции большинства исследованных полимеров и выявить, что в них одинаково. Одним из таких общих летучих продуктов, к тому же самым мелким, оказался водород.
Напомним, что речь идет об органических полимерах. Органическую химию иногда называют химией соединений углерода. Это верно: уникальная способность атомов углерода соединяться друг с другом в сколь угодно длинные и разветвленные химические структуры и оправдывает обособление органических веществ. Но в какой-то мере органическую химию можно называть и химией углеводородов. Почти во всех органических соединениях присутствует С-Н группировка. Есть она и почти во всех, в том числе и в термостойких, полимерах. Поэтому считалось само собой разумеющимся, что при термической деструкции полимеров в составе летучих продуктов обнаруживается водород. Хотя и в небольших количествах, но его почти без исключений находили всегда. И не придавали этому особого значения. Лишь А. Н. Праведников, соединив чисто химический подход к проблеме повышения термостойкости с подходом физико-химическим, понял, что водород может и должен играть в этих процессах особую роль - роль Агента передачи цепи. Но не молекулярный водород Н2 - он для такой роли недостаточно активен, а водород атомарный, Н! Именно он обладает уникальной всепроникающей способностью. Даже сквозь металлы он может просачиваться, что уж там говорить о слое разлагающегося полимера. Именно он обладает такой высокой реакционной способностью, что может инициировать разложение любой органической молекулы. И в то же время он отлично законспирирован: в атомарной форме водород может существовать лишь ничтожно малые отрезки времени. Потом он либо вступает в реакции с соседними молекулами, либо превращается в молекулы Н2 и выходит из игры под внешне безобидной маской ничтожной примеси в составе летучих продуктов.
Тщательный расчет подтвердил, что такая роль вполне по силам атомарному водороду даже при ничтожном его содержании. Логично было проверить на модельных соединениях, а что даст полное устранение водорода от участия в деструктивных процессах. Синтез соответствующих соединений, совсем не содержащих водорода, и испытание их термической стабильности убедительно и однозначно подтвердили, что преодолен тот порог термостойкости, о котором говорилось в начале этого параграфа. Так, например, полимер с такой химической структурой главных звеньев макромолекулы
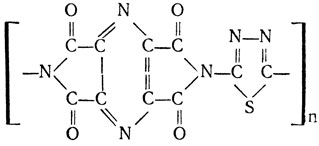
оказался термостойким выше 600° С. Вдобавок, как это уже неоднократно бывало в истории химии, теперь стало ясно, почему самый термостойкий из известных на сегодня органический полимер черный орлон способен без разрушения выдерживать температуры до 1000° С. Ведь черный орлон - это пиролизованный по особой методике полиакрилонитрил. На стадиях пиролиза и карбонизации, проводимых при повышенных температурах в атмосфере, содержащей следы кислорода, происходило именно "выжигание" остатков водорода из лестничных гетероциклических макромолекул этого полимера. Таким образом ученые смогли сделать еще один шаг по пути повышения термической стабильности органических полимеров. (Химия и жизнь, 1982, № 1).
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'