
7.2. Приближение Борна - Оппенгеймера
Гамильтониан для системы ядер (обозначаемых здесь греческими буквами (μ, ν ...) с координатами X и электронов (обозначаемых латинскими буквами i, j, k ...) с координатами х имеет следующий вид:
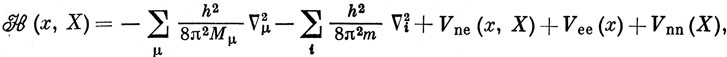
где Vee, например, представляет собой межэлектронное отталкивание:
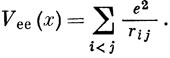
Если выделить кинетическую энергию ядер,
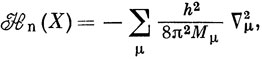
то разность
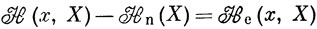
представляет собой гамильтониан, описывающий движение электронов при фиксированных ядрах. Заметим, что He зависит только от координат, но не от импульсов ядер.
Предположим теперь, что полная волновая функция, являющаяся решением уравнения
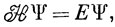
может быть представлена в виде
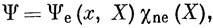
где "электронная" волновая функция удовлетворяет уравнению
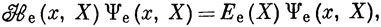
а ядерная волновая функция - уравнению
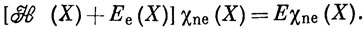
Система этих двух уравнений соответствует приближению Борна - Оппенгеймера *).
*) (Такое приближение часто называют также адиабатическим приближением. - Прим. перев.)
Каков же смысл этих уравнений? Прежде всего в них содержится предположение, что полная волновая функция молекулы может быть представлена в виде произведения электронной функции на ядерную. Электронная волновая функция получается при решении уравнения (7.13) для различных конфигураций ядер. Это дает также электронную энергию Ее, которую для двухатомной молекулы (X в этом случае есть межъядерное расстояние) можно представить графически, как это сделано на рис. 5.1. Эта электронная энергия рассматривается далее в качестве потенциальной энергии в уравнении, определяющем движение ядер, так что уравнение Шредингера имеет вид (7.14). Его решения χne (X) не зависят от электронных координат, но зависят от характера электронного состояния, так как последнее определяет форму потенциальных кривых. Каждому электронному состоянию Ψе соответствует свой набор ядерных волновых функций.
Электронная энергия не является наблюдаемой величиной, хотя и может быть вычислена. Обычно полную энергию представляют в виде суммы электронной энергии, вычисленной при равновесной конфигурации ядер, и ядерной энергии
Е = Ее(Х0) + Еn. (7.15)
Таким образом, электронная и ядерная энергии могут быть разделены в выражении для полной энергии.
Спектроскопия дает убедительное подтверждение того, что в общем приближение Борна - Оппенгеймера является достаточно хорошим. В инфракрасных спектрах наблюдаются переходы между различными колебательными уровнями основного электронного состояния; соответствующая картина колебательного спектра может быть выражена через волновые функции χne и энергии Еn, определенные выше. В видимой и ультрафиолетовой областях спектра наблюдаются переходы между различными электронными уровнями, так что результирующий спектр содержит структуры, возникающие из различных колебательных компонент рассматриваемых электронных состояний. Расположение этих колебательных структур и относительные интенсивности их отдельных компонент могут быть объяснены также на основе рассмотренных выше уравнений.
Теперь обсудим условия, при которых справедливо приближение Борна - Оппенгеймера. Подставляя уравнения (7.10) и (7.12) в уравнение (7.11), можно получить
[He (x, X) + Hn (X)] Ψе (x, X) χne(X) = ЕΨе(x, X) χne(X). (7.16)
Оператор He содержит дифференцирование только по электронным координатам х и поэтому, используя уравнение (7.13), можно написать
He(x, Х) Ψе(х, Х) χne(Х) = χne(Х) He(х, Х) Ψe(х, Х) = = χne(Х) Ее(Х) Ψе(х, X). (7.17)
Оператор Hn - оператор дифференцирования по ядерным координатам X, от которых зависит как χne, так и Ψe; следовательно, применяя выражение (7.9), получим
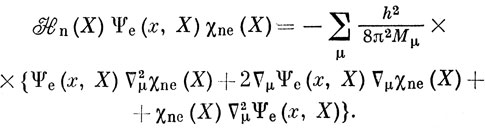
Подставляя уравнения (7.17) и (7.18) в уравнение (7.16)" мы приходим к уравнению (7.14) для ядерной волновой функции, если можно пренебречь членами ∇μΨe и ∇μ2Ψе в уравнении (7.18). Иначе говоря, приближение Борна - Оппенгеймера справедливо, если электронная волновая функция Ψe есть медленно меняющаяся функция ядерных координат. Единственный случай, когда приближение Борна - Оппенгеймера, по-видимому, непригодно - это наличие вырожденных или почти вырожденных электронных состояний. В таких случаях члены ∇μΨe, которыми пренебрегают в приближении Борна - Оппенгеймера, приведут к заметному взаимодействию между двумя вырожденными или почти вырожденными электронными состояниями, и только одна волновая функция типа (7.12) не даст хорошего описания системы.
В этой книге рассматриваются методы вычисления только электронной волновой функции Ψе и электронной энергии Ее. По этой причине в дальнейшем под волновой функцией, энергией или гамильтонианом мы будем подразумевать соответствующие электронные величины, хотя и не будем писать в каждом случае значок "е".
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'