
14.3. Многогранники, образованные атомами бора
Среди боридов, образуемых многими электроположительными элементами, имеются интересные примеры соединений с электронным дефицитом. Например, в СаВ6 шесть атомов бора расположены в форме октаэдра, каждая вершина которого связана с соседним октаэдром, и атомы бора образуют гигантский анион, простирающийся по всему кристаллу. Ионы кальция расположены между этими октаэдрами, образуя решетку типа NaCl.
Обсуждение МО октаэдров В6 весьма сходно с тем, которое было проведено для МО лигандов в октаэдрическом комплексе (гл. 13). Должны быть внесены два основных изменения. Во-первых, нужно включить 2s-орбитали каждого из атомов бора; они преобразуются подобно а-орбиталям лигандов для неподеленных пар электронов в октаэдрическом комплексе (то есть по представлению А1g + Eg + T1u). Во-вторых, необходимо учесть перекрывание волновых функций атомов бора. Орбитали 2s и 2рσ атома бора смешиваются, образуя орбитали типа А1g + Eg + T1u, ориентированные по линиям, выходящим из вершин октаэдра В6, и ответственные за связи между октаэдрами, а также набор функций, ориентированных вдоль линий, направленных внутрь октаэдра к его центру. Включая двенадцать 2pπ-орбиталей бора, получаем орбитали с симметрией A1g, Eg, 2T1u, T1g, T2g и T2u, описывающие связи внутри каждого октаэдра. Расчеты [53] по методу МО показывают, что из них только A1g, T2g и Т1u (то есть семь орбиталей) будут связывающими. Связи между октаэдрами - обычные двухэлектронные связи, и для заполнения всех связывающих орбиталей структуры нужно 7·2 + (6·2)/2 = 20 электронов. Именно столько их содержится в анионе Bg62-.
В молекуле карбида бора (В4С)n и в анионе (B12H12)2- атомы бора образуют икосаэдр B12. Эта структура имеет очень важное значение, так как ей родственны структуры всех остальных бороводородов и их анионов. Если мысленно удалять атомы бора из аниона (B12H12)2-, то можно получить последовательно структуры большинства бороводородов.
На рис. 14.10 изображен икосаэдр. Существует 120 операций симметрии, переводящих эту фигуру саму в себя. Это число равно порядку группы. Операции разбиваются на десять классов. Поэтому среди НП группы должны быть представлены с размерностью, большей трех [так как даже если бы все НП были трижды вырожденными, то сумма квадратов их размерностей 10·32 = 90 была бы меньше порядка группы (см. стр. 134)]. На самом деле в группе икосаэдра имеются два одномерных представления (Ац и Аи), четыре трижды вырожденных (T1g, T1u, T2g и T2u), два четырежды вырожденных (Ug и Uu) и два пятикратно вырожденных представления (Vg и Vu). Мы не будем строить МО соответствующие такой симметрии, потому что это очень длинная процедура, а только приведем окончательные результаты [54]. Как и ранее, находим, что 2s- и 2рσ-орбитали бора преобразуются таким образом, что можно построить линейные комбинации их, направленные как к центру икосаэдра, так и наружу. В анионе (B12H12)2- эти последние МО описывают двухэлектронные связи В - Н; в соединениях (В4С)n, которые лучше представлять в виде (С32+ - B122-)n, шесть орбиталей описывают связь с другими икосаэдрами, а шесть - связь с группами С3. В случае икосаэдра имеется тринадцать связывающих МО - Ag, T1u, Vg, Uu. Для их заполнения требуется двадцать шесть электронов, и потому для получения структуры с замкнутой оболочкой нужно всего тридцать восемь электронов (двенадцать из них участвуют в образовании внешних связей). Это условие как раз выполняется в соединениях (B12H12)2- и (В4С)n, где имеется 3·12 + 2 = 38 валентных электронов.
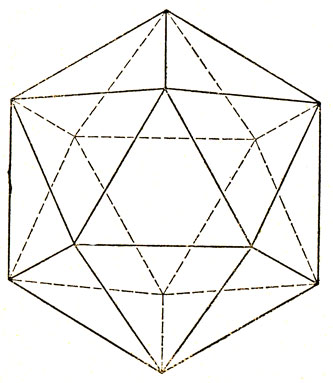
Рис. 14.10. Икосаэдр
Несмотря на существование в икосаэдре осей третьего порядка, простая картина трехцентровых орбиталей не дает адекватного описания структуры в силу того, что каждый атом бора имеет пять ближайших соседей, а из 2s- и 2р-АО невозможно получить пять независимых гибридов. Единственный конструктивный путь описания подобных структур - рассмотрение их как систем делокализованных электронов.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'