
Простая связь
Самое простое органическое соединение - метан. Его молекула состоит из пяти атомов - одного атома углерода и четырех атомов водорода, равномерно распределенных в пространстве вокруг этого центрального атома углерода. Здесь мы сталкиваемся прежде всего с важнейшим постулатом органической химии - во всех незаряженных органических молекулах углерод всегда четырехвалентен. Графически это выражается в том, что он должен быть соединен с химическими символами других элементов или того же углерода четырьмя черточками. В метане все четыре атома водорода находятся на одинаковом расстоянии от атома углерода и максимально удалены друг от друга в пространстве.
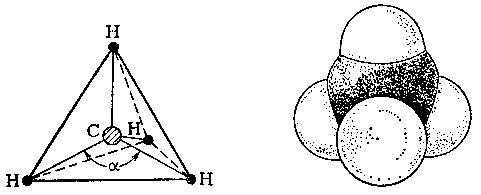
В молекуле метана атом углерода находится в центре правильного тетраэдра, а четыре атома водорода - по его вершинам.
Так выглядит молекула метана с учетом размеров атомов.
Чтобы построить модель молекулы, возьмем тетраэдр, т. е. правильный четырехгранник, составленный из равносторонних треугольников, и поместим в его центр атом углерода. Атомы водорода расположатся по вершинам тетраэдра. Соединим все водороды с центральным атомом углерода. Угол α между двумя такими линиями составит 109 градусов и 28 минут.
Итак, мы построили модель метана. Но каковы размеры молекул в действительности? В последние десятилетия при помощи физических методов исследования (о них речь впереди) удается точно определить межатомные расстояния в молекулах органических соединений. В молекуле метана расстояние между центрами атома углерода и любого водородного атома равно 0,109 нм (1 нанометр, нм, равен 10-9 м). Чтобы представить наглядно, как выглядит молекула в пространстве, пользуются моделями Стюарта - Бриглеба, в которых атомы изображаются шариками определенного радиуса.
Теперь зададимся таким вопросом: какие силы связывают атомы в молекуле органического соединения, почему атомы водорода не отрываются от углеродного центра?
Атом углерода состоит из положительно заряженного ядра (его заряд равен +6) и шести электронов, занимающих различные орбитали* вокруг ядра, каждой из которых соответствует определенный уровень энергии.
*(Орбиталь можно рассматривать как область пространства, в которой наиболее велика вероятность встретить электрон)
Два электрона занимают самую нижнюю, ближайшую к ядру орбиталь. Они всего сильнее взаимодействуют со "своим" ядром и участия в образовании химических связей не принимают. Иное дело - остальные четыре электрона. Считают, что в так называемом невозбужденном атоме углерода, т. е. в отдельном атоме, не образующем никаких связей с другими атомами, эти электроны располагаются следующим образом: два на нижнем подуровне s и два на более высоком подуровне р. Несколько упрощенно и схематично можно считать, что облако, которое образует электрон, находящийся на s-подуровне, имеет форму сферы. Облака р-электронов выглядят объемными восьмерками, причем эти восьмерки могут быть расположены в пространстве вдоль осей х, y и z. В соответствии с этим в каждом атоме имеются три р-орбитали: px, рy и pz. Итак, каждая орбиталь в атоме имеет определенную форму и особым образом расположена в пространстве.
Для того чтобы вступить во взаимодействие с другими атомами, образовать с ними химические связи, атом углерода должен прежде всего перейти в особое, возбужденное состояние. При этом один электрон перескакивает с s-орбитали на p-орбиталь. В результате один электрон занимает сферическую s-орбиталь, а три остальных электрона образуют три орбитали-восьмерки. Однако такое положение атому энергетически невыгодно. Более низкой энергии атома соответствуют четыре одинаковые орбитали, симметрично расположенные в пространстве. Поэтому происходит смешивание, усреднение, или, как говорят, гибридизация имеющихся орбиталей, и в результате получаются четыре новые одинаковые орбитали.
Эти орбитали-гибриды также похожи на восьмерки, но восьмерки однобокие: электронная плотность почти полностью смещена в одну сторону. Такие гибридизованные орбитали обозначаются sp3 (по числу электронов с разных не гибридных орбиталей, участвующих в их образовании: один с s-орбитали и три - с р-орбитали).
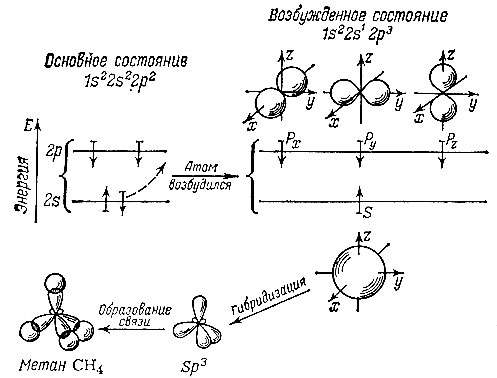
Здесь схематично показана гибридизация орбиталей при образовании молекулы метана. Стрелками показано относительное направление спинов электронов
Как же устроена молекула метана? К каждой из четырех гибридных орбиталей, направленных от атома углерода в разные стороны (а точнее, в углы воображаемого тетраэдра, который можно построить вокруг него), подходят атомы водорода Н. Атом водорода- это ядро с зарядом +1 (для легкого изотопа обычного водорода - просто протон), и один электрон, занимающий сферическую орбиталь вокруг протона. Облака "углеродных" и "водородных" электронов перекрываются, а это и означает образование химической связи. Чем сильнее перекрываются облака электронов разных атомов, тем прочнее связь. Теперь становится понятным, почему гибридизованные орбитали выгоднее - ведь такая однобокая, выпяченная в одну сторону восьмерка может гораздо сильнее перекрываться с облаком водородного электрона, чем менее протяженные в пространстве не гибридные орбитали. Отметим, что эти рассуждения носят несколько условный характер: чистый, так сказать, одиночный и невозбужденный атом углерода не существует реально. Поэтому нет смысла обсуждать, как же в действительности происходят все эти трансформации орбиталей, называемые гибридизацией. Однако для удобства описания химических связей посредством формул и чисел такие условности оказываются полезными. Мы в этом еще не раз убедимся.
Как получить метан?
Один из простейших путей - подействовать водой на карбид алюминия:
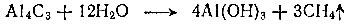
Однако карбид алюминия - слишком дорогое исходное вещество для получения такого обычного, такого дешевого продукта, как метан, и получать его из других соединений нет надобности - ведь природный газ на 85-98 % состоит из метана.
Метан - один из основных "кирпичиков", из которых можно строить органические соединения. Какие же это соединения и как их получить из метана?
Вообще-то метан - вещество сравнительно инертное, и набор химических реакций, которые можно с ним провести, невелик.
Возьмем смесь двух газов - метана и хлора и поместим ее в стеклянный сосуд. Если этот сосуд держать в темноте, то никакой реакции не наблюдается. Но попробуем осветить склянку солнечным светом ..
Квант света взаимодействует с молекулой хлора, в результате молекула расщепляется на две части - два атома хлора:
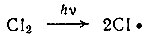
Получившиеся атомы гораздо активнее молекул, они тут же атакуют молекулы метана и захватывают атомы водорода. При этом образуются молекулы хлористого водорода НСl и весьма неустойчивые, очень активные частицы, так называемые метальные радикалы ⋅СН3:
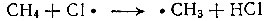
Метальный радикал далее "расщепляет" молекулу хлора:

В результате получается уже известный нам атом хлора (его дальнейшую судьбу нетрудно предугадать: он атакует новые молекулы метана, и все повторяется) и хлорметан, или метилхлорид,- производное метана, в котором один из атомов водорода заменен на хлор.
Реакция, о которой мы рассказали, принадлежит к разряду так называемых цепных реакций, в которых каждая стадия, как в цепи, связана с предыдущей и с последующей. Активные частицы - продукт одной стадии (здесь это атомы хлора и метальные радикалы ⋅СН3) -используются в следующей стадии как исходные вещества. Открытие цепных реакций было одним из крупных событий в истории химической науки, а академик Н. Н. Семенов и английский ученый С. Н. Хиишельвуд за вклад в изучение таких реакций и создание их теории были удостоены Нобелевской премии.
Если в реакцию вводить такие количества реагентов, чтобы на одну молекулу хлора приходилось две молекулы метана, то в основном мы получим хлористый метил СН3Сl. Если же взять хлор в избытке, то реакция замещения пойдет дальше и получится, помимо хлористого метила, еще хлористый метилен СН2Сl2, хлороформ СНСl3 и, наконец, продукт полного замещения водорода на хлор, четыреххлористый углерод ССl4:
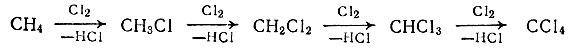
Но не будем забывать о нашей задаче: построить различные сложные молекулы из простых кирпичиков-молекул метана. Для этого нам понадобится метилхлорид. Если подействовать на это соединение металлическим натрием, то из каждых двух молекул СН3Сl образуется одна молекула этана, в которой имеется связь углерод - углерод:

Что такое этан? Это метан, в котором один из водородов заменен на радикал метил ⋅СН3. А сам этот радикал, как мы уже знаем, получается при отрыве от метана одного водородного атома.
Если теперь в этане заместить один из водородов (любой атом) на метил, то мы получим новое вещество - пропан СН3-СН2-СН3. Как это можно сделать практически, мы знаем: сначала в метане и этане заместить один водород на хлор и затем подействовать на смесь метил- и этилхлорида натрием (эта реакция называется реакцией Вюрца в честь французского химика, ее открывшего):
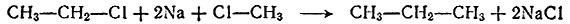
Пойдем дальше. Заместим в пропане один из атомов водорода на хлор. Оказывается, теперь уже не все равно, какой атом замещать! Замещая водород при крайнем атоме углерода (таких атомов два) или же при среднем, мы получим два разных соединения: нормальный пропилхлорид (н-пропилхлорид) и изопропилхлорид:
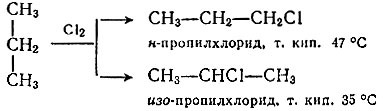
Заменим теперь в каждом из этих соединений атомы хлора на метальные группы. Мы получим два различных бутана - нормальный (т. е. не разветвленный) бутан (н-бутан) и изо-бутан:
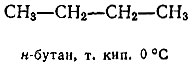
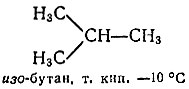
Приставим к полученным молекулам еще по "кирпичику". Начнем с н-бутана. Здесь можно заместить на метил один из крайних атомов водорода. Получим нормальный пентан. Можно заместить один из средних водородов. Придем к изо-пентану. По-видимому, из н-бутана больше ничего нового не получишь. Обратимся к изо-бутану. Если в нем заместить один из крайних водородов (в СН3-группах), то придем к уже упоминавшемуся изо-пентану, а замещая средний единственный атом водорода, получим неопентан:
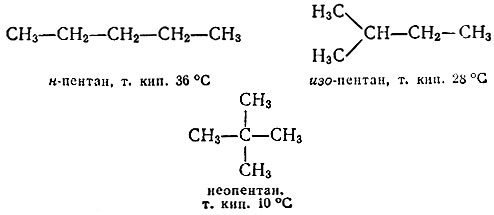
Продолжать эту процедуру можно до бесконечности. Все эти соединения называются углеводородами (точнее - предельными, насыщенными углеводородами, или алканами), потому что состоят они всего из двух элементов-углерода и водорода. В любом алкане число водородных атомов составляет 2n + 2, где n - число углеродных атомов. Поэтому формулу предельного углеводорода можно в общем виде записать так: СnН2n+2.
В построении наших структур мы, надо сказать, во-время остановились. Дело в том, что количество возможных изомеров катастрофически быстро возрастает с увеличением числа углеродных атомов в молекуле алкана. Так, для декана, углеводорода С10Н22, возможно 75 различных изомеров, число изомеров для углеводорода С20Н42 (эйкозан) равно 366 319. Количество же возможных изомеров для тетраконтана, углеводорода С40Н82, даже трудно себе представить: 62 491 178 805 831.
Теперь становится понятно, почему уже сегодня известно такое огромное число органических соединений - несколько миллионов - и почему в этом отношении химия органическая далеко обогнала химию неорганическую. А ведь до сих пор говорилось только о самых простых представителях органических веществ - о насыщенных углеводородах.
Мы выводили ряд изомерных углеводородов из метана, пользуясь реакцией Вюрца. Однако на практике так никто не поступает. Дело в том, что простейшие углеводороды наряду с метаном содержатся в природном газе, состав которого различен для разных месторождений. Например, в газе Северо-Ставропольского месторождения содержится 85 % метана, около 5% этана, 2,5% пропана и 1,4% пентана и более тяжелых углеводородов. Газ Газлинского месторождения состоит из метана на 98 %, этана в нем лишь 1,6 %. Много углеводородов в нефти, но об этом - в следующих главах.
Углеводороды низшие - метан, этан, пропан и бутан - бесцветные газы без запаха или со слабым запахом бензина. Углеводороды от пентана до пентадекана С15Н32 - жидкости и, наконец, высшие углеводороды при обычной температуре - твердые вещества.
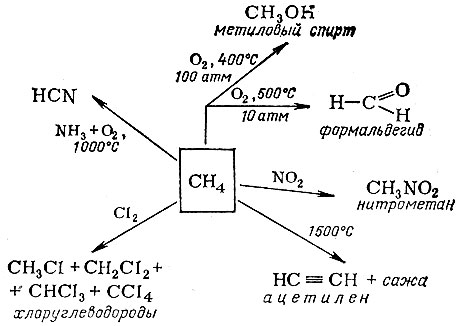
Некоторые примеры использования метана
По мере увеличения числа атомов углерода растет температура кипения и плавления соединения.
У предельных углеводородов есть другое название - парафины, отражающее их химическую инертность (по латыни parum affinis - малое сродство). И все же они довольно широко применяются в химической промышленности для получения самых разнообразных веществ. Основные направления промышленного использования метана показаны на схеме.
Прежде чем закончить разговор о метане и предельных углеводородах, ответим на один вопрос: как осуществляется связь в парафинах между двумя атомами углерода, например, в этане? Здесь все просто - вокруг каждого углеродного атома имеются, как и в метане, четыре гибридизованные sр3-орбитали, три из них осуществляют связи с атомами водорода, а одна перекрывается точно с такой же орбиталью другого углеродного атома. Длина связи С-С составляет 0,154 нм.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'