
Металл соединяется с углеводородом
Вовсе не каждое органическое соединение, содержащее атом металла, называется металлоорганическим, Вот формула ацетата калия.
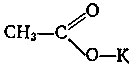
В этой соли есть органическая часть - ацетат-ион, есть и ион металла, но это не металлоорганическое соединение. Истинно металлоорганические соединения - такие, в которых содержится связь металл углерод.
Итак, начнем с металлов первой группы, т. е. со щелочных металлов.
Металлоорганические производные щелочных металлов - одни из самых активных, самых реакционно способных соединений. Эти твердые бесцветные вещества часто загораются на воздухе, с кислотами и водой они реагируют мгновенно, даже со взрывом. Поэтому часто и? не выделяют в чистом виде, а, едва получив на одной из стадий синтеза, сразу же "за* пускают" в дальнейшие превращения. Лучше всего изучены производные натрия и лития.
Металлоорганические производные натрия - это в основном ионные соединения. Получают их действием металлического натрия на галогеналкилы. Например, для этилнатрия:

Это соединение может реагировать дальше с другой молекулой этилхлорида и давать бутан:
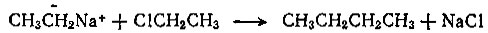
Это уже знакомая нам реакция Вюрца. Итак, один из способов получения углеводородов - не что иное как реакция с промежуточным образованием металлоорганического производного.
Второй пример, когда металлоорганическое производное образуется на промежуточных стадиях реакции - полимеризация непредельных соединений- Именно полимеризацией бутадиена под действием натрия был получен первый советский синтетический каучук (1930 г.). Руководил этой работой выдающийся химик-органик С. В. Лебедев.
Сейчас искусственный каучук, полностью идентичный натуральному, получают действием литийорганических соединений на изопрен. Чаще всего берут бутиллитий. На первой стадии бутиллитий атакует молекулу изопрена, радикал бутил присоединяется к одному концу, литий - к другому (литийорганические соединения построены не ионно, а ковалентно). Новое литийорганическое соединение присоединяется ко второй молекуле изопрена, затем "нанизывается" третья, и так далее, пока не получится длинная полимерная цепь.
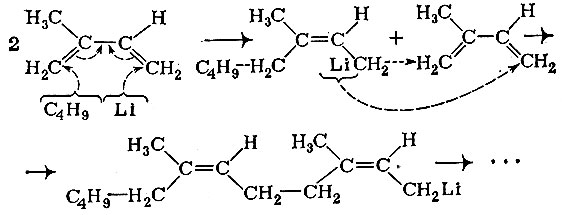
Большое преимущество такого процесса - образуются двойные связи цик-конфигурации. Регулярность структуры резко улучшает свойства каучука и придает ему сходство с натуральным продуктом.
Металлоорганические соединения элементов I группы (в практике чаще всего применяют производные лития) присоединяются не только к углерод - углеродной двойной связи. Охотно реагируют с металлов органическим производным натрия или лития органические соединения, содержащие карбонильную, нитрильную и другие группы. Вот как ревгирует бутиллитий с кетоном:
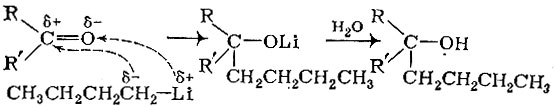
Таким образом, мы из кетона получаем третичный спирт. Происходит образование новой углерод - углеродной связи, а это значит, что такую реакцию можно использовать для синтеза новых органических соединений.
Еще большее значение для органического синтеза имеют открытые в 1900 г. французским химиком В. Гриньяром магнийорганические соединения (мы переходим ко второй группе элементов).
Если стружки магния залить в колбе совершенно сухим эфиром и постепенно прибавлять в колбу какое-нибудь органическое соединение, содержащее галоген, то магний растворится, получится бесцветный прозрачный раствор. Образуется так называемый реактив Гриньяра. Его строение можно записать так:
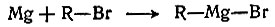
Какие огромные возможности для органического синтеза дают реактивы Гриньяра, видно хотя бы из приведенной здесь сводной схемы.
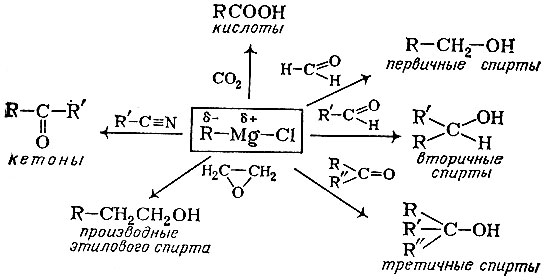
При помощи реактива Гриньяра можно легко получать органические соединения разных классов
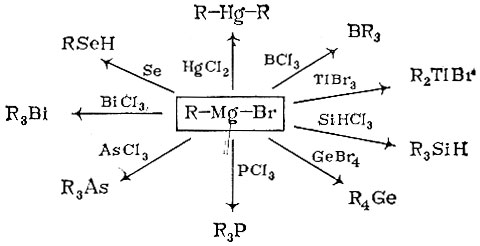
От реактива Гриньяра - к самым разнообразным элементоорганическим соединениям
Достаточно широко применяются в органическом синтезе и производные цинка и кадмия. Первое в истории металлоорганическое соединение - диэтилцинк (C2H5)2Zn - было получено английским химиком Франкландом в 1849 г. А вот металлоорганические соединения Be, Са, Sr и Ва изучены гораздо меньше.
Очень много внимания уделяют химики металлов органическим производным ртути, которые можно получить через уже известные нам реактивы Гриньяра. Впрочем, от магнийорганических соединений можно перейти к производным многих других металлов, да и неметаллов, как показано на схеме. Мы расскажем только о некоторых самых "знаменитых".
III группа периодической системы: алюминий. Алюминийорганические соединения - весьма реакционноспособные, самовозгорающиеся на воздухе вещества - нашли широчайшее применение. В 1953 г немецкий химик К. Циглер (ФРГ) и итальянский химик Дж. Натта обнаружили, что триалкйлалюминий R3AL с добавкой четыреххлористого титана TiCl4 - прекрасный катализатор полимеризации этилена и других олефннов. Катализаторы Циглера - Натта позволяют проводить процесс полимеризации при низком давлении. Именно этому открытию и обязаны тем, что изделия из полиэтилена и других полиолефинов так широко вошли в нашу жизнь. В 1963 г. ученые были удостоены Нобелевской премии.
Получаются же триалкилалюминиевые соединения по способу, открытому Циглером в 1955 г, - действием олефина и водорода на порошок алюминия:
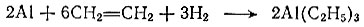
IV группа: германий, олово, свинец (кремний - неметалл, к его органическим производным мы еще вернемся). Все эти металлы четырехвалентны и, следовательно, могут присоединять четыре органических радикала. Наряду с алкилами может быть связан с металлом и галоген. Вот, например, набор соединений, содержащих атом олова, хлор и этил:
SnCl4, C2H5SnCl3, (C2H5)2SnCI2, (C2H5)3SnCI, (C2H5)4Sn
Оловоорганические соединения находят применение в практике - стабилизируют пластмассы, служат для борьбы с грибковыми заболеваниями животных и растений. Но их известность меркнет по сравнению с популярностью ТЭС - так сокращенно называют тетраэтилсвинец (C2H5)4Pb. В 1922 г. было найдено, что небольшие добавки тетраэтилсвинца к бензину резко улучшают его антидетонационные свойства. К великому сожалению, ТЭС - чрезвычайно ядовитое соединение и, разумеется, применение его в автомобилях отнюдь не способствует очищению окружающей среды. Ему сейчас упорно ищут замену.
В V группе менделеевской таблицы находятся два непереходных металла - сурьма и висмут. Для них также известны металлоорганические соединения, их довольно много и некоторые из них даже применяются как лекарственные препараты.
Теперь снова вернемся к началу периодической системы и рассмотрим по порядку органические производные неметаллов (кроме, разумеется, обычных для органики элементов - азота, кислорода, серы, хлора, брома и йода).
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'