
О неорганическом бензоле и удивительных двадцатигранниках
Химикам хорошо известны бораны - бороводороды, состоящие из атомов бора и водорода. Но бораны не органические соединения, ведь в них нет углерода.?
Существуют, однако, и органические аналоги бороводородов, например простейший метилдиборан:
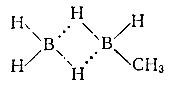
Борорганические соединения, как и бораны, выделяют при сгорании огромное количество тепла и поэтому представляют большой интерес для ракетной техники. Бор образует довольно необычные соединения с водородными мостиками, подобные метилдиборану. Этот элемент вообще склонен к экзотике.
В 1926 г. было получено необычное соединение - шестичленный цикл с чередующимися атомами азота и бора. Похоже на бензол?
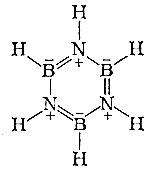
Действительно, свойства боразола - так назвали новое соединение - удивительно похожи на свойства бензола. Боразол - бесцветная жидкость с запахом ароматического соединения. Он кипит при 55 °С, горит, растворяет жиры и другие органические вещества. Получить боразол можно разными способами, например при реакции аммиака с дибораном В2Н6 или действуя борогидридом лития UBH4 на нашатырь NH4CI.
Далее. В 1963 г. под руководством профессора Л. И. Захаркина был осуществлен интереснейший синтез: из бороводорода и ацетилена был получен барен (впоследствии его назвали карбораном).
Барен (а точнее орто-карборан-10) состоит из 10 атомов бора и двух атомов углерода, образующих правильный двадцатигранник (икосаэдр). К каждому атому бора и углерода присоединен атом водорода. Помимо орто-карборана, в котором атомы углерода расположены рядом друг с другом, были получены мета- и пара-карбораны. Удивительна прочность всех этих соединений - их можно нагревать до 600 °С, на них не действуют сильные окислители и кислоты. Это еще не все - карбораны оказались ароматическими системами, атомы водорода при углероде ведут себя, подобно атомам водорода в бензоле.
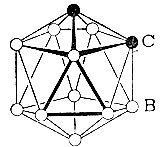
Орто
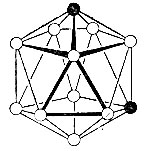
Мета
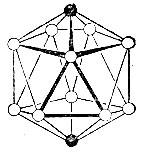
Пара
А теперь посчитайте валентность углерода и бора в этом соединении. Каждый атом связан с шестью другими. Не удивляйтесь. Мы еще столкнемся с соединениями, которые невозможно описать обычной классической теорией валентности.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'