
Отличие ферментов от других видов катализаторов
При изучении свойств ферментов было установлено, что по своему действию они являются катализаторами, в основном обеспечивающими положительный катализ. Поэтому для них характерны все особенности процесса катализа.
Наряду с этим ферменты имеют свои определенные отличия, к которым относятся "космические" скорости катализируемых ими реакций, очень сложная химическая структура, которая в ряде случаев может изменяться в ходе реакции и восстанавливаться в исходную после ее окончания, и, наконец, высокая специфичность действия.
Для подтверждения высокой скорости реакций, катализируемых ферментами, снова обратимся к нашему примеру с перекисью водорода. В организме разложение Н2О2 катализируется ферментом каталазой со скоростью, в 2*1011 раз превышающей скорость некатализируемой реакции и в 107 раз в случае с платиновой чернью. Энергия активации при ферментативной реакции снижается соответственно в 9 и 6 раз. Из других примеров можно указать на следующие. В желудке человека вырабатывается фермент пепсин, который расщепляет белки. Один грамм пепсина за час способен гидролизовать 50 кг яичного белка, а 1,6 г амилазы, синтезируемой в поджелудочной и слюнных железах, за час может расщепить 175 кг крахмала.
Сложность структуры ферментов обусловлена тем, что все они являются белками (см. Структура белков), т. е. высокомолекулярными соединениями с большим молекулярным весом.
Высокая специфичность действия ферментов проявляется в том, что, как правило, каждый фермент катализирует только одну или несколько близких химических реакций.
Действие ферментов как биологических катализаторов можно изобразить следующей формулой:
S + E 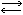 ES → Е + Р,
ES → Е + Р,
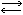 ES → Е + Р,
ES → Е + Р,где Е - фермент; S - субстрат - вещество, на которое действует фермент; ES - фермент-субстратный комплекс, промежуточное соединение, образующееся в ходе реакции типа АК (2); Р - продукты реакции.
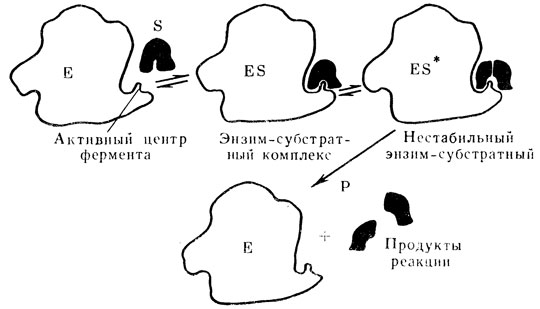
Рис. 38. Схема взаимодействия фермента с субстратом (объяснение в тексте)
И в этом случае действие фермента на субстрат приводит к активированию субстрата, в результате чего снижается энергия активации и повышается скорость реакции. Основное значение в этом имеет образование промежуточного продукта - фермент-субстратного комплекса - ES, скорость образования которого определяет скорость всей реакции. Фермент-субстратный комплекс распадается на фермент и продукты реакции. На рис. 38 дано схематичное изображение хода ферментативной реакции.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'