
Получение безводных хлоридов редкоземельных элементов (С.А Репин)
При разделении изотопов электромагнитным методом в качестве исходных продуктов большей частью применяют хлориды.
Для обезвоживания хлоридов рзэ прибегают к медленной сушке их гидратов в токе сухого водорода, хлористого водорода или азота в вакууме или без него при 70-250° С и выше. Получение безводных хлоридов рзэ представляет значительную трудность.
Клейнхексель и Кремерс [1] еще в 1928 г. описали метод получения безводных хлоридов рзэ. Сущность метода заключается в растворении окислов рзэ в НСl, медленном упаривании растворов хлоридов до кристаллизации и медленном удалении кристаллизационной воды хлористым водородом в вакууме. Однако этот метод трудоемок и малопроизводителен.
Автором настоящей статьи предложены новые методы получения безводных хлоридов рзэ - метод быстрой сушки хлоридов с последующим переводом оксихлоридов в хлориды парами ССЦ при 500 - 650° С и метод непосредственного хлорирования окислов рзэ парами ССЦ при той же температуре.
Предварительно были проведены опыты без применения вакуума. При этом выяснилось, что выпаривание на воздухе растворов хлоридов эрбия и иттербия досуха (первая стадия) приводит к получению гексагидратов с пониженным содержанием хлора. Дальнейшая сушка при 250-300° С дает соли состава Ln2OCl4 (вторая стадия), а при 450- 500° С (третья стадия) получают оксимонохлориды состава LnOCl.
С целью предотвращения гидролиза на первой и третьей стадиях сушки был использован метод обезвоживания солей, применяющийся при весовом определении кремнекислоты (сухую соль смачивали концентрированной НСl и сушили при непрерывном помешивании стеклянным пестиком). Операцию смачивания и выпаривания повторяли еще два раза. Затем повышали температуру до расплавления продукта, подсушивали при помешивании до затвердевания, охлаждали, счищали продукт стальной отверткой со стенок и дна фарфоровой чашки, крупные частицы размельчали 'пестиком; полученное вещество поступало на установку для про-ведения третьей стадии сушки.
Установка (рис. 1) состоит из трубчатой печи 1 (800-1000° С) с диаметром рабочего пространства 40-50 мм, автотрансформатора 2 (2 кв), термопары 3 (1000° С), кварцевой реакционной трубки 4 (один конец ее уже -8-10 мм), диаметром 35-45 мм и длиной ∼700 мм и кварцевой лодочки 5 длиной около 180 мм,
Лодочку с сырым продуктом помещали в зону нагрева кварцевой трубки и проводили сушку в различных газовых средах (в токе сухого воздуха, азота, хлористого водорода и в парах четыреххлористого углерода), соблюдая следующий температурный режим и время:

Как показал анализ, высушивание гексагидрата хлорида методом обезвоживания кремнекислоты повышает содержание хлора в безводном продукте с 15% (в оксимонохлориде) до 25-30%, что приблизительно соответствует оксидихлориду.
Сушка в атмосфере хлористого водорода не имеет преимуществ перед сушкой в атмосфере азота; содержание хлора в сухом продукте постоянное (25-30%).
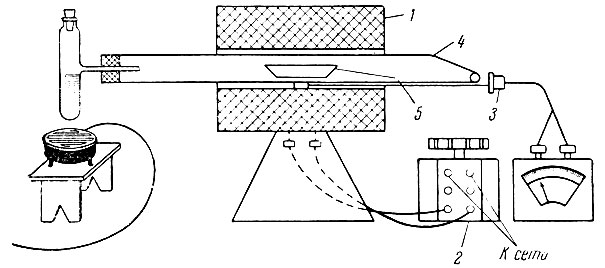
Рис. 1. Установка для сушки хлоридов и хлорирования окислов рзэ. 1 - трубчатая печь; 2 - автотрансформатор; 3 - термопара; 4 - реакционная трубка; 5 - кварцевая лодочка
Для проведения сушки в парах ССЦ к реакционной кварцевой трубке присоединяли при помощи резиновой пробки баллончик-испаритель (v = 60-70 мл), наполовину заполненный ССЦ, под баллончиком устанавливали электроплитку для подогрева ССЦ и при слабом его кипении вели процесс сушки по тому же режиму. Скорость подачи паров ССЦ должна быть такой, чтобы в противоположном конце трубки наблюдалось редкое падение капель (капля в 4-6 сек.!), либо чуть заметное выделение пара. После сушки подачу пара в трубку прекращали, выключали печь, выдерживали лодочку в остывающей печи около 30 мин. и выгружали продукт в сухую тару с резиновой или с хорошо притертой стеклянной пробкой.
Анализ высушенных по этому методу образцов неизменно соответствовал безводному хлориду эрбия или иттербия. Следовательно, то количество хлорокисей, которое образуется на первых двух стадиях сушки сырого хлорида, успешно переводится парами ССЦ в хлориды.
Следует отметить, что хлорирование парами ССЦ образцов, уже прошедших высокотемпературную сушку при 500° С в атмосфере хлористого водорода или азота, происходит чрезвычайно трудно. При необходимости повышения содержания хлорида в соли до теоретического следует растворить образец в НС1 при нагревании и получить безводный хлорид заново по описанному методу.
Непосредственное хлорирование окислов эрбия и иттербия парами ССЦ при 500-650° С (второй метод) проводили на той же установке (см. рис. 1).
Лодочку с 30-40 г Еr2O3 или Yb2O3 вдвигали шомполом в зону нагрева кварцевой трубки. Температуру печи повышали до 500-650° С, одновременно нагнетая в реакционную трубку умеренный ток паров ССЦ из баллончика-испарителя. Процесс хлорирования проводили 4- 4,5 часа при слабом кипении ССЦ (см. метод сушки в ССЦ, стр. 72).
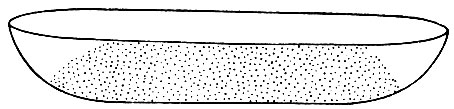
Рис. 2. Схема наполнения лодочки, обеспечивающая равномерное хлорирование окислов рзэ
Если температура печи не превышала 650-700° С, то продукт в лодочке представлял собой слегка сцементированный порошок, довольна легко извлекаемый стальной отверткой. Хлорирование при более высокой температуре приводит к плавлению хлоридов эрбия и иттербия и к возможной порче кварцевых лодочек. При 400-450° С процесс хлорирования замедляется.
Равномерное хлорирование окислов достигается, если лодочка имеет умеренную глубину, т. е. когда ее борта стачиваются несколько больше 7з диаметра трубки, из которой она изготовляется, и когда проба в ней расположена, как показано на рис. 2.
На процесс хлорирования оказывает влияние и структура окисла. Если окислы получены прокаливанием гидроокисей, осажденных аммиаком, то они имеют мелкую плотную структуру и хлорируются медленнее, чем мелкогранулированные пористые окислы, образующиеся при прокаливании оксалатов. Поэтому тонкоизмельченные плотные окислы предварительно переводили в пористые и гранулированные.
Хлорирование окислов парами ОСЬ происходит следующим образом:
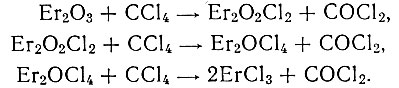
Образующийся фосген также хлорирующий реагент [2, 3], поэтому возможна вторичная реакция:
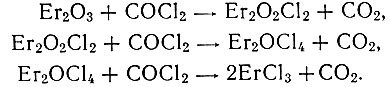
Кроме того, в реакционной трубке протекают побочные реакции, приводящие к сильному загрязнению хлорида газами и твердыми полимерами.
Очистку от этих примесей можно произвести на той же установке. Для этого прекращают подачу паров ССl4 в реакционную трубку (отключают баллончик-испаритель), выключают печь; в остывающей печи выдерживают лодочку 30-40 мин. при 500-550° С. Удаление газов ускоряют продуванием через реакционную трубку сухого азота при той же температуре.
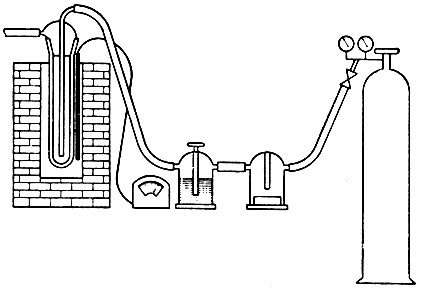
Рис. 3. Установка для обезгаживания хлоридов рзэ
Обезгаживание хлорида можно проводить и на других установках (рис. 3) или в вакуумных сушильных шкафах при 150-200° С и остаточном давлении 0-5 мм рт. ст.
Метод непосредственного хлорирования парами ССl4 применим для хлорирования окислов рзэ, следующих за диспрозием, хотя о гольмии и тулии окончательных данных пока нет.
Реакционная способность ССl4 зависит от основности рзэ, т. е. от радиуса его иона. Иначе говоря, чем меньше основность элемента, тем .легче протекает реакция замещения кислорода окиси на хлор.
Литература
- J. Н. Kleinheksel, Н. S. Kremers. J. Am. Chem. Soc., 50, 954 (1928).
- F. P. Van able, C. Baskerville. J. Am. Chem. Soc., 20, 321 (1898).
- E. Chauvenet. Ann. Chim. Phys., 13 (9), 59 (1920).
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'