
Осаждение редкоземельных элементов из расплавов (В.К. Вальцев, А.А. Камарзин, Н.Ф. Дидора, С. М. Артамонова, Л.X. Кравченко, А. К. Куприянова)
Развитие химии пасплавленных сред как органических, так и неорганических веществ, открывает новые перспективы разделения рзэ.
Нами изучалось поведение рзэ в расплавленных нитратах щелочных металлов и аммония. Нитраты рзэ в расплавленных нитратах щелочных металлов и аммония с сульфатами, оксалатами, фосфатами щелочных металлов, а также со щелочами в расплавленных нитратах щелочных металлов вступают в реакции обмена и в некоторых случаях могут образовывать нерастворимые соединения, которые отделяют от расплавов фильтрованием. Результаты таких опытов показывают, что свойства элементов в разных растворителях могут меняться в зависимости от природы растворителя. Так, например, в расплаве LiNO3 неодим осаждается едким натром, а в расплаве NH4NO3 он не осаждается [1].
Различие в свойствах элементов может быть использовано для их разделения [1]. Эффективность разделения показана на примере пары Nd - Са (табл. 1).
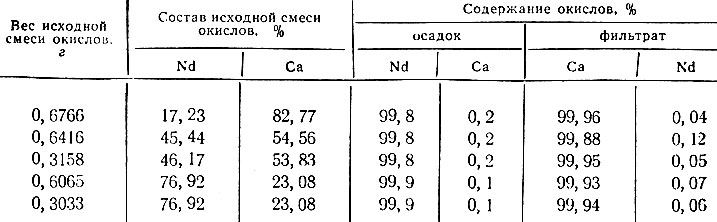
Таблица 1. Результаты распределения неодима и кальция в осадке и фильтрате*. Растворитель - LiNO3, осадитель - NaOH
* (Анализ осадков и фильтратов был выполнен спектральным методом. )
Для изучения состава осадки отделяли от расплавов фильтрованием, промывали расплавленным растворителем и определяли составляющие их компоненты. Фильтрование осуществляли через стеклянные фильтры под вакуумом. Иногда стекло заменяли нержавеющей сталью, стеклянные фильтры - металлическими фильтрами из спрессованного под давлением порошка алюминия зернением 0,2-0,3 мм [1, 2]. Сульфаты и оксалаты щелочных металлов и аммония образуют, как правило, двойные соли, а гидроокиси - осадок состава Ме(ОН)n.
Для изучения процессов, протекающих в расплавах, использовали физико-химические методы исследования: высокочастотное, кондуктометрическое, амперометрическое титрование, спектрофотометрию. Для исследования процессов осаждения наиболее пригодными оказались амперометрия и кондуктометрия.
Кондуктометрический метод титрования
Сущность метода заключается в том, что непрерывно измеряют сопротивление ячейки с расплавом, в которую погружены электроды в строго зафиксированном положении. На рис. 1 приведена полная блок-схема установки для кондуктометрического титрования. С целью измерения сопротивления ячейки с расплавом был применен полууравновешенный мост переменного тока. Напряжение с диагонали мосга подавали на электронный усилитель 1, частота пропускания которого составляла 20-15 000 гц. Усиленный сигнал поступал на фазочувствительный каскад 2% который не реагировал на напряжения, сдвинутые по фазе на 90° С, обусловленные реактивностями ячейки и магазина сопротивлений. Далее, сигнал с катодного повторителя подавали на визуальный прибор 3 или, в случае надобности,- на самописец 4. Ячейка с расплавом находилась в печи, температуру которой можно регулировать в пределах 30-350° С терморегулятором.
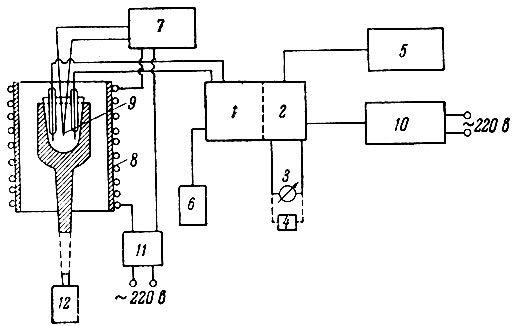
Рис. 1. Блок-схема установки для кондуктометрического титрования. 1 - электронный усилитель; 2 - фазочувствительный каскад; 3 - визуальный прибор; 4- самописец; 5 - звуковой генератор ЗГ-12; 6 - магазин сопротивлений; 7 - терморегулятор ЭПП-09; 8 - печь; 9 - термопара; 10 - стабилизатор; 11 - ЛАТР; 1 - отор
Применяли платиновые электроды в виде проволоки (диаметр 1 мм), запаянные в стекло и закрепленные на крышке печи. При титровании перемешивание осуществляли вращением сосуда с расплавом относительно неподвижно закрепленных электродов. Осадитель добавляли малыми порциями через воронку, помещенную в отверстие крышки печи, и записывали изменение электропроводности системы в процессе, осаждения.
Этим методом было проведено титрование Nd(NO3)3 сульфатом аммония в расплавленном нитрате аммония.
Амперометрический метод титрования
Необходимым условием для применения этого метода к реакциям осаждения было предварительное полярографическое (вольтамперное) исследование реагирующих веществ.
Путем полярографических исследований Nd(NO3)3 и Pr(NO3)3 в расплавленном KNO3 были определены потенциалы полуволн и угловые коэффициенты, а также зависимость высоты волны от концентрации этих элементов в расплаве. При амперометрическом титровании были взяты потенциалы для неодима - 1,1 а, празеодима - 1,0 в.
Ячейка, которую использовали при полярографических исследованиях, а также для амперометрического титрования, представляет собой кварцевый сосуд с диафрагмой.
Катод-платиновая проволока диаметром 1 мм, анод - платиновая пластинка площадью 5 см2. Кроме кварцевого сосуда с диафрагмой, измерение проводили также в фарфоровом тигле без диафрагмы (анод и катод те же). Нами был применен полярограф системы Гейровского марки LP55-2A с автоматической записью. Все измерения проводили при 350° С.
В расплав нитрата калия вводили неодим и празеодим в виде Nd(NO3)3 и Pr(NO3)3, которые готовили сплавлением соответствующих окислов (99%-ной чистоты!) с нитратом аммония. Электроды погружали в расплав на глубину 22 мм.
При исследовании осаждения осадитель добавляли в количестве, недостаточном для полного выделения растворенных рзэ. После перемешивания включали полярограф и записывали предельный ток для растворенного вещества, не прореагировавшего с осадителем. На рис. 2 приведена полученная кривая титрования. При помощи этих кривых изучали стехиометрическое соотношение реагирующих веществ при осаждении неодима и празеодима сульфатом калия в нитрате калия, а также их гидроокисей в нитрате калия. Результаты приведены в табл. 2.
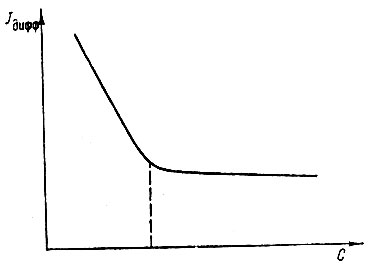
Рис. 2. Зависимость изменения диффузионного тока (Jдифф) от количества добавленного осадителя (С)
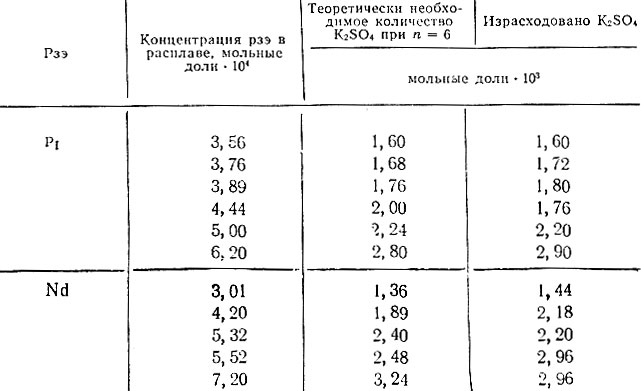
Таблица 2. Результаты титрования празеодима и неодима сульфатом калия в нитрате калия
Оказалось, что при титровании неодима и празеодима в нитрате калия сульфатом калия расходуется значительно больше осадителя, чем при реакции обмена между нитратом рзэ и сульфатом калия. На наш взгляд это объясняется образованием двойных солей по реакции
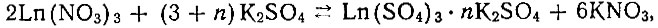
где n - число молекул осадителя. Подобное образование двойных солей по реакции обмена между рзэ и сульфатом аммония в NH4NO3 описано ранее [2]. Число n в реакции с участием неодима и празеодима в интервале всех опробованных концентраций элементов равно шести (см. табл. 2).
В некоторых опытах наблюдались отклонения от значения n = 6. Причина таких отклонений пока не выяснена.
Литература
- В. К. Вальцев, С. М. Артамонова, Л. X. Кравченко. Изв. СО АН СССР, № 5, 59 (1961).
- В. К. Вальцев, С. М. Артамонова, Н. Ф. Дидора, Л. X. Кравченко. Изв. СО АН СССР, № 4, 38 (1961).
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'