
Спектрально-люминесцентное определение некоторых редкоземельных элементов (А.Н. Севченко, В.В. Кузнецова)
Простые соли некоторых рзэ имеют яркую люминесценцию при возбуждении ультрафиолетовым светом 200-300 ммк. Характерная линейчатость видимого спектра люминесценции Eu, Sm, Tb и Dy позволяет обнаруживать довольно малые количества этих элементов (0,001 г-атом!л в растворе и 0,01 ат.% в твердом состоянии для Еu и Тb, 1-5 ат. % для Sm и Dy [1]).
Однако применение флуоресценции для целей анализа затруднено необходимостью употреблять для возбуждения коротковолновое ультрафиолетовое излучение и близостью расположения линий спектра для различных элементов [2].
Исследование люминесценции комплексных соединений рзэ позволило выявить возможность упрощения и повышения чувствительности люминесцентного анализа для некоторых из них. Возможность упрощения анализа связана с тем, что возбуждение люминесценции иона рзэ в комплексе происходит за счет поглощения света органической частью молекулы в области 365 ммк, т. е. светом ртутной лампы. Различия спектрально-люминесцентных свойств комплексов позволяют качественно и количественно определять отдельные рзэ IB смеси.
Органические внутрикомплексные соединения Еu с р-дикетонами, салициловым альдегидом и его производными, салициловой кислотой и ее эфирами, о-фенантролином и α, α'-дипиридилом и многими другими комплексообразующими лигандами обнаруживают интенсивную линейчатую флуоресценцию иона Еu3+ в красной области спектра [3-6]. Некоторые соединения Sm, Tb и Dy с упомянутыми органическими лигандами также обладают люминесценцией, характерной для иона рзэ. Возбуждение иона рзэ в комплексе обусловлено передачей энергии от органической части молекулы к 4f-электрона;м иона, т. е. внутримолекулярной миграцией энергии. Использование различных комплексообразующих лигандов позволило выяснить условия, при которых можно наблюдать люминесценцию иона рзэ в комплексе при возбуждении длинноволновым ультрафиолетом (365 ммк). Миграция энергии в комплексе приводит к появлению люминесценции иона рзэ только в том случае, если резонансный уровень иона рзэ - самый нижний возбужденный уровень комплекса. Если триплетный уровень π-электронов комплекса расположен ниже резонансного уровня иона рзэ, то в спектре испускания комплекса наблюдается полоса фосфоресценции. Свечение иона рзэ в таком случае отсутствует [7, 8].
Так как резонансные уровни различных рзэ не совпадают, то один и тот же комплексообразующий лиганд может давать соединения с различным характером спектра: один рзэ будет люминесцировать в комплексе, другой нет. Самый низкий резонансный уровень среди указанных выше рзэ у иона Еu3+ (17 300 см-1), затем соответственно выше Sm3+ (17 900 см-1), Тb3+ (20 500 см-1), Dy3+ (2100 см-1) и Gd3+ (32 100 см-1). Остальные рзэ имеют очень низкие резонансные уровни, соответствующие им переходы расположены в основном в инфракрасной области и вероятность люминесценции мала [9]. Триплетные состояния комплексообразующих лигандов, образующих в комплексе замкнутые пяти- или шестичленные циклы сопряженных систем, соответствуют уровням, почти всегда расположенным выше резонансного уровня Еu3+. Поэтому Еu3+ ярко флуоресцирует почти во всех исследованных нами внутрикомплексных соединениях в растворе и в кристаллическом состоянии (исключение составляют некоторые производные 8-оксихинолина).
Следует отметить, что в некоторых случаях флуоресценция иона рзэ, отсутствующая у комплекса в кристаллическом состоянии, появляется при переходе комплекса в раствор, что связано с различным положением триплетного уровня для раствора и кристаллического состояния. Так, соединения самария с 8-оксихинолином и этилендиамин-5-нитросали- цилальдегидом и соединения тербия с этими же лигандами и с этилен-диаминсалицилальдегидом не обнаруживают люминесценцию иона рзэ в кристаллическом состоянии. Спектр люминесценции растворов этих соединений принадлежит соответственно Sm3+ и Тb3+. Остальные исследованные соединения обнаруживают спектры Sm3+ и Тb3+ как в растворе, так и в кристаллическом состоянии. Спектр диспрозия обнаруживается у еще меньшего числа соединений (с о-фенантролином, α, α'-дипи- ридилом, ацетил ацетоном, бензоилацетоном, фениловым эфиром салициловой кислоты, пикриновой кислотой и другими). Ион гадолиния не возбуждается, так как его резонансный уровень расположен очень высоко; в спектре испускания наблюдается полоса фосфоресценции комплекса.
В большинстве случаев яркая люминесценция растворов комплекса обнаруживается только при понижении температуры. При комнатной температуре велика вероятность безызлучательной дезактивации энергии, препятствующей передаче энергии иону рзэ. Однако у ряда соединений квантовый выход мало зависит от температуры и близок к единице даже при комнатной температуре. Интенсивность люминесценции комплекса при комнатной температуре сильно зависит от природы комплекса и иона рзэ. Яркую люминесценцию ионов рзэ имеют комплексы с о-фенантролином и α, α'-дипиридилом в кристаллическом состоянии. Можно выбрать такие комплексообразующие лиганды, которые образуют комплекс, имеющий яркую люминесценцию только одного рзэ. Так, например, в нерастворенном комплексе с 5-нитросалицилальдегидом при комнатной температуре ярко флуоресцирует только Еu3+, с этилен- диаминсалицилальдегидом - Sm3+, фениловым эфиром салициловой кислоты - Тb3+. В растворе комплекса с дибензоилметаном ярко флуоресцирует Еu3+.
При температуре жидкого кислорода квантовый выход люминесценции внутрикомплексных соединений европия и тербия близок к единице, что позволяет обнаруживать очень малые количества этих элементов [10]. Например, при возбуждении комплексов с о-фенантролином светом ртутной лампы СВДШ-250 и наблюдении спектра люминесценции обычным спектроскопом нижние границы определения линий в спектре рзэ следующие: Еu еще обнаруживается при разбавлении его La 1 : 50 000, Sm - 1 : 1000, Tb - 1 : 5000, Dy - 1 : 250 при комнатной температуре. При температуре жидкого азота: Еu - 1:500 000, Sm- 1:5000, Tb - I : 100 000, Dy - 1 : 500. Комплекс Eu с дибензоилметаном обнаруживается в растворе при концентрации 10-7 мол/л цри комнатной температуре и 10-9 мол/л при температуре жидкого кислорода (Tb, Sm и Dy при комнатной температуре не флуоресцируют в этом комплексе). В комплексе с фениловым эфиром салициловой кислоты цри комнатной температуре обнаруживается 1 : 10 000 Тb, при низкой температуре- 1 : 50 000 Тb. В случае увеличения мощности источника возбуждающего света и применения спектрографической регистрации спектра люминесценции чувствительность определения рзэ может быть значительно увеличена.
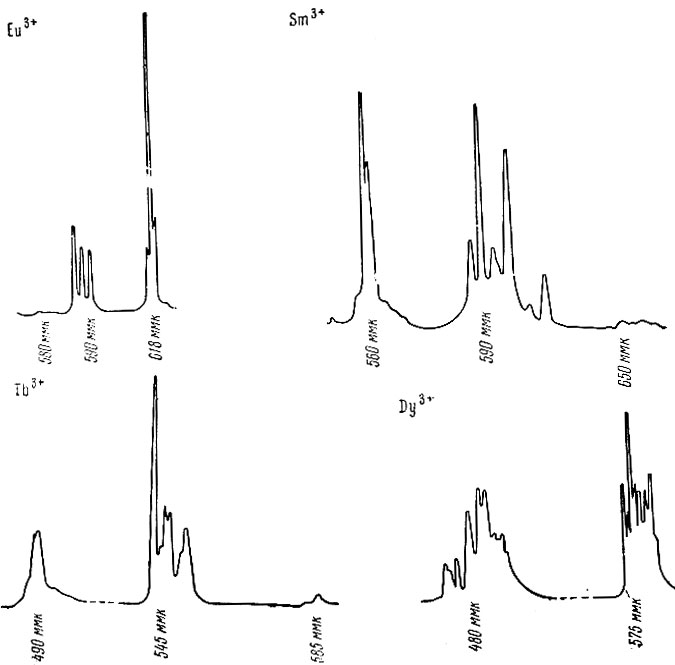
Спектры люминесценции комплексов Eu, Sm, Tb и Dy с о-фенантролином (запись на диаграммной ленте ФЭП-1)
В связи с этим можно быстро осуществлять последовательный качественный и полуколичественный анализ материалов на содержание в них Еu, Тb и Sm. Для одновременного определения сразу четырех элементов следует использовать комплекс с о-фенантролином, в котором люминесцируют все эти элементы. Для каждого из элементов есть соответствующие ему характерные интенсивные линии в спектре:

Спектры люминесценции в видимой области фенантролиновых комплексов Eu, Sm, Tb и Dy приведены на рисунке (стр. 360). Если нужно определить только Ей, то можно использовать комплекс с 5-нитросали-цилальдегидом при комнатной температуре, когда флуоресцирует только Еu3+. Тb легко определяют при комнатной температуре в комплексе с фениловым эфиром салициловой кислоты; Еu и Sm в этих условиях люминесцируют слабо. Для обнаружения Sm можно использовать комплекс с этилендиаминсалицилальдегидом, в спектре люминесценции которого при комнатной температуре наиболее яркая линия Sm3+ λ = 599 ммк. Разбавляя пробу лантаном в определенное число раз (по весу), можно установить границу изчезновения в спектре линий обнаруживаемого рзэ. Зная минимальную обнаружимую концентрацию, можно приближенно определить концентрацию элемента в анализируемой пробе.
Количественное определение Eu, Sm, Tb и Dy основывается на сравнении интенсивности линий спектра исследуемой пробы с интенсивностью линий эталонного образца с известным содержанием соответствующего элемента (комплекс La с примесью соответствующего элемента).
Особенно эффективен предлагаемый метод при анализе суммы рзэ и контроле чистоты их препаратов, так как присутствие остальных элементов не мешает определению Eu, Sm, Тb и Dy.
Ход анализа. Навеску анализируемого материала переводят в азотнокислую соль (избыток HNO3 выпаривают). Соль растворяют в минимальном количестве этилового спирта, приливают раствор комплексообразователя и 30%-ный избыток NaOH по сравнению со стехиометрическим количеством. В случае о-фенантролина и α, α'-дипиридила комплекс образуется при сливании растворов без NaOH. Для качественного анализа комплексное соединение можно приготавливать растиранием порошков в ступке.
Эталонный образец приготавливают при таких же весовых соотношениях количеств соли, комплексообразователя и NaOH.
После отстаивания или фильтрования осадок высушивают на воздухе.
Снимают (спектры полученного и соответствующего эталонного комплекса; сравнивают интенсивности соответствующих линий и определяют концентрации. При записи нужных участков спектра следует устанавливать большую или меньшую чувствительность регистрирующего устройства.
Литература
- Н. Gobrecht, R. Tomaschek. Ann. Phys., 29, 324 (1937).
- Л. В. Левшин, Э. Я. Аралова, Е. Г. Баранова. Тр. Комиссии по анал. химии, 12, 393 (I960).
- J. Weissman. J. Chem. Phys., 10, 214 (1942).
- А. Н. Севченко, А. К. Трофимов. ЖЭТФ, 21, 2 (1951).
- А. Н. Севченко, А. Г. Морачевский. Изв. АН СССР, сер. физ., 15, 628 (1951).
- В. В. Кузнецова, А. Н. Севченко. Изв. АН СССР, сер. физ., 23, 2 (1959).
- В. В. Кузнецова, А. Н. Севченко. Физич. проблемы спектроскопии, 1, 2.36 (1962).
- G. A. Crosby, R. Е. Whan. J. Chem. Phys., 32, 614 (1960).
- М. А. Ельяшевич. Спектры редких земель. М., ГИТТЛ, 1953.
- В. В. Кузнецова. ДАН БССР, 5, 203 (1961).
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'