
4. Оптическая изомерия
Теперь уже необходимо рассмотреть явление оптической изомерии. Ниже кратко описано это явление, а также приведено несколько примеров оптически активных комплексов металлов. Оптическая изомерия была открыта давно. Классические эксперименты, проведенные в 1848 г. Луи Пастером, одним из самых знаменитых ученых, показали, что натрийаммонийтартрат существует в двух различных формах, отличающихся формой кристаллов. Пастер смог их разделить вручную.
Водные растворы двух изомеров обладают способностью вращать плоскость поляризации света (поляризованный луч - луч света, колебания в котором происходят в одной плоскости) либо вправо, либо влево. Это свойство изомеров называют оптической активностью, а сами соединения - оптическими изомерами; одно из них назвали правым (d - dextro), а другое - левым (I - levo) изомерами. Степень вращения плоскости поляризации обоими изомерами одинакова, только d-изомер вращает ее слева направо, а l-изомер - справа налево. Следовательно, в растворе, содержащем оба изомера в равной концентрации, вращения плоскости поляризации, вызываемые этими изомерами, компенсируют друг друга. Такую смесь называют рецематом. Так как этот раствор не вращает плоскость поляризации света, он не активен.
Какое же свойство молекулы или иона делает их оптически активными? Теперь можно дать ответ - асимметрия (отсутствие симметрии). Симметрия оптических изомеров аналогична симметрии правой и левой рук, ног, перчаток или ботинок. Имеется и более тонкое различие в строении: относительные положения большого и остальных пальцев на каждой руке одно и то же, и все-таки обе руки различны - одна является зеркальным изображением другой. Аналогичное положение должно иметь место, если молекула или ион оптически активны. Чтобы молекула или ион были оптически активными, нужно, чтобы они не имели плоскости симметрии, т. е. чтобы нельзя было их разделить на две одинаковые половины. При попытке решить, будет ли данная структура оптически активной, можно использовать иной критерий: для этого необходимо сравнить структуру с ее зеркальным изображением. Если структура и ее зеркальное изображение будут различны, то она будет оптически активной. d- и l-Изомеры данного соединения называют энантиоморфными или энантиомерами, что означает "противоположные формы". Вообще же они имеют одинаковые химические и физические свойства. Различие их заключается только в направлении вращения плоскости поляризации света. Это свойство позволило их открыть и различить. Для этой цели используют очень простой прибор - поляриметр.
Интересно отметить, что иногда физиологическое действие энантиомеров очень различно. Так, l-никотин, содержащийся в природном табаке, значительно более токсичен, нежели d-никотин, синтезированный в лаборатории. Их специфическое действие приписывают асимметричному расположению реакционноспособных групп в биологических системах. Так как энантиомеры очень похожи и обе формы вступают в химические реакции всегда в равных количествах, то для их разделения требуется специальная техника. Процесс разделения называется рацемическим расщеплением. Некоторые методы рацемического расщепления описаны в разд. 10 гл. IV. Часто чистый оптический изомер способен превратиться в рацемат; этот процесс назван рацемизацией.
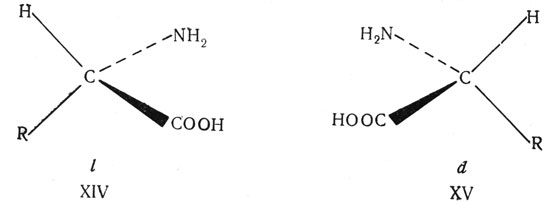
Самым простым примером асимметричной молекулы является тетраэдрическая структура, в которой центральный атом окружен четырьмя разными атомами или группами. Среди органических соединений известно много молекул такого типа. Аминокислоты XIV и XV являются примером строения оптических изомеров. Тетраэдрические комплексы металлов обычно очень реакционноспособны, поэтому их чрезвычайно трудно получить в изомерных формах. Первое сообщение о получении тетраэдрического комплекса металла с четырьмя различными лигандами было сделано в 1963 г., но его рацемическое расщепление пока не осуществлено. Однако комплексы, содержащие два несимметричных бидентатных лиганда, могут быть рацемически расщеплены на оптически активные формы. Оптически активные изомеры этого типа известны для комплексов Ве(II), В(III) и Zn(II). Энантиомеры β-бензоилацетоната бериллия(II) имеют строение XVI и XVII. Надо отметить, что для оптической активности не требуется четырех различных групп вокруг центрального атома; единственным требованием является различие молекулы и ее зеркального изображения.
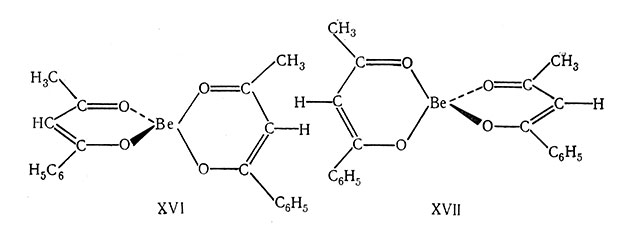
Плоские квадратные комплексы очень редко оптически активны. В большинстве случаев (например, в комплексах типа [MABCD]) плоскость молекулы является и плоскостью симметрии.
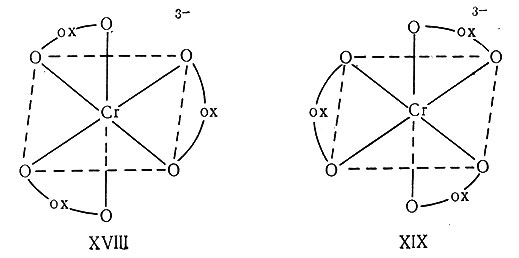
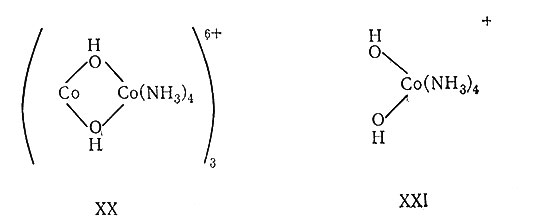
В противоположность системам с координационным числом четыре шестикоординационные комплексы дают много примеров оптической изомерии; очень часто они встречаются среди соединений или ионов типа [М(АА)3], например оптические изомеры триоксалатного комплекса хрома(III), XVIII и XIX. Бидентатные лиганды обычно содержат атом углерода, но известны по крайней мере три оптически активных, чисто неорганических комплекса. Один из них был приготовлен Вернером для доказательства того, что оптическая активность этих систем обусловлена не атомом углерода. Чтобы это продемонстрировать, он использовал мостиковый комплекс XX, в котором бидентатным лигандом служит дигидроксокомплекс XXI. Возможность рацемического расщепления комплексов типа [М(АА)3] на оптические изомеры явилась прекрасным доказательством их октаэдрической конфигурации. Ни тригональные призмы, ни плоские структуры не показали бы оптической активности (табл. 5).
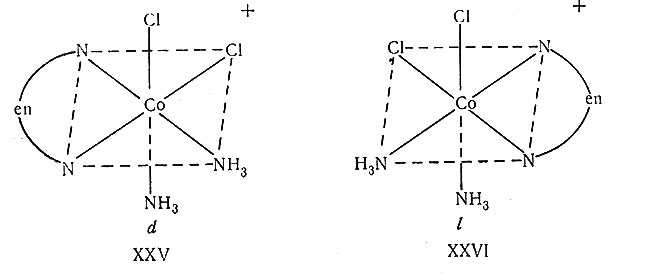
Другой часто встречающийся тип оптически активных комплексов имеет общую формулу [М(АА)2Х2]. В этих системах важно отметить, что транс-изомеры имеют плоскость симметрии и не могут быть оптически активными. Таким образом, если комплекс оптически активен, то ему определенно можно приписать роструктуру. Этот способ доказательства строения используют довольно часто; например, идентификация цис- и транс-изомеров новых комплексов дихлоро-бис-(этилендиамин)родий(III) [XXII, XXIII, XXIV] была проведена этим методом. Один из изомеров [Co(en)(NH3)2Cl2]+ может существовать в неодинаковых формах, одна из которых будет являться зеркальным изображением другой; эти формы были получены (XXV, XXVI) и применены для доказательства цис-цис-структуры комплекса.
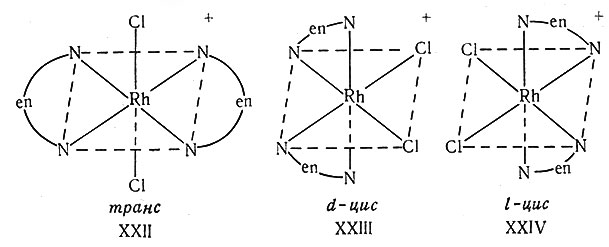
Известно много примеров этого типа и для комплексов платины(IV).
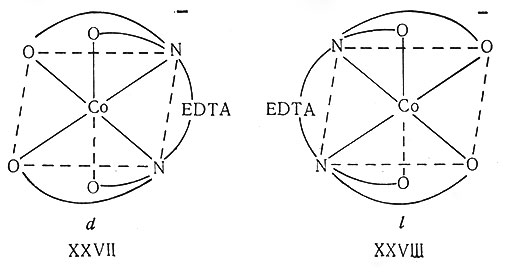
Полидентатные лиганды могут также вызывать оптическую изомерию в комплексах металлов. Один из многих таких комплексов - d- и l-Co(EDTA)]- (XXVII и XXVIII).
Ни в одном из приведенных выше примеров оптическая активность не вызвана наличием шести различных лигандов вокруг центрального атома. В комплексе, содержащем шесть различных лигандов, центральный атом координирует их асимметрично; каждый из его пятнадцати пространственных изомеров рацемически расщеплялся бы на оптические изомеры. Таким образом, одна форма [Pt(py)(NH3)(NO2)(Cl)(Br)(n] имеет оптические изомеры XXIX и XXX.
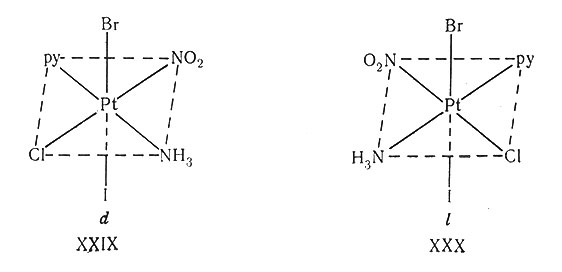
Однако рацемическое расщепление комплекса этого типа пока не осуществлено.
В заключение следовало бы заметить, что обозначение оптических изомеров d и l имеет смысл, только если известна длина волны использованного света. На рис. 24 ясно показано, что оптический изомер может вращать плоскость поляризации света вправо при одной длине волны и влево при другой. Наличие зеркального изображения для изомера обусловливает и зеркальную кривую. Графически выраженная зависимость оптического вращения от длины волны света называется кривой вращательной дисперсии. Она имеет большее значение и более полезна, чем данные просто об оптическом вращении для одной длины волны. Точную конфигурацию (+)Na - [Со(en)3]3+ определили, изучая дифракцию им рентгеновских лучей. Затем, применяя ее 8 качестве стандарта, можно было определить точные структуры других комплексов сравнением их кривых вращательной дисперсии.
![Рис. 24. Кривые вращательной дисперсии и структуры оптических изомеров [Со(en)><sub>3</sub>]<sup>3+</sup>](pic/000091.jpg)
Рис. 24. Кривые вращательной дисперсии и структуры оптических изомеров [Со(en)3]3+
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'