
7. Реакции замещения без разрыва связи металл - лиганд
Найдено, что образование некоторых комплексов происходит без разрыва связи металл - лиганд. При получении солей [Co(NH3)5OH2]3+ из [Co(NH3)5CO3]+ выделяющаяся при реакции двуокись углерода образуется при разрыве связи углерод - кислород, а связь металл - кислород (35) остается неповрежденной. Это было подтверждено проведением реакции в воде, меченой 180. Оба продукта содержали кислород с нормальным
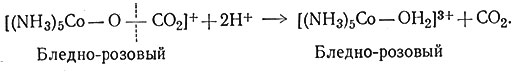
(35)
изотопным составом. Это свидетельствует о том, что растворитель - вода не участвует в реакции, и, следовательно, кислород поставляют реагирующие вещества. Простым, но не решающим доказательством сохранения связи Со - О является тот факт, что реакция протекает полностью сразу же после подкисления карбонатного комплекса. Так как известно, что реакции с разрывом связи Со - О для большинства соединений идут очень медленно, то быстрое течение реакции в этом случае заставляет предположить другой механизм.
Реакции типа (35) довольно распространены; они были применены для получения акво-комплексов из соответствующих карбонатных комплексов. Аналогичным образом могут реагировать такие системы, как [(NH3)5Co - OSO2]+ и [(NH3)5Co - ONO]2+, с образованием [(NH3)5Co - OH2]3+ и выделением соответственно SO2 и NO. Можно ожидать и течение обратных реакций (36).
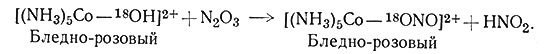
(36)
Такие реакции были детально изучены, и установлено, что они проходят без разрыва связи Со - О. Лучшим доказательством сохранения этой связи явился экспериментальный факт, полученный при исследовании с меченым кислородом; [Co(NH3)5OH]2+ был помечен 18O, и оказалось, что конечный продукт [(NH3)5Co - 18ONO]2+ содержал 99,4% изотопа 18O, первоначально присутствующего в исходном веществе. Естественно предположить, что все реакции гидроксо-комплексов с другими кислотными окислами, такими, как CO2 и SO2, будут протекать аналогично. Так, комплекс [Co(NH3)6CO3]+ можно получить взаимодействием [Co(NH3)5OH]2+ с CO2.
Без разрыва связи металл - лиганд протекает большое число других реакций. По этому типу идут реакции превращения азотсодержащих лигандов в аммиак, например путем окисления роданид-иона (37) и восстановления нитрит-иона (38), причем координированные лиганды часто сохраняют характерные для них химические свойства. Так, PCl3,
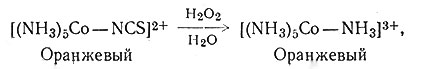
(37)
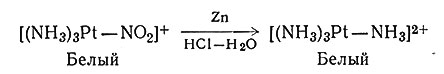
(38)
выполняя функции лиганда, в то же время может подвергаться гидролизу (39) и фторированию (40).
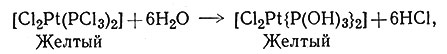
(39)
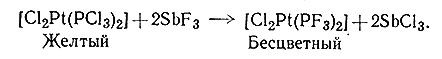
(40)
К числу очень интересных реакций относятся реакции присоединения или замещения органических молекул, координированных ионами металлов. Так, ацетилацетон (асас) (41) образует со многими металлами очень прочные хелатные
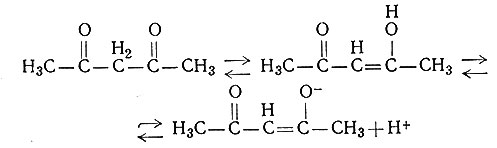
(41)
соединения. Оба комплекса [Cr(асас)3] и [Со(асас)3] устойчивы (равновесие 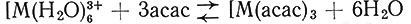 сдвинуто далеко вправо) и кинетически инертны (обмен асас в
сдвинуто далеко вправо) и кинетически инертны (обмен асас в 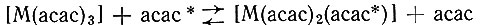 идет очень медленно). Однако комплекс [Cr(асас)3] быстро взаимодействует с бромом в ледяной уксусной кислоте с образованием хелата хрома, в котором атомы водорода в каждом ацетил ацетоновом кольце заменены на атомы брома (42).
идет очень медленно). Однако комплекс [Cr(асас)3] быстро взаимодействует с бромом в ледяной уксусной кислоте с образованием хелата хрома, в котором атомы водорода в каждом ацетил ацетоновом кольце заменены на атомы брома (42).
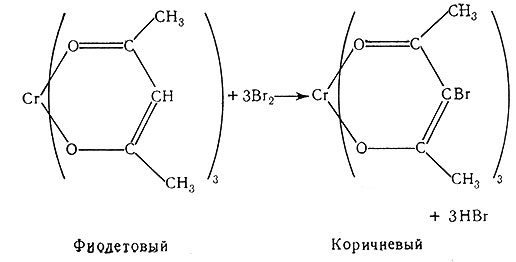
(42)
Подобным же образом были приготовлены иодо- и нитро-соединения, а также аналогичные производные других металлов.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'