
5. Механизм реакций замещения
Теперь нужно рассмотреть приложение кинетических методов, а также других способов определения реакционного механизма. Реакции, в которые вступают координационные соединения, можно разделить на две большие категории: реакции замещения и окислительно-восстановительные реакции. Для каждой из них можно допустить большое число механизмов реакций.
Для реакций замещения различают два основных механизма: диссоциативный и процесс смещения. Оба механизма можно описать общей реакцией замещения в октаэдрическом комплексе (23). Диссоциация предусматривает, что процессом, определяющим скорость всей реакции (медленный процесс), является отрыв лиганда Y с образованием пятикоординационного промежуточного соединения. Последующее же присоединение Z к промежуточному комплексу проходит быстро (24). Такой механизм обозначают SN1, означающим нуклеофильное, мономолекулярное замещение. Реакция является нуклеофильной потому, что входящий лиганд присоединяется к положительно заряженному центру - иону металла (подобно ядру в атоме). Мономолекулярная реакция - это такая реакция, в которой скорость определяющая ступень включает только один вид реагирующих частиц.

(23)

(24)
Механизм смещения или SN2 предусматривает образование семикоординационного промежуточного соединения как медленную стадию и последующую быструю его диссоциацию (25). Эта реакция бимолекулярная, так как в медленной стадии принимают участие два вида реагирующих частиц. Оба механизма можно различить, имея в виду, что в SN1-процессе важную роль играет разрыв связи, а в SN2-процессе - образование дополнительной связи металл - лиганд. Таким образом, обозначения SN1 и SN2 показывают, каково относительное значение для скорость определяющей ступени реакции имеют образование и разрыв связей. Теперь следует рассмотреть некоторые системы, которые были изучены с целью получения сведений о механизме реакций замещения в координационных соединениях.
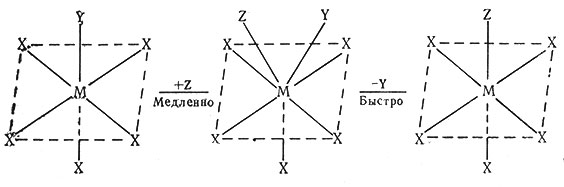
(25)
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'