
Уроки в VII классе
В VII классе учащиеся приобретают лишь первые познания по химии. Ввиду этого научная база для изучения химических производств еще невелика. Поэтому круг химических производств, с которыми можно элементарно ознакомить учащихся в VII классе, также невелик. Это - производство извести, генераторного газа и чугуна. На примере производства извести покажем, как на базе еще небольших познаний по химии можно приступить к первоначальному ознакомлению учащихся с применением законов химии в производстве, с элементами технологии и техники химического производства.
Урок по ознакомлению учеников с производством извести. На изучение производства извести следует затратить один урок после того, как будет дано понятие об основных окислах и щелочах.
В конце урока, предшествующего изложению сведений о производстве извести, следует сообщить учащимся, что в следующий раз будет рассмотрен вопрос о производстве извести и что для этого сейчас ставится химический опыт, который будет закончен без учащихся. Анализ результатов опыта будет сделан на следующем уроке.
Куски известняка или мрамора (СаСO3) кладут в тигельную электрическую печь для прокаливания или в жаровню с раскаленными углями (и учащиеся отпускаются с урока). Прокаливание производится в течение трех часов.
На следующем уроке учитель просит вспомнить, как был поставлен опыт, а затем переходит к анализу его результатов.
В фарфоровую чашку кладут кусочки известняка или мрамора и обливают водой. Никаких признаков химической реакции не наблюдается. Тогда этот же опыт повторяют с кусочками прокаленного известняка или мрамора во второй фарфоровой чашке. Наблюдается энергичное взаимодействие вещества с водой, сопровождающееся обильным выделением тепла. Куски разваливаются.
В первую чашку с кусочками мрамора или известняка, смоченного водой, приливается раствор фенолфталеина. Никаких изменений не наблюдается. Затем проделывается испытание содержимого второй чашки. Фенолфталеин становится малиновым. Учащимся известно, что такое изменение фенолфталеина наблюдается при действии на него щелочи.
На основании этих опытов делается вывод, что при прокаливании мрамора или известняка они превращаются в какое-то новое вещество, которое при взаимодействии с водой превращается в щелочь. Первое вещество называется негашеной известью, второе - гашеной известью. Состав негашеной извести выражается формулой СаО, а состав гашеной извести - Са(ОН)2.
Учитель сообщает учащимся, что при обжиге известняка или мрамора, кроме негашеной извести, получается еще СO2, а потому сущность реакции можно выразить уравнением: СаСO3 = СаО + СO2.
При обливании негашеной извести водой происходит соединение этих веществ с образованием гашеной извести:
СаО + Н2O = Са(ОН)2.
Теперь, когда раскрыты химические основы получения негашеной и гашеной извести, следует рассказать учащимся о том, что эти продукты применяются в строительном деле и в других отраслях народного хозяйства (назвать их). Необходимо рассказать учащимся, для чего и как применяется известь в строительном деле. Раз известь имеет такое большое использование, то, естественно, ее надо производить, так как в природе она не встречается (разъяснить почему).
Как же получается известь в промышленности?
Получение извести основано на применении химических реакций, изученных выше. Для производства извести используют известняк или мел, имеющие в своем составе СаСО3. Обжиг известняка производится в известково-обжигательных печах. Известково - обжигательная печь (рис. 1) представляет собой высокое (около 20 м) сооружение, сделанное из огнеупорного кирпича. В верхней части печи имеется загрузочное устройство, в нижней части-отверстие для вдувания воздуха, а также вращающаяся решетка для выгрузки полученной извести. Углекислый газ, образующийся одновременно с известью, отводится по особой трубе, расположенной в верхней части печи.
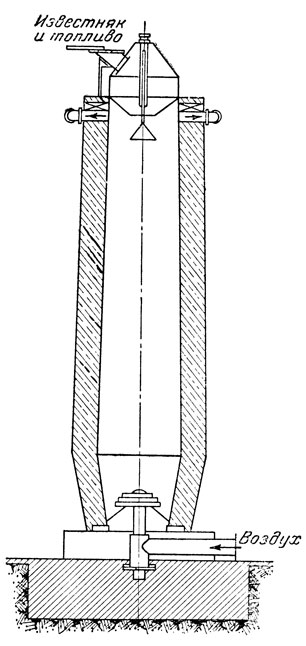
Рис. 1. Известково-обжигательная печь
Печь загружается известняком и топливом (коксом или антрацитом) в кусках величиною приблизительно 5-10 см в поперечнике. Наиболее быстрое разложение известняка происходит в средней части печи, где температура от сгорания топлива достигает 1200°. В нижней части печи полученная известь отдает тепло поступающему в печь воздуху и подогревает его. В верхней части печи происходит подсушивание и нагревание известняка за счет тепла нагретых газов, выходящих из печи. Печь работает непрерывно.
Для закрепления знаний о производстве извести полезно решить следующие задачи:
- Сколько негашеной извести можно получить при обжиге 500 т известняка, если он содержит 5% примесей?
- Сколько воды вступает в химическую реакцию при гидратации 20 т негашеной извести, содержащей 90% СаО?
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'