
Уроки в VIII классе
В VIII классе учащиеся знакомятся с производством соляной кислоты синтетическим способом и с производством серной кислоты контактным способом. Этим начинается ознакомление учащихся с тяжелой химической промышленностью, имеющей решающее значение для химизации народного хозяйства СССР. В процессе изучения серной и соляной кислот кладется начало ознакомлению учащихся с общими научными принципами химического производства: с разделением производственного процесса на фазы, с непрерывным потоком, с применением противотока, оптимальных температур, катализаторов и т. д.
Рассмотрим содержание уроков по ознакомлению учеников с производством серной кислоты.
Серная кислота имеет очень большое значение для химизации народного хозяйства нашей страны, так как находит применение почти во всех отраслях производства. Вот почему ознакомление учащихся с применением и производством серной кислоты предоставляет возможность разъяснить учащимся такие важные для создания политехнического кругозора вопросы, как основная химическая промышленность, химизация народного хозяйства СССР, значение сернокислотного производства в народном хозяйстве страны.
Для ознакомления учащихся с применением и производством серной кислоты отводится четыре урока. На первом уроке учащиеся знакомятся с применением серной кислоты, на втором уроке - с производством сернистого газа, на третьем -с получением серного ангидрида и серной кислоты в лаборатории и на четвертом - с синтезом серного ангидрида и получением серной кислоты на заводах. Учащиеся знакомятся только с контактным способом получения серной кислоты, так как химизм башенного способа сложен для понимания учащихся VIII класса.
Первый урок. К ознакомлению учащихся с применением серной кислоты и народнохозяйственным значением ее следует приступить после изучения свойств серной кислоты. Изложение сопровождается показом продуктов, изготовляемых при участии серной кислоты и демонстрацией таблицы, характеризующей ее значение (см. табл.). Эта таблица изготовляется учащимися на большом листе бумаги. Разъясняя учащимся вопрос о> применении серной кислоты, очень важно добиться понимания ими того, в каких отраслях производства и почему применяется серная кислота и какое значение она имеет для химизации страны.

Применение серной кислоты
Изложение вопроса следует начать с применения серной кислоты в химическом производстве и прежде всего в туковой промышленности, так как последняя является главным потребителем ее, Серная кислота d огромных количествах применяется для изготовления таких широко применяемых удобрений, как суперфосфат, преципитат, сульфат аммония и др.
Огромные количества серной кислоты потребляются нефтяной промышленностью, где она применяется для очистки бензина, керосина и других продуктов.
Серная кислота широко используется в основной химической промышленности. Основная или тяжелая химическая промышленность - это промышленность, вырабатывающая кислоты, щелочи и соли. Она дает полупродукты, которые применяются в различных отраслях промышленности и в сельском хозяйстве. Производство серной кислоты также относится к основной химической промышленности. В основной химической промышленности серная кислота применяется для изготовления разнообразных кислот и солей.
Учащимся предлагается подумать, на чем основано применение серной кислоты для производства кислот. Оно основано на том, что серная кислота является дешевой, сильной и в то же время малолетучей кислотой, вытесняющей другие кислоты из их солей.
Например:
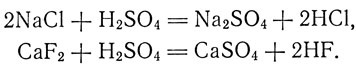
Эти уравнения реакций полезно написать на доске.
Далее предлагается учащимся подумать над тем, благодаря каким свойствам серная кислота получила применение для производства солей. Оно основано настом, что серная кислота, будучи сильной -и двухосновной кислотой, энергично взаимодействует со многими металлами, основными окислами, основаниями и солями, давая кислые и нормальные растворимые и нерастворимые в воде соли. Здесь опять важно написать несколько примеров, иллюстрирующих приведенную выше мысль.
Например:
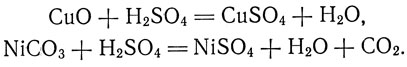
Кислоты и соли, изготовляемые при участии серной кислоты, имеют очень большое значение для народного хозяйства. Эту мысль можно развить на ряде примеров. Например: сульфат натрия применяется для изготовления стекла, соляная кислота - для изготовления красок и лекарств, медный и железный купоросы - для борьбы с вредителями и болезнями сельскохозяйственных растений как инсектофунгисиды и т. д.
Серная кислота применяется также в коксохимической промышленности (получение сульфата аммония), при производстве красителей и лекарственных веществ, в металлургической (очистка металлов) и в других отраслях промышленности.
Таковы главные применения серной кислоты в области химического производства. Нет ни одной области химического производства, где прямо или косвенно не применялась бы серная кислота.
Серная кислота применяется также и в других главных отраслях производства. В машиностроении она применяется для очистки поверхности металлов при никелировании, хромировании, меднении и пр., в энергетике и на транспорте -для зарядки аккумуляторов, в текстильной промышленности серная кислота применяется при белении, отделке и крашении тканей, в пищевкусовой промышленности - для изготовления крахмальной патоки, из которой делают конфеты. Можно с полным основанием сказать, что серная кислота применяется почти во всех отраслях производства. Это обусловлено ее физическими и химическими свойствами, а также дешевизной производства.
Строительство новых химических заводов, внедрение в различные отрасли производства химических продуктов, изготовляемых химической промышленностью, внедрение в различные отрасли производства химических методов обработки материалов называется химизацией народного хозяйства. Серная кислота играет огромную роль в химизации народного хозяйства нашей страны. Отсюда понятно, как велика потребность в широком производстве серной кислоты.
Вопросы и задачи
- Медный купорос применяется в борьбе с сельскохозяйственными вредителями, для приготовления медных красок и разнообразных соединений меди. В производстве его исходят из меди. Как получается медный купорос? Почему для получения медного купороса редко пользуются непосредственным взаимодействием меди с серной кислотой?
- Сернокислое, олово применяется как протрава в текстильной промышленности, для приготовления которой пользуются металлическим оловом или хлористым оловом. Сообразите, как получается сернокислое олово.
- Для получения сернокислой ртути металлическая ртуть обрабатывается концентрированной серной кислотой при нагревании. Напишите уравнение данной реакции.
- Для никелирования металлических предметов применяется сернокислый никель. Его изготовляют, применяя углекислый никель. Сообразите, как получается сернокислый никель.
- Для изготовления сернокислого свинца применяют азотнокислый или уксуснокислый свинец и серную кислоту. Как получается сернокислый свинец?
- Для приготовления белил "Литопон" исходят из сернокислого бария и сернокислого цинка. Как получается "Литопон", если он представляет собой смесь сернистого цинка и сернокислого бария?
- Для получения фосфорной кислоты применяется фосфорнокислый кальций и серная кислота. Напишите уравнение реакции получения фосфорной кислоты. Рассчитайте, сколько серной кислоты придется затратить, чтобы получить одну тонну фосфорной кислоты.
- Плавиковая кислота получается растворением фтористого водорода в воде. Как получить плавиковую кислоту, используя фтористый кальций.
Второй урок начинается изложением основных стадий производства серной кислоты контактным способом. Сначала из некоторых природных материалов, содержащих серу, получают сернистый газ; затем сернистый газ окисляют в серный ангидрид:
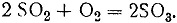
и, наконец, серный ангидрид гидратируют:
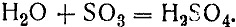
Далее учащимся сообщается план работы на предстоящих трех уроках. Данный урок посвящается ознакомлению с производством сернистого газа.
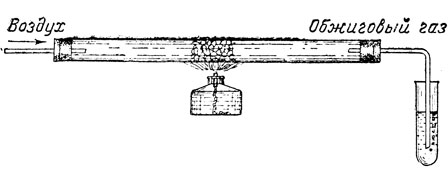
Рис. 2. Прибор для обжига колчедана
В тугоплавкую стеклянную трубку (рис. 2) помещают кусочки железного колчедана (пирита) величиной в гречневое зерно (показать пирит учащимся), затем трубка присоединяется одним концом к газометру с воздухом, а другим концом к пробирке с водой. Пустив ток воздуха из газометра, сильно нагревают железный колчедан в трубке. При температуре около 600° железный колчедан начинает разлагаться с выделением серы:
FeS2 = FeS + S.
Сера сгорает с образованием сернистого газа:
S + O2 = SO2.
Сернистое железо также взаимодействует с кислородом воздуха с образованием окиси железа и сернистого газа:
4FeS + 7O2 = 2Fe2O3 + 4SO2.
Таким образом, в результате этих реакций получаются сернистый газ и окись железа (сернистый газ обнаруживается по запаху).
Описанные выше реакции лежат в основе получения сернистого газа на сернокислотных заводах.
Сырьем для получения сернистого газа является железный колчедан. Если в железном колчедане в качестве примеси содержится больше, чем 1,5% меди, то из него выгоднее предварительно выделить соединения меди для переработки в медь. На медеплавильных заводах отделение железного колчедана от соединений меди производится методом флотации.
В чем заключается метод флотации?
С методом флотации учащихся можно познакомить на следующем опыте. На листе бумаги приготовляется тонкая смесь серы с песком. В банку с водой наливается немного растительного масла и в эту смесь из газометра пропускается воздух (стеклянная трубка опускается почти до дна банки), чтобы образовалась пена; если газометра нет, то воздух продувается пульверизационной грушей. Не прекращая продувания воздуха, в жидкость бросают щепотками смесь серы и песка. Частички серы поднимаются на поверхность раствора, а песок частично оседает на дно, а частично некоторое время остается во взмученном состоянии и потом оседает. Происходит разделение серы и песка. Разделение основано на том, что песок смачивается водой и оседает на дно, а сера не смачивается водой, к ней прилипают пузырьки воздуха, заключенные в масляную пленку, и поднимают серу на поверхность жидкости. Явление, которое было показано в этом опыте, называется флотацией. Флотация заключается в отделении веществ, смачивающихся водой, от веществ не смачивающихся. Флотация - метод обогащения сырья, т. е. повышения в нем содержания вещества, служащего исходным для химического процесса. Флотация широко применяется в современном химическом и металлургическом производствах.
Для отделения пирита от сернистых соединений меди медную руду измельчают в мелкую пыль и затем высыпают во флотационные машины. Резервуар машины наполняется водой с примесью веществ, образующих пену (сосновое масло, деготь и др.), и веществ, затрудняющих смачивание водой минералов, содержащих медь, и облегчающих смачивание водой пирита. При продувании воздуха через эту смесь омасленные пузырьки его прилипают к не смачивающимся водой минералам и поднимают их наверх. Пирит же оседает на дно. Этот осадок собирают и высушивают. Получается мелкораздробленный железный колчедан - флотационные хвосты. Для заводов цветной металлургии флотационные хвосты являются отходом производства, а для сернокислотной промышленности они являются ценным сырьем.
Если сернокислотный завод применяет рядовой колчедан (т. е. кусковой колчедан в том виде, как он встречается в природе), то его предварительно измельчают. Измельчением достигается увеличение поверхности колчедана, что содействует лучшему выгоранию серы при обжиге. Увеличение поверхности реагирующих веществ - один из основных принципов химического производства.
Для получения сернистого газа измельченный колчедан и флотационный колчедан, в смеси или порознь, сжигают в механических печах. Рассмотрим устройство и принцип работы печи ВХЗ (Воскресенского химического завода), сконструированной советскими инженерами.
Печь (рис. 3) представляет собой стальной цилиндр 1, выложенный внутри огнеупорным кирпичем 2. Печь разделена кирпичными сводами 3 на этажи, сообщающиеся между собой посредством отверстий 7, расположенных У стенок печи или у центра свода. В центре печи, сверху Донизу, проходит полый вал 4, который приводится во вращательное движение вместе с гребками 5 и зубьями 6. Зубья в гребках устанавливаются под различным углом так, чтобы на одних этажах колчедан передвигался от Центра к стенкам, на других - наоборот.
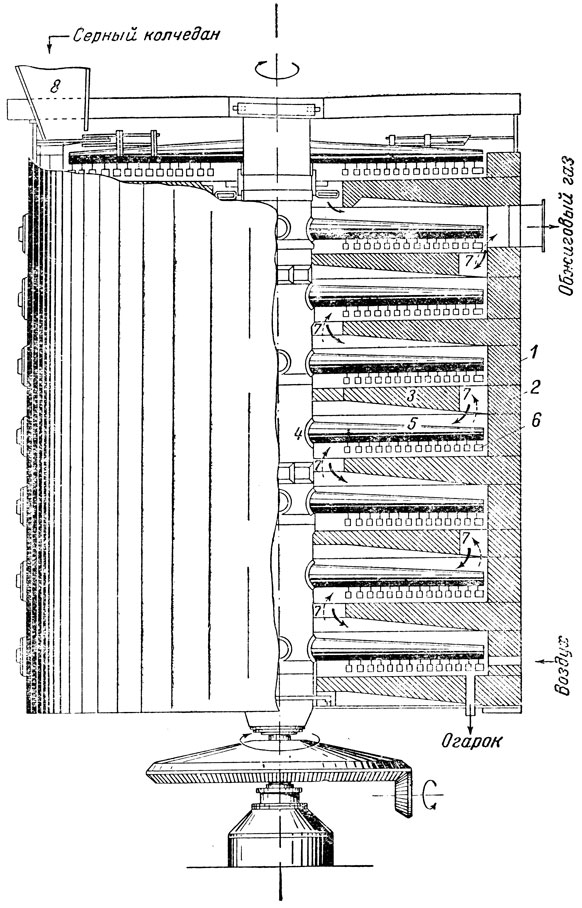
Рис. 3. Печь для обжига колчедана с вращающимися гребками
Измельченный рядовой колчедан (или флотационный) поднимается на верх печи и ссыпается в бункер 8 (большую воронку), откуда поступает на верхний этаж печи. Здесь колчедан подсушивается, гребками передвигается отверстию у центра и ссыпается на следующий этаж. На этом этаже начинается выгорание серы. Движением гребков колчедан перемешивается (что способствует лучшему обжигу), передвигается к отверстию у стенок печи и здесь ссыпается на второй этаж, где выгорание серы продолжается. Обжиг продолжается и на следующих этажах. Внизу колчеданный огарок выбрасывается из печи в вагонетку.
Воздух, необходимый для горения, поступает в печь снизу через отверстия в количестве в 1,6 раза большем, чем надо, благодаря чему достигается избыточная концентрация воздуха, способствующая лучшему обжигу колчедана. Обжиг ведется при температуре около 850°. При более высокой температуре печь быстро разрушается. Воздух проходит над всей поверхностью горящего колчедана. Так осуществляется взаимно противоположное по направлению движение колчедана и воздуха, т. е. противоток. Благодаря противотоку почти до конца обожженный колчедан, в котором содержится мало серы, встречается со свежим воздухом, в котором много кислорода, а поступающий в печь колчедан, хотя и встречается с газами, в которых мало кислорода, но также интенсивно обжигается потому, что содержит большое количество серы.
Итак, в механических печах ВХЗ
- обжиг измельченного колчедана ведется при постоянном перемешивании и непрерывно при оптимальной (наиболее выгодной) температуре 850°, чем достигается наиболее полное использование колчедана и высокая производительность печи;
- воздух поступает в печь в избыточной концентрации в направлении, противоположном движению колчедана (принцип противотока), что также способствует наиболее полному и быстрому выгоранию серы в колчедане.
Непрерывный поток, увеличение поверхности колчедана, противоток, применение избыточной концентрации дешевого материала (воздуха), оптимальная температура обжига - вот основные принципы, обеспечивающие наиболее быстрый и полный обжиг колчедана.
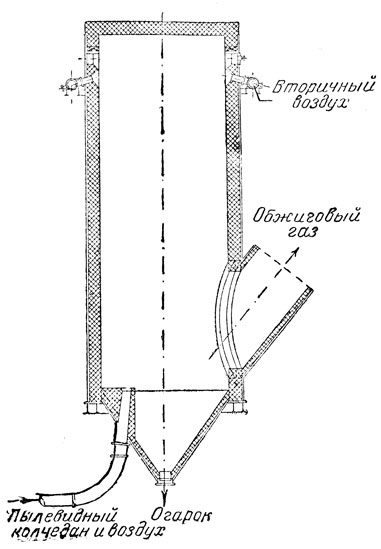
Рис. 4. Печь для обжига колчедана во взвешенном состоянии
Кроме полочных механических печей, в настоящее время применяются также печи для сжигания колчедана в пылевидном состоянии. В печь (рис. 4) форсунками вдувается пыль в смеси с воздухом и здесь сжигается. Для полноты обжига в верхнюю часть печи вводится добавочный (вторичный) воздух. При таких условиях горение идет очень быстро.
Газ, получающийся в печах, называется печным газом. Он имеет примерно следующий состав:
SО2 - 9%, О2 - 8%, N2 - 83%.
Кроме этих составных частей, печной газ содержит еще пыль и различные примеси: водяной пар, серный ангидрид, соединения мышьяка и селена. Последние получаются из примесей, имеющихся в колчедане. Пыль и соединения мышьяка и селена - вредные примеси в газе, загрязняющие кислоту.
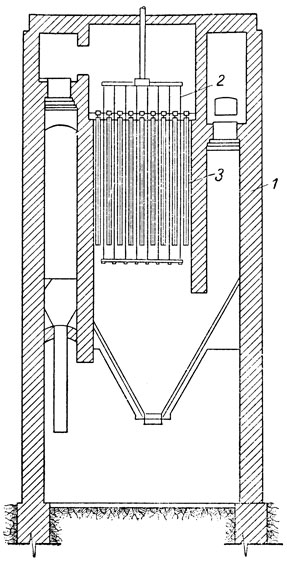
Рис. 5. Электрофильтр для очистки обжигового газа от пыли
Очистка печного газа от пыли производителя в электрофильтрах (рис. 5). Электрофильтр - это камера 1, сделанная из кирпича. Внутри камеры рядами сверху вниз протянуты тонкие хромо-никелевые проволоки 2 и между ними металлические сетки 3. По проволокам пропускается постоянный ток напряжением 50 тыс, вольт. Металлические сетки заземлены. Пылинки, находящиеся в газах, попадая в электрическое поле, заряжаются и притягиваются главным образом сетками, на которых и оседают. Ток периодически выключается, и пыль очищается с сеток постукиванием автоматических молотков. В 1 камерах задерживается 90-98% пыли, содержащейся в газе.
Вопросы и задачи
- Какие материалы применяются в качестве сырья для производства сернистого газа? Напишите уравнения реакций, происходящих при обжиге колчедана.
- Как устроена печь для обжига колчедана?
- Как производится обжиг колчедана?
- Какой состав имеет обжиговый или печной газ?
- Как производится очистка газа?
- Назовите основные принципы производства сернистого газа.
На третьем уроке, после опроса учащихся по материалу предыдущего урока, излагаются научные основы окисления сернистого газа в серный ангидрид и гидратация серного ангидрида с образованием серной кислоты. Изложение проводится на основе Демонстрационного эксперимента.
Серный ангидрид получается при окислении сернистого газа кислородом воздуха:
2SО2 + О2 = 2SО3.
Это обратимая реакция.
Уже давно было замечено, что окись железа, пяти-окись ванадия V2О5 и особенно мелкораздробленная платина ускоряют реакцию окисления сернистого газа в серный ангидрид. Эти вещества являются катализаторами реакции окисления сернистого газа. Так, например, при 400° в присутствии платинированного асбеста (т. е. асбеста, на поверхность которого нанесена мелкораздробленная платина) почти 100% сернистого газа окисляется кислородом воздуха в серный ангидрид. При более высокой температуре выход серного ангидрида уменьшается, так как ускоряется обратная реакция - реакция разложения серного ангидрида на сернистый газ и кислород. При 1000° серный ангидрид почти нацело разлагается на исходные вещества.
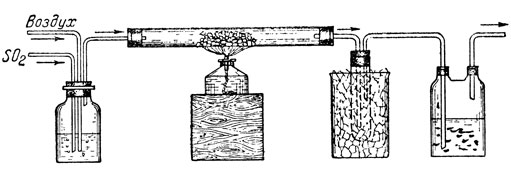
Рис. 6. Прибор для окисления двуокиси серы
Сообщив эти данные, учитель переходит к демонстрации опыта получения серного ангидрида. Объясняется устройство прибора (рис. 6). Показывается газометр с воздухом, прибор для получения сернистого газа, промывалка с серной кислотой для осушения газов, контактная трубка, катализатор, перегонная колба или пробирка для собирания серного ангидрида, охладительная смесь из снега и соли и двугорлая склянка с концентрированной серной кислотой для предупреждения попадания паров воды в приемник с серным ангидридом. Обращается внимание на то, как соединены части прибора. Катализатором может служить прокаленная окись железа, обожженный кирпич, пятиокись ванадия, прокаленный платинированный асбест. После ознакомления учащихся с прибором пускается очень медленный ток сернистого газа и воздуха. Одновременно нагревается катализатор (примерно до 450° при платиновом катализаторе, jXo 500° при ванадиевом катализаторе и до 600° при окиси железа и кирпиче в качестве катализаторов). Ток воздуха устанавливается в 2-3 раза быстрее, чем сернистого газа. Надо следить за тем, чтобы приемник серного ангидрида хорошо охлаждался. Через 8-12 мин. нагревание прекратить и выключить ток газов. Отнять приемник с серным ангидридом от контактной трубки и про-мывалки с серной кислотой. Делать это осторожно, чтобы не выпачкать рук серным ангидридом и чтобы капли его не попали в лицо. Концы трубок приемника серного ангидрида соединить каучуковой трубкой. Контактную трубку соединить посредством пробки со вставленной в нее стеклянной трубкой и каучуковой перемычки (иметь на столе в запасе) с двугорлой склянкой с серной кислотой. Взяв колбу или пробирку с серным ангидридом за горлышко, вынуть ее из охладительной смеси, быстро обтереть полотенцем и показать учащимся. В описанном опыте может получиться или твердый, или жидкий серный ангидрид, или белый "дым". Все зависит от катализатора и других условий опыта.
Следует открыть приемник с серным ангидридом и обратить внимание на выделение тяжелых клубов белого дыма. Делать это под тягой, а если тяги нет, то возле окна с открытой форточкой. Длинной сухой стеклянной трубкой осторожно захватить немного серного ангидрида и опустить в стакан с водой. Наблюдается шипение и разогревание. В стакан прилить раствора лакмуса фиолетового цвета. Он краснеет. Колбу или пробирку с серным ангидридом оставить на воздухе под тягой или между рамами окна. Обратить внимание учащихся на то, что через некоторое врем"я твердый серный ангидрид становится жидким.
Все эти опыты должны быть тщательно проанализированы и усвоены учащимися.
Опираясь на эти опыты, учитель должен изложить вопрос о научных основах получения серной кислоты контактным способом. Этот способ называется так потому, что серный ангидрид, необходимый для получения серной кислоты, получается при соприкосновении (контакте) сернистого ангидрида и кислорода с катализатором. Применение катализаторов - первое условие, которое выполняется в производстве серной кислоты этим способом. Чтобы обеспечить возможно более полное превращение исходных веществ (сернистого газа и кислорода воздуха) в серный ангидрид, синтез ведут при оптимальной температуре. Так как сейчас на наших заводах применяется ванадиевый катализатор, то процесс ведут при температуре 450-600°, обеспечивая окончание окисления при температуре не выше 480°. Печной газ тщательно очищается и осушается, так как примесь в газах соединений мышьяка и селена и водяного пара делают катализатор неактивным (отравляют катализатор).
Серный ангидрид поглощается 98% серной кислотой. Применять воду или разбавленный раствор серной кислоты для поглощения серного ангидрида нельзя, так как над ними всегда находится водяной пар. Он реагирует с серным ангидридом с образованием туманообразной серной кислоты. А она не поглощается никакими жидкостями.
Вопросы и задачи
- Напишите уравнения реакций получения серной кислоты, исходя из сернистого газа.
- При каких условиях происходят эти реакции?
- Какие свойства имеет серный ангидрид?
На четвертом уроке учащиеся знакомятся с техникой производства серной кислоты контактным способом. Процесс производства разделяется на следующие стадии:
- дополнительная очистка сернистого газа,
- окисление сернистого газа в серный ангидрид в контактном аппарате,
- поглощение серного ангидрида 98% серной кислотой. Демонстрируется схема производственного процесса (рис. 7 а, б и в).
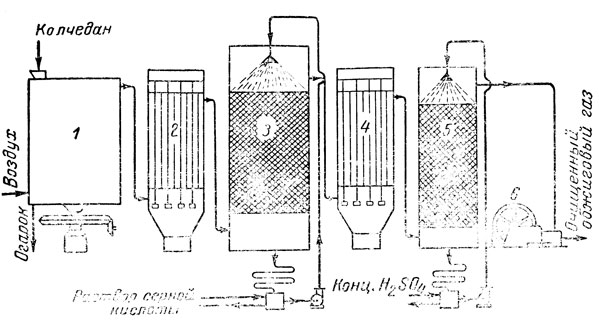
Рис. 7а. Получение и очистка обжитого газза
Печной газ в описанном выше электрофильтре 2 (рис. 7а) очищается от пыли не полностью. Кроме того, он содержит вещества, отравляющие катализатор. Поэтому он направляется на дополнительную очистку сначала в башни 3, орошаемые раствором серной кислоты. Демонстрируется схема устройства промывных башен. Здесь также осуществляется принцип противотока. Печной газ движется снизу вверх, а кислота разбрызгивается вверху и стекает по насадке из керамических колец вниз. Насадка увеличивает поверхность соприкосновения газа с кислотой. Очищенный от пыли, охлажденный и увлажненный газ проходит через электрофильтр 4 для очистки от мышьяковистого ангидрида As2О3, который является особенно опасным ядом для катализатора. Здесь же происходит очистка газов от туманообразной серной кислоты. Далее газы направляются в сушильную башню 5, орошаемую крепкой серной кислотой, которая, как известно, хорошо поглощает влагу. Из сушильных башен газы поступают в компрессор 6, проталкивающий их через остальные аппараты установки. Башни снабжены водяными холодильниками, сборниками и насосами.
Окисление сернистого газа в серный ангидрид происходит в контактных аппаратах.
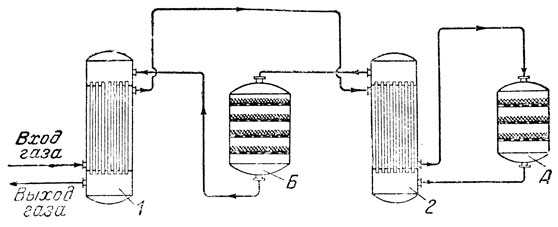
Рис. 7б. Окисление двуокиси серы
Газы проходят через теплообменники 1 и 2 (рис. 7б), где они подогреваются до 450° и затем направляются в контактный аппарат А. Из этого контактного аппарата, где окисляется около 80% сернистого газа, а температура газов поднимается до 580° (за счет теплоты реакции), газы направляются в теплообменник 2. Здесь они отдают тепло стенкам трубок, по которым газ идет в контактный аппарат, и, охладившись до 450°, направляются во второй контактный аппарат Б. В этом аппарате окисляется остальной сернистый газ и газы, содержащие серный ангидрид, поступают в теплообменник нагревая там своим теплом холодный газ, направляющийся в контактный аппарат.
Теплообменник представляет собой стальной цилиндр, скрытый слоем нетеплопроводных материалов (демонстрируется схема устройства и разборная модель теплообменника). В нем укреплены две решетки, в отверстия которых вставлены открытые с концов трубки. Газы, направляющиеся в контактный аппарат, проходят между трубками, а газы, направляющиеся из контактного аппарата, проходят по трубкам и передают через стенки трубок свое тепло холодным газам. Отсюда и название аппарата - теплообменник. Устройство аппарата предупреждает смешение газов, обеспечивая в тоже время обмен теплом.
Контактный аппарат (демонстрируется схема устройства и разборная модель контактного аппарата) представляет собой стальной цилиндрический котел с решетчатыми полками.
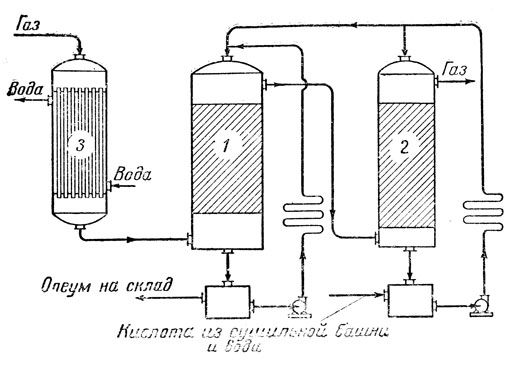
Рис. 7в. Поглощение серного ангидрида
Поглощение серного ангидрида производится в башнях (рис. 7 в). Из теплообменника газы идут в холодильник 3, а затем в две последовательно соединенные поглотительные башни 1 и 2 (демонстрируется схема устройства такой башни). Башни изготовляются из стали и выкладываются внутри кислотостойким кирпичом. Для увеличения поверхности соприкосновения башни наполняются керамическими кольцами. В первой башне серный ангидрид поглощается олеумом, во второй башне 98%-ной серной кислотой. Башни снабжены сборниками, насосами и водяными холодильниками.
Таким образом, основными принципами производства серного ангидрида и поглощения его являются непрерывный поток, применение оптимальных температур, применение катализаторов, противоток, теплообмен, увеличение поверхностей взаимодействующих веществ.
В конце урока следует упомянуть о башенном способе, сказав, что здесь сернистый газ окисляется окислами азота в башнях. Тут же в башнях получается и серная кислота. Надо указать учащимся, что вся работа по управлению сернокислотными заводами строится на научных основах. Лаборатория посредством разных способов и приемов, в том числе и автоматических приборов и анализаторов, исследует сырье, состав продуктов на различных стадиях производства, качество продукции и т. д. Опираясь на данные этих анализов, управляют аппаратами и техническим процессом в целом.
До революции в России сернокислотная промышленность не была развита, так как промышленность и сельское хозяйство были крайне отсталыми. Спрос на серную кислоту вследствие этого был крайне невелик. В 1913 г. было произведено всего лишь 110 тыс. т серной кислоты.
После Великой Октябрьской социалистической революции, когда началась социалистическая реконструкция промышленности и сельского хозяйства, стало расти и производство серной кислоты. За годы пятилеток в СССР создана мощная сернокислотная промышленность, дающая серной кислоты в десятки раз больше, чем в дореволюционное время.
Согласно директивам XIX съезда КПСС, будет осуществлен дальнейший рост производства серной кислоты.
Сернокислотное производство служит важным фактором химизации народного хозяйства нашей страны, непрерывного роста и совершенствования производства на базе высшей техники.
Вопросы и задачи
- Напишите уравнение реакций получения серной кислоты контактным способом.
- При каких условиях совершается окисление сернистого газа в серный ангидрид?
- Назовите основные фазы, на которые разделяется производственный процесс получения серной кислоты контактным способом.
- Назовите сырье для получения сернистого газа.
- Какой состав имеет уральский колчедан? Что такое флотационный колчедан и как он получается?
- Какая связь существует у заводов сернокислотной промышленности с заводами цветной металлургии?
- Сколько тонн сернистого газа можно получить при обжиге 1 т колчедана, имеющего 48% серы, если в огарке остается 1,5% серы?
- Как устроены промывные башни, контактный аппарат, теплообменник, поглотительные башни?
- Перечислите основные принципы производственного процесса получения серной кислоты.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'